АДСОРБЦІЙНО-РЕОЛОГІЧНІ ВЛАСТИВОСТІ СИНОВІАЛЬНОЇ РІДИНИ У ХВОРИХ НА РЕВМАТОЇДНИЙ ГОНІТ
Синяченко О.В.1, Лукашенко Л.В. 2
- 1Донецький національний медичний університет ім. Максима Горького
- 2Донецкий медицинский университет им. Максима Горького
Резюме. Резюме. При ревматоїдному артриті підвищуються порівняно з показниками сироватки крові об’ємна в’язкість, в’язкоеластичність, рівноважний поверхневий натяг і релаксація синовіальної рідини, при цьому її інтегральні характеристики адсорбційно-реологічних властивостей пов’язані з віком хворих, наявністю кіст Бейкера та лімфаденопатією, а окремі параметри залежать від ступеня активності захворювання, поширеності суглобового синдрому, його тяжкості й темпів прогресування, наявності інтраартикулярних хондромних тіл, тіл Пеллагрі — Штайді та Гоффа, а також екстраартикулярних (системних) ознак хвороби, причому порушення адсорбційно-реологічного стану синовіальної рідини беруть участь у патогенетичній основі захворювання, а показники інтегрального адсорбційного індексу можуть мати прогностичне значення.
Введение
Как известно, исследование синовиальной жидкости (СЖ) относится к наиболее информативным и доступным методам диагностики (дифференциальной диагностики) заболеваний суставов (Чернякова Ю.М., Сементовская Е.А., 2008; Brannan S.R., Jerrard D.A., 2008). В настоящее время при изучении синовиального ликвора используют методы поляризационной микроскопии, культур клеток, фильтрования в агарозном геле, электрофореза, радиоиммунного и иммуноферментного анализа, полимеразной цепной реакции, жидкостной хроматографии, спектрофотометрии, ядерно-магнитной спектроскопии, иммуногистохимии, цитохимии (авидинбиотинпероксидазная реакция, желатиназная зимография) и др. В наших предыдущих работах (Синяченко О.В., 2009; 2012; Синяченко О.В. (ред.), 2011) подчеркнута особая клиническая значимость при артикулярной патологии исследования физико-химических адсорбционно-реологических свойств синовиальной жидкости (АРСС), что быстро и точно (ошибка измерений не превышает 0,1%) позволяет четко проводить диагностику заболеваний суставов и надежно контролировать ход лечебных мероприятий.
В состав СЖ входят протеины (Jablonka A. et al., 2012; Zamani B. et al., 2012), пептиды, небелковые азотистые продукты (Chenevier-Gobeaux C. et al., 2012), гормоны, ферменты (Zamani B. et al., 2012), адипокины (Hulejova H. et al., 2012), липиды (Oliviero F. et al., 2012; van Beers J.J. et al., 2012), цитокины и факторы роста (Fiocco U. et al., 2012; Gordon R.A. et al., 2012), способные изменять АРСС, и как следствие — и лубрикантные характеристики данной биологической жидкости. Протеино-липидные поверхностно-активные вещества (сурфактантны) и неорганические инсурфактанты СЖ разнонаправленно изменяют межфазную (поверхностную) активность на границе воздух/СЖ. Исследования АРСС могут быть основаны на методах максимального давления в пузырьке, анализа формы осесимметричных и осциллирующей капель, для которых достаточны микрообъемы жидкостей (Collins G.W. et al., 2008; Ren H. et al., 2010; van Steijn V. et al., 2010; Rosenfeld L., Fuller G.G., 2012).
За последние годы с помощью компьютерных тензиометров появилась возможность в интегральном виде определять содержание сурфактантов/инсурфактантов в биологических жидкостях, оценивать поверхностные вязкость (m) и упругость (r), суммарный модуль вязкоэластичности (e), динамическое поверхностное натяжение (s) и состояние релаксации (t) (Kotsmar C. et al., 2009; Fainerman V.B. et al., 2010). Целью и задачей данной работы стали изучение АРСС у больных c разными вариантами течения ревматоидного артрита (РА) по сравнению с аналогичными при гонартрозе с синовитом (контрольная группа) и с показателями сыворотки крови, а также выяснение факторов, определяющих физико-химическое состояние суставного ликвора, и оценка его патогенетической значимости.
Материалы и методы исследования
Изучение СЖ, которую получали из коленных суставов в случаях ревматоидного гонита (РГ), выполнено у 35 больных в возрасте от 29 лет до 61 года (в среднем — 46,7±8,99±1,52 года) и 27 — гонартрозом с синовитом в возрасте 40–63 лет (в среднем — 50,5±5,40±1,04 года). Среди пациентов с РА было 20% мужчин и 80% женщин в возрасте 50,1±7,15±2,70 и 45,9±9,31±1,76 года соответственно. Длительность РА составила от 3 до 28 лет (12,2±6,11±1,03 года). II степень активности РА констатирована в 49% наблюдений, III — в 51%, I рентгенологическая стадия патологического процесса установлена в 6% случаев, II — в 43%, III — в 34%, IV — в 17%. Серопозитивный вариант болезни на момент обследования имел место у 77% числа больных, экстраартикулярные (системные) признаки — у 43%. Индекс Лансбури составил 218,9±71,98±12,17 балла, индекс тяжести артрита (ИТА) — 180,0±125,18±21,16 о.е., индекс прогрессирования артрита (ИПА) — 1,9±1,39±0,24 о.е. Тендовагинит диагностирован в 66% наблюдений, энтезопатия — в 49%, дигитальный артериит, лимфаденопатия и синдром Шегрена — соответственно в 6%, миозит или миалгии, изменения эндокарда и клапанов сердца — соответственно в 20%, поражение миокарда (миокардит, миокардиодистрофия) — в 29%, легких (интерстициальный пневмофиброз, ревматоидные узлы) — в 17%, печени — в 11%, почек (гломерулонефрит, амилоидоз) и серозных оболочек (плеврит, перикардит) — соответственно в 9%, периферической нервной системы — в 26% наблюдений.
Пациентам выполняли рентгенологическое (аппарат «Multix-Compact-Siеmens», Германия), ультразвуковое (аппарат «Envisor-Philips», Нидерланды) и магнитно-резонансное (томограф «Signa-Excite-HD», Германия) исследование коленных суставов, а также выполняли двухэнергетическую рентгеновскую остеоденситометрию проксимального отдела бедренной кости (аппарат «QDR-4500-Delphi-Hologic», США).
Межфазную тензиореометрию надосадочного слоя после центрифугирования СЖ и сыворотки крови проводили с использованием компьютерных аппаратов «MPT2-Lauda» (Германия), основанного на методе максимального давления в пузырьке, «ADSA-Toronto» (Германия — Канада), основанного на методе анализа формы осесимметричных капель, и «PAT2-Sinterface» (Германия), основанного на методе осциллирующей капли. Изучали m, r, e и t, а также s при времени существования поверхности, равном 0,01 с (s1), 1 с (s2) и 100 с (s3), оценивали равновесное (статическое) s при t→∞ (s4). В наших исследованиях применялась быстрая стрессовая деформация расширения поверхности капли (при t=1200 с), после чего s медленно релаксировало, возвращаясь к первоначальному значению. Релаксационные свойства СЖ и сыворотки крови характеризовали способность монослоя восстанавливать исходное состояние (Miller R., Liggieri L. (Eds), 2009). Кроме того, мы подсчитывали угол наклона (l) и фазовый угол тензиореограмм (j), а также интегральный адсорбционный коэффициент (w) по формуле:
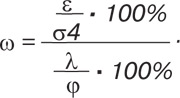
С помощью ротационного вискозиметра «Low Shear-30» (Швейцария) исследовали объемную вязкость (h) биологических жидкостей.
Статистическая обработка полученных результатов исследований проведена с помощью компьютерного вариационного, корреляционного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы «Microsoft Excel» и «Statistica-Stat-Soft», США). Оценивали средние значения (M), стандартные отклонения (SD) и ошибки, коэффициенты корреляции, критерии дисперсии, Стьюдента, Уилкоксона — Рао и достоверность статистических показателей.
Результаты и их обсуждение
Показатели h СЖ у больных РА составляют 2,7±0,66±0,11 мПа•с, m — 16,7±2,40±0,41 мН/м, r — 41,8±13,14±2,22 мН/м, e — 37,6±5,76±0,97 мН/м, s1 — 62,0±4,29±0,72 мН/м, s2 — 60,2±4,65±0,79 мН/м, s3 — 57,0±4,24±0,72 мН/м, s4 — 53,3±5,33±0,90 мН/м, l — 8,0±3,37±0,57 мН/мс, j — 208,4±53,2±8,99 мН/мс, w — 23,5±14,80±2,50 о. е., t — 512,9±80,18 с. По сравнению с больными гонартрозом (рис. 1), при РГ выявлено достоверное снижение на 77% параметров h, на 16% — e, на 12% — s1, на 11% — s2, на 9% —s3, на 32% — l при повышении на 14% — s4 и на 32% — t. Как видно из рис. 2, отдельные параметры АРСС у больных с серонегативным и серопозитивным РА мало отличаются между собой. Можно отметить лишь определенную тенденцию повышения параметров l СЖ (на 35%) в случаях наличия ревматоидного фактора в периферической крови (как известно, l отражает общее адсорбционное состояние любой жидкости).
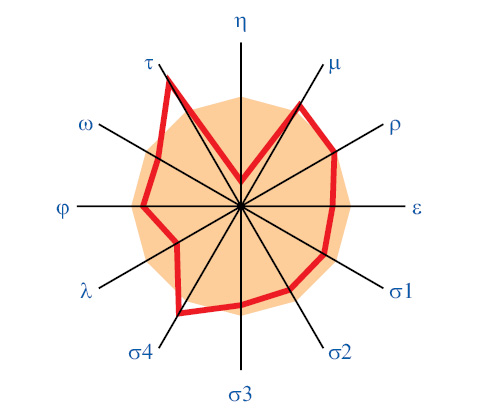
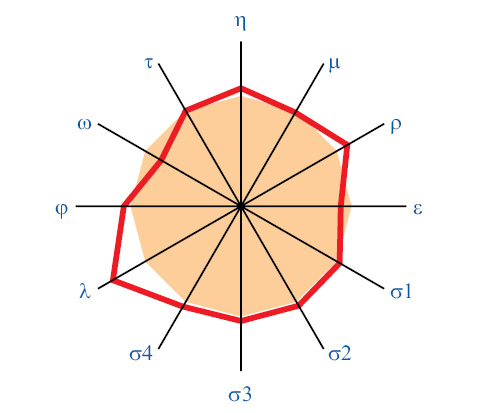
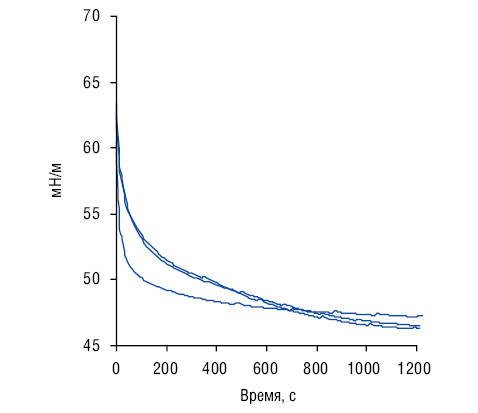
Не выявлено корреляционных связей e, s2, s3, l, j и w СЖ с физико-химическими параметрами крови, а также e и s4 сыворотки крови с АРСС. Прямые высокодостоверные корреляции касаются таких одинаковых показателей в СЖ и крови, как h, m, r и t. Соотношение значений h сыворотки крови и СЖ при РГ составляют 77,9±15,82±2,67%, m — 95,5±16,34±2,76%, r — 119,5±54,86±9,27%, e — 61,0±23,17±3,92%, s4 — 79,9±8,73±1,48%, t — 24,3±1,57±0,27%. Установлено, что h СЖ высокодостоверно выше, чем крови на 29%, e — на 66%, s4 — на 26%, t — 4,1 раза, тогда как значения m и r этих биологических жидкостей мало отличаются между собой. Наиболее типичные тензиограммы СЖ и крови у трех больных РГ представлены на рис. 3.
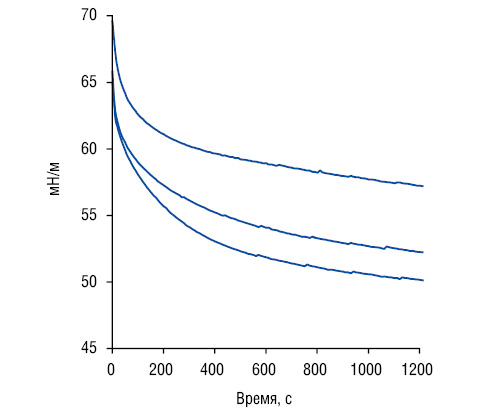
По данным многофакторного дисперсионного анализа Уилкоксона — Рао, интегральные АРСС при РГ тесно связаны только с возрастом пациентов и не определяются степенью тяжести течения заболевания. ANOVA демонстрирует влияние возраста больных на параметры m, s1, s2 и s4. Установлены прямая корреляционная связь с возрастом значений m, а также обратные соотношения s3 и s4. С учетом полученных результатов можно сделать заключение, что согласно возрасту пациентов с РА повышаются поверхностные вискозные свойства СЖ на фоне уменьшения межфазной активности.
Однофакторный дисперсионный анализ свидетельствует о достоверной зависимости показателей h от степени активности патологического процесса, распространенности суставного синдрома, ИТА и ИПА, r — только от ИПА, а e — от наличия экстраартикулярных (системных) признаков болезни. Корреляционный анализ показывает отрицательные связи с активностью РА показателей h и m, а также обратные взаимоотношения h c ИПА.
Дискуссия
Выполненный дисперсионный и корреляционный анализ позволил нам сделать заключения, имеющие практическую значимость: показатели СЖ h<1,4 мПа•с (<M-2SD больных) свидетельствуют о высокой степени активности и значительных темпах прогрессирования РА. По результатам выполненного ANOVA/MANOVA, на интегральное состояние АРСС у больных РА оказывает воздействие наличие кист Бейкера, но не отдельные артикулярные костно-деструктивные проявления заболевания. Однофакторный дисперсионный анализ демонстрирует отсутствие влияния рентгеносонографических признаков суставного синдрома на r, e, s2, s4, j и w СЖ, но при этом наблюдается связь h с наличием субхондрального склероза, m — интраартикулярных тел Пеллагри — Штайди, s1 — тел Гоффа, s3 — лигаментоза, t — хондромных тел, l — изменений рогов менисков.
На интегральные АРСС у больных РА оказывает влияние наличие лимфаденопатии, о чем свидетельствует анализ Уилкоксона — Рао. Показатели m зависят от поражения легких и синдрома Шегрена, e — от изменений со стороны почек и печени, s2 — от поражения миокарда, эндокарда и клапанов сердца, s3 — от наличия дигитального артериита, l — от лимфаденопатии. С отдельными экстраартикулярными признаками РА не связаны показатели h, r, s1, s4, j, w и t СЖ. Соотношение параметров h сыворотки крови и СЖ достоверно зависит от тяжести поражения миокарда и легких, значений равновесной межфазной активности — от наличия интраартикулярных тел Пеллагри — Штайди, показателей релаксационных свойств этих жидкостей — от тендовагинитов.
Следующим этапом нашей работы стала оценка патогенетической значимости нарушений АРСС при РА. Показатели вискозных свойств СЖ (h, m) определяют степень активности заболевания, значения r, e, s2 и s3 влияют на параметры индекса Ричи, t — на индекс Лансбури и формирование интраартикулярных кальцинатов, l — на развитие изменений рогов менисков и внутрисуставных хондромных тел. Появление лигаментоза тесно связано с параметрами r и e СЖ, тел Пеллагри — Штайди — с межфазной активностью в зонах коротких времен существования поверхности. Синдром Шегрена зависит от показателей соотношения статического s СЖ и сыворотки крови. Необходимо отметить, что ИТА определяет значение интегрального w. Между этими показателями существует обратная корреляционная связь. С учетом сказанного сделано следующее заключение: параметры СЖ w<8 о.е. (<M-SD больных) являются прогностически негативными в отношении течения РА.
Необходимо отметить, что на самом высоком уровне биологической организации поверхностно-активные свойства жидкостей обеспечиваются мембранными межмолекулярными взаимосвязями, обусловленными гидрофобными силами (Benjamins J., Lucassen-Rey E.H., 2008). При наличии двух фаз (воздух/СЖ) силы полярного взаимодействия молекул выталкивают гидрофобную часть из жидкой фазы и занимают энергетически наиболее выгодное положение на границе раздела. У больных РА в результате выталкивания гидрофобной и притягивания гидрофильной частей молекул сурфактанта в суставном ликворе образуются поверхностные адсорбционные слои (Brzozowska A.M. et al., 2011; Dash U., Misra P.K., 2011; Kao P. et al., 2011), вследствие чего снижается динамическое s СЖ.
Выводы
При РА по сравнению с показателями сыворотки крови достоверно повышаются на 29% значения h СЖ, на 66% — e, на 26% — s4 и в 4,1 раза — t, при этом интегральное состояние АРСС связано с возрастом больных, наличием кист Бейкера и лимфаденопатией, а отдельные параметры (h, m, r, s1, t) зависят от степени активности заболевания, распространенности суставного синдрома, его тяжести и темпов прогрессирования, наличия интраартикулярных хондромных тел, тел Пеллагри — Штайди и Гоффа, а также экстраартикулярных (системных) признаков болезни (m, e, s2, s3, l), причем нарушения АРСС участвуют в патогенетических построениях РА, а показатель w может иметь прогностическое значение. Надеемся, что методы межфазной тензиореометрии СЖ найдут широкое применение в артрологической практике (в частности при РА) для дифференциальной диагностики суставной патологии, оценки степени активности и прогнозирования темпов прогрессирования патологического процесса, а также для интегрального контроля за эффективностью лечебных мероприятий.
Список использованной литературы
- Синяченко О.В. (2009) Сучасне дослідження синовіальної рідини у ревматологічній практиці. Укр. ревматол. журн., 37(3): 14–15.
- Синяченко О.В. (ред.) (2011) Адсорбционно-реологические свойства биологических жидкостей в ревматологии. Донеччина, Донецьк, 286 с.
- Синяченко О.В. (2012) Диагностика и лечение болезней суставов. Издатель А.Ю. Заславский-ЭЛБИ, Донецк — Санкт-Петербург, 560 с.
- Чернякова Ю.М., Сементовская Е.А. (2008) Синовиальная жидкость: состав, свойства, лабораторные методы исследования. Мед. новости, 2: 9–14.
- Benjamins J., Lucassen-Reyn E.H. (2008) Surface dilatational rheology of proteins adsorbed at air/waret and oil/water interfaces. Protein. Liquid. Interfac., 7: 241–284.
- Brannan S.R., Jerrard D.A. (2008) Synovial fluid analysis. J. Emerg. Med., 30(3): 331–339.
- Brzozowska A.M., Spruijt E., De Keizer A. et al. (2011) On the stability of the polymer brushes formed by adsorption of ionomer complexes on hydrophilic and hydrophobic surfaces. J. Colloid Interf. Sci., 353(2): 380–391.
- Chenevier-Gobeaux C., Simonneau C., Lemarechal H. et al. (2012) Hypoxia induces nitric oxide synthase in rheumatoid synoviocytes: consequences on NADPH oxidase regulation. Free Radic. Res., 46(5): 628–636.
- Collins G.W., Patel A., Dilley A. et al. (2008) Molecular modeling directed by an interfacial test apparatus for the evaluation of protein and polymer ingredient function in situ. J. Agric. Food Chem., 56(10): 3846–3855.
- Dash U., Misra P.K. (2011) Evidence in favor of formation of hydrophobic complexes in aqueous solution. J. Colloid Interf. Sci., 357(2): 407–418.
- Fainerman V.B., Aksenenko E.V., Petkov J.T. et al. (2010) Adsorption layer characteristics of mixed oxyethylated surfactant solutions. J. Phys. Chem B., 114(13): 4503–4508.
- Fiocco U., Oliviero F., Sfriso P. et al. (2012) Synovial biomarkers in psoriatic arthritis. J. Rheumatol., Suppl. 89: 61–64.
- Gordon R.A., Grigoriev G., Lee A. et al. (2012) The interferon signature and STAT1 expression in rheumatoid arthritis synovial fluid macrophages are induced by tumor necrosis factor α and counter-regulated by the synovial fluid microenvironment. Arthritis Rheum., 64(10): 3119–3128.
- Hulejova H., Andres Cerezo L., Kuklova M. et al. (2012) Novel adipokine fibroblast growth factor 21 is increased in rheumatoid arthritis. Physiol. Res., 61(5): 489–494.
- Jablonka A., Schmidt R.E., Meyer-Olson D. (2012) Differential diagnosis of inflammatory arthritis of the hip joint. Unfallchirurg., 115(11): 959–966.
- Kao P., Parhi P., Krishnan A. et al. (2011) Volumetric interpretation of protein adsorption: Interfacial packing of protein adsorbed to hydrophobic surfaces from surface-saturating solution concentrations. Biomaterials, 32(4): 969–978.
- Kotsmar C., Aksenenko E.V., Petkov J.T. et al. (2009) Thermodynamics, adsorption kinetics and rheology of mixed protein-surfactant interfacial layers. Adv. Colloid Interface Sci., 150(1): 41–54.
- Miller R., Liggieri L. (Eds) (2009) Interfacial Rheology. Brill Publ., Leiden, 519 p.
- Oliviero F., Lo Nigro A., Bernardi D. et al. (2012) A comparative study of serum and synovial fluid lipoprotein levels in patients with various arthritides. Clin. Chim. Acta, 413(1–2): 303–307.
- Ren H., Xu S., Wu S.T. (2010) Deformable liquid droplets for optical beam control. Opt. Express., 18(11): 11904–11910.
- Rosenfeld L., Fuller G.G. (2012) Consequences of interfacial viscoelasticity on thin film stability. Langmuir, 28(40): 14238–14244.
- van Beers J.J., Schwarte C.M., Stammen-Vogelzangs J. et al. (2012) The RA synovial fluid citrullinome reveals novel citrullinated epitopes in apolipoprotein E, myeloid nuclear differentiation antigen and beta-actin. Arthritis Rheum., 64(10): 3225–3227.
- van Steijn V., Kleijn C.R., Kreutzer V.T. (2010) Predictive model for the size of bubbles and droplets created in microfluidic T-junctions. Lab. Chip., 10(19): 2513–2518.
- Zamani B., Jamali R., Ehteram H. (2012) Synovial fluid adenosine deaminase and high-sensitivity C-reactive protein activity in differentiating monoarthritis. Rheumatol. Int., 32(1): 183–188.
Адрес для переписки:
Синяченко Олег Владимирович
83003, Донецк-3, просп. Ильича, 16
Национальный медицинский
университет им. Максима Горького

Leave a comment