РОЗВИТОК ТОКСИКО-ЕПІДЕРМАЛЬНОГО НЕКРОЛІЗУ НА ФОНІ ЛІКУВАННЯ ГІДРОКСИХЛОРОХІНОМ СИСТЕМНОГО ЧЕРВОНОГО ВОВЧАКА
Кулик М.С.1, Джус М.Б.1, Івашківський О.І.2, Карасевська Т.А.1, Потьомка Р.А.2
- 1Національний медичний університет ім. О.О. Богомольця, Київ
- 2Олександрівська клінічна лікарня м. Києва
Резюме. Вступ. Гідроксихлорохін — це синтетичний протималярійний препарат; серед побічних ефектів з боку шкіри, як повідомляють різні автори, є: тяжкий гострий генералізований екзантематозний пустульоз (Acute generalized exanthematous pustulosis — AGEP), фотоіндукована токсидермія, висип з еозинофілією та системними симптомами (Drug reaction with eosinophilia and systemic symptoms —DRESS) і токсико-епідермальний некроліз (TEН) [1, 10, 11, 17, 19, 21]. На сьогодні до цього препарату прикута особлива увага у зв’язку з його потенційною противірусною дією, що є актуальною в лікуванні тяжкого гострого респіраторного синдрому на тлі коронавірусу (SARS-CoV-2) в умовах пандемії; хоча ці дані є досить суперечливими та неоднозначними і потребують подальших досліджень [28]. Мета. З метою підвищення обізнаності та запобігання можливим життєво небезпечним наслідкам застосування гідроксихлорохіну пропонуємо ревматологам та лікарям загальної практики клінічний випадок розвитку та успішного лікування ТЕН на тлі застосування гідроксихлорохіну у хворої на системний червоний вовчак (СЧВ). Матеріали і методи. У статті представлений клінічний випадок хворої Т., у якої розвинувся ТЕН на тлі застосування гідроксихлорохіну, яка проходила лікування в умовах ревматологічного стаціонару Олександрівської клінічної лікарні м. Києва з приводу СЧВ. Результати. Хворій проведена системна терапія глюкокортикоїдами та підтримувальна терапія — регідратація, місцева обробка уражених ділянок шкіри, відміна препарату-«винуватця». Незважаючи на тяжкий перебіг ТЕН, після проведеного лікування пацієнтка виписана з позитивним результатом — повною епітеліалізацією шкіри. Висновки. У статті представлений власний досвід лікування та ведення пацієнтки з ТЕН. Проведений аналіз клінічних випадків виникнення ТЕН на тлі застосування гідроксихлорохіну в літературі, представлені дані щодо доказового лікування в разі цього стану. Розглянуто важливі практичні клінічні питання, що стосуються діагностики та ведення цих хворих з акцентом на ключові досягнення в його лікуванні.
УДК 616.5-002.525.2-085.065:616.591-002.4
DOI: 10.32471/rheumatology.2707-6970.81.15474
Вступ
Гідроксихлорохін використовують із 1940-х років для лікування різних аутоімунних порушень, тому в практиці ревматолога накопичений значний досвід його застосування. Загалом гідроксихлорохін є досить безпечним препаратом, найчастіші побічні ефекти на тлі його застосування такі: ретинопатія, макулопатія, дегенерація макули, кардіоміопатія, блокади серця, подовження інтервалу Q–T, ангіоневротичний набряк, порфирія, бронхоспазм, гіпоглікемія, втрата маси тіла та алергічні реакції, в тому числі з боку шкіри [17].
Мета роботи — представити клінічний випадок розвитку токсико-епідермального некролізу (TEН) у хворої на системний червоний вовчак (СЧВ) на тлі застосування гідроксилорохіну для запобігання можливим побічним ефектам препарату та подальшого лікування, спрямованого на цю реакцію. Проведено аналіз сучасних рекомендацій з лікування пацієнтів із ТЕН, а також сфер невизначеності та необхідних напрямків подальшого пошуку більш дієвих методів лікування з метою поширення інформації щодо побічних дій з боку шкіри на тлі лікування гідроксихлорохіном.
Матеріали і методи дослідження
Хвора Т. 1957 року народження поступила у 1-ше ревматологічне відділення Олександрівської клінічної лікарні м. Києва у квітні 2018 р. зі скаргами на біль у дрібних та середніх суглобах мігруючого характеру, набряк правого гомілково-ступневого суглоба, біль у м’язах, загальну слабкість, макуло-папульозний висип на обличчі за типом «метелик», що посилювався при інсоляції, випадіння волосся. Із анамнезу захворювання відомо, що протягом останнього місяця утворювалися виразки на слизовій оболонці ротової порожнини. У березні 2018 р. госпіталізована в терапевтичне відділення Київської міської клінічної лікарні № 4 зі скаргами на підвищення артеріального тиску (АТ) до 160/100 мм рт. ст., периферичні набряки, асцит. У ході обстеження виявлено полісерозити (асцит, плеврит, перикардит), підвищення швидкості осідання еритроцитів (ШОЕ), C-реактивного білка (СРБ), панцитопенію. При обстеженні виключені вірусні гепатити В, С, ВІЛ. У стаціонарі призначені антигіпертензивні препарати (валсартан + гідрохлоротіазид, лерканідипін), АТ нормалізувався, набряки зменшилися, пацієнтка була виписана з покращенням та направлена до ревматологів для виключення діагнозу СЧВ.
При госпіталізації в ревматологічний стаціонар загальний стан пацієнтки відносно задовільний. На шкірі обличчя — макуло-папульозний висип, хейліт, ділянки вогнищевої алопеції. АТ 140/90 мм рт. ст., тони приглушені, дихання ослаблене в нижніх відділах. При пальпації лімфатичних вузлів виявлена незначна аксилярна лімфаденопатія. Суглобовий статус: артрит правого гомілково-ступневого суглоба, болісність при пальпації суглобів та м’язів. В аналізах крові виявлено підвищення ШОЕ, СРБ, панцитопенію, позитивний антинуклеарний фактор (титр АНФ 1:320), антитіла до двоспіральної ДНК IgG (АТ до дс-ДНК) 12 МО/мл (референтні значення >10 позитивний), зниження показників системи комплементу С3 і С4 — 0,7 і 0,6 г/л відповідно (референтні значення — 0,9–1,8). Згідно з даними ехокардіографії (ехоКГ), виявлена сепарація листків перикарда до 1,3 см із фібрином (випіт 220 мл), помірна недостатність мітрального клапана, гіпертрофія міокарда лівого шлуночка. У загальному аналізі сечі виявлена лейкоцитурія (5–10 лейкоцитів у полі зору), еритроцитурія (6–8 еритроцитів у полі зору), циліндрурія. За даними ультразвукового дослідження (УЗД) органів черевної порожнини з нирками виявлені дифузні зміни печінки, хронічний холецистопанкреатит, мікроліти обох нирок. Згідно з діагностичними критеріями SLICC 2012, а саме макуло-папульозні висипання, фотосенсибілізація, нерубцева алопеція, артрит, серозит, еритроцитурія >5, лейкопенія, тромбоцитопенія, позитивні АНФ, АТ до дс-ДНК, низький рівень комплементу [16] встановлено діагноз: СЧВ, гострий перебіг, ІІ ступінь активності за SLEDAI, з ураженням шкіри (дерматит), суглобів (поліартралгії, артрит правого гомілково-ступневого суглоба, функціональна недостатність суглобів 1-го ступеня), нирок (люпус-нефрит, сечовий синдром, хронічна хвороба нирок (ХХН) IIа стадії (швидкість клубочкової фільтрації 68,3 мл/хв за CKD-EPI), м’язів (міалгія), слизових і серозних оболонок (хейліт, полісерозит), ретикуло-ендотеліальної системи (лімфаденопатія), з гематологічним синдромом (панцитопенія), позитивність за АНФ, АТ до дс-ДНК, гіпокомплементемія. Супутній діагноз: сечокам’яна хвороба, хронічний пієлонефрит. Артеріальна гіпертензія II ст., 3 ст., ризик 2, серцева недостатність I ст. зі збереженою фракцією викиду лівого шлуночка (ФВ 58%).
Згідно з рекомендаціями EULAR [5] 2019 р., хворим на СЧВ призначено таке лікування: метилпреднізолон 40 мг/добу, гідроксихлорохін 200 мг/добу, препарати кальцію з вітаміном D. Продовжено застосування антигіпертензивних препаратів (валсартан + гідрохлоротіазид, лерканідипін). Пацієнтка виписана через 2 тиж з покращенням, що проявлялося у вигляді регресу шкірних проявів, артриту, міалгій, нормалізації кількості тромбоцитів, лейкоцитів, гострофазових показників (ШОЕ та СРБ).
Однак через 7 днів від дня виписки та на 11-й день від початку застосування гідроксихлорохіну у хворої з’явилася рясна плямиста висипка на верхній ділянці тулуба з подальшим її розвитком і поширенням донизу (рис. 1), що не було спровоковано інсоляцією та не супроводжувалося загостренням клінічних проявів вовчака. До появи висипки хвора приймала ту саму антигіпертензивну терапію, а з доданих препаратів були метилпреднізолон, у зв’язку з чим його замінено на преднізолон; та гідроксихлорохін, який був одразу відмінений.
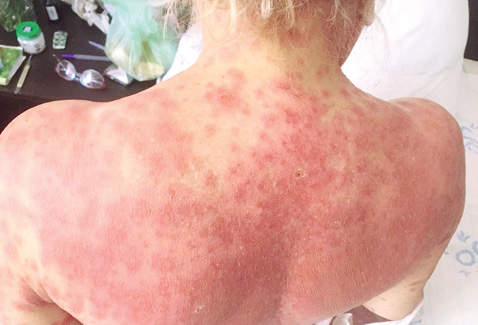
Враховуючи епідеміологічну ситуацію з підвищенням захворюваності на кір в Україні, хвора госпіталізована в інфекційне відділення для ізоляції та виключення цього захворювання. У ході обстеження виявлено негативні антитіла класу IgM (0,4 АІ) та позитивні антитіла класу IgG (2.14 АІ) до вірусу кору, таким чином виключено кір, а пацієнтку переведено у 1-ше ревматологічне відділення для продовження обстеження і лікування.
У ревматологічному відділенні хворій повторно проведені загальноклінічні та інструментальні обстеження. Згідно з даними ехоКГ, ознак випоту в перикарді та плевральних порожнинах не виявлено. Відсутність клініко-лабораторної активності СЧВ, позитивна динаміка з боку системи комплементу С3, С4, нормалізація гострофазових показників, відсутність панцитопенії свідчили на користь стабілізації захворювання. Враховуючи характерну висипку у вигляді багряно-червоних плям та некроліз епідермісу, а також етапність її поширення зверху донизу запідозрено ТЕН (рис. 2). Проведено консиліум за участю ревматологів, дерматологів та реаніматологів і встановлено остаточний клінічний діагноз: ТЕН, гострий перебіг, тотальне ураження шкіри. Супутній діагноз: СЧВ, мінімальний ступінь активності за SLEDAI.
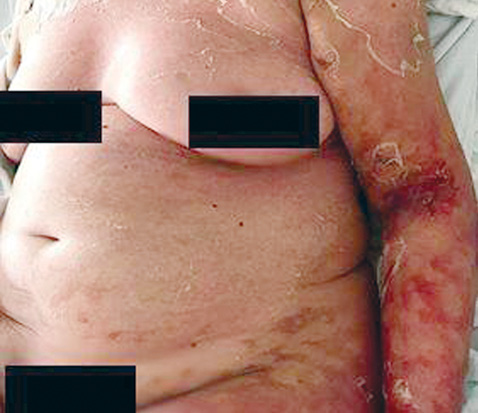
У зв’язку зі швидко прогресуючим погіршенням стану, ураженням шкіри >90%, необхідністю проводити цілодобовий моніторинг з інтенсивною терапією (пульс-терапією глюкокортикоїдами, дезінтоксикаційною та антибіотикотерапією), пацієнтка переведена у реанімаційне відділення.
На фоні проведення пульс-терапії метилпреднізолоном 500 мг внутрішньовенно протягом трьох днів з подальшим повільним зниженням дози до 250 та 125 мг внутрішньовенно протягом трьох днів відповідно, дезінтоксикаційної терапії (стерофундин), антибактеріальної (левофлоксацин 500 мг 2 рази на добу внутрішньовенно 10 днів, флуконазол 100 мг внутрішньовенно десять днів) та місцевої обробки шкіри (оксикорт-спрей, фукорцин, дермовейт), відзначалося повільне покращення стану та поступова епітелізація уражених ділянок (рис. 3).
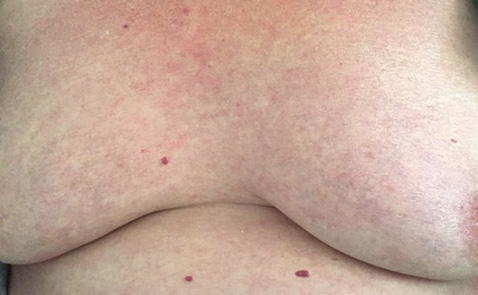
Пацієнтка виписана зі стаціонару з покращенням, та рекомендовано таке лікування: медрол 48 мг/добу протягом 4 тиж з поступовим зниженням дози до підтримувальної, препарати інгібіторів протонної помпи, кальцію з вітаміном D, попередня антигіпертензивна терапія. Питання базисної терапії рекомендовано вирішити після стабілізації стану.
Результати та їх обговорення
Токсичний епідермальний некроліз (ТЕН) вперше описав A. Lаyell у 1956 р., у зв’язку з чим ТЕН отримав назву синдрому Лайєлла. Схожий варіант ТЕН — синдром Стівенса — Джонсона (ССД) тривалий час розцінювався як крайній прояв мультиформної еритеми, яку вперше описав F. Herba у 1866 р. Згідно з сучасними уявленнями ССД та ТЕН розцінюються як варіанти одного патологічного процесу та об’єднані в синдром Стівенса — Джонсона — токсико-епідермальний некроліз (ССД-ТЕН).
Залежно від площі відшарування епідермісу виділяють три форми: 1. Синдром Стівенса — Джонсона («мала форма ТЕН») — відшарування епідермісу не більше 10% поверхні тіла. 2. Проміжна форма ССД-ТЕН («overlapping» ССД-TEН) — відшарування епідермісу від 10 до 30% поверхні тіла. 3. ТЕН (синдром Лайєлла) — відшарування епідермісу >30% поверхні тіла [20]. У представленому клінічному випадку уражена ділянка шкіри становила >90% поверхні тіла, що відповідає ТЕН.
Зазначимо, що діагноз ТЕН встановлюється переважно клінічно і немає жодних специфічних лабораторно-інструментальних підтверджувальних тестів. На користь ТЕН у нашому клінічному випадку свідчив, перш за все, характер висипки у вигляді поширених червоно-синюшних плям або плоских атипових мішенеподібних елементів, на тлі яких з’являються пухирці на фоні багряно-синюшних плям або в центральній зоні плоских атипових мішенеподібних елементів (рис. 4, 5), площа ексфоліації епідермісу досягає максимуму протягом декількох днів від моменту маніфестаціі клінічних проявів, у зв’язку з чим протягом перших 1–2 діб може бути встановлений лише попередній діагноз ТЕН; остаточний діагноз формулюється після стабілізації процесу і припинення появи нових висипань.
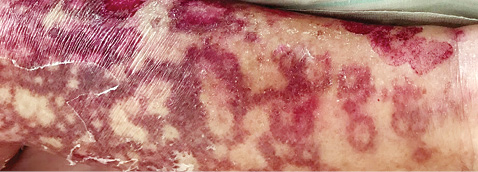
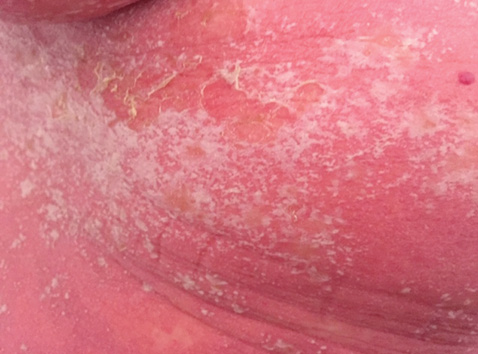
TEН — це бульозна токсико-алергічна реакція організму, індукована лікарським засобом, що руйнує шкіру і слизові оболонки. У нашому випадку ідентифікація цього препарату не була складною, оскільки гідроксихлорохін був єдиною новою молекулою, яку пацієнтка приймала протягом останніх 2 тиж. Як правило, що підтверджується і в нашому випадку, TEН розвивається протягом 1–3 тиж після введення препарату-«винуватця» [8].
Анатомо-патологічний аналіз шкіри показує досить типові зміни, але не є специфічним методом діагностики. Біопсія шкіри виявляє глибокий некроз епідермісу (рис. 5), який «відірваний» від більш-менш інтактної дерми з ледь помітним лімфоцитарним інфільтратом [13].
Дискусія
В існуючих алгоритмах та гайдлайнах ведення хворих з ТЕН особлива увага приділяється підтримувальній терапії, а саме — проведенню регідратаційної терапії, місцевій обробці шкіри та профілактичному введенню антибіотиків (рис. 6).
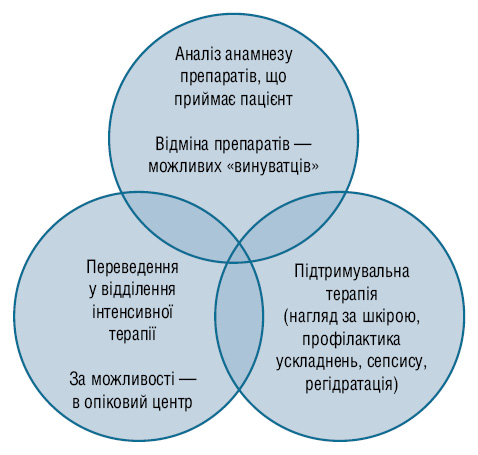
Необхідність системного лікування ТЕН залишається дискутабельним питанням та зводиться до декількох груп препаратів, серед яких: глюкокортикоїди, циклоспорин, імуноглобулін та блокатори фактора некрозу пухлини-альфа.
Зауважимо, що кількість летальних випадків не залежить від того, чи отримував хворий системне лікування чи лише підтримувальну терапію. Аналіз клінічних випадків розвитку алергічних реакцій з боку шкіри на тлі лікування гідроксихлорохіном, які викладені в літературі, систематизований у таблиці. Виходячи з цих даних, можна зробити висновок, що позитивний та негативний результати лікування не залежали від вибраної стратегії (у підтримувальній чи системній терапії), що значно ускладнює вибір тактики ведення хворих у таких випадках.
Таблиця. Випадки побічних реакцій з боку шкіри, викликаних гідроксихлорохіном (адаптовано за: Nour Abou Assalie [12])
| Повідомлення | ГХ-індукована побічна реакція | Захворювання | Лікування | Наслідки |
|---|---|---|---|---|
| Cameron M.C. et al., 2014 | ТЕН | СЧВ | В/в імуноглобуліни | Смерть |
| Park J.J. et al., 2010 | Гострий генералізований екзантематозний пустульоз | Дерматоміозит і поліартралгія | В/в ГК | Одужання |
| Lateef A. et al., 2009 | Гострий генералізований екзантематозний пустульоз, ТЕН | СЧВ | В/в імуноглобуліни
В/в ГК |
Одужання |
| Callaly E.L. et al., 2008 | ТЕН | Синдром Шегрена | В/в ГК | Одужання |
| Perez-Ezquerra P.R. et al., 2006 | Мультиформна еритема | Анкілозуючий спондилоартрит | В/в ГК антигістамінні | Одужання |
| Leckie M.J. et al., 2002 | Синдром Стівенса — Джонсона | Ревматоїдний артрит | В/в ГК | Одужання |
| Murphy M. et al., 2001 | ТЕН | Ревматоїдний артрит | без системного лікування | Смерть |
ГК — глюкокортикоїди.
З посиланнями на останній британський гайдлайн [3] була вибрана стратегія введення глюкокортикоїдів, оскільки вона має найбільшу, хоч і не завжди однозначну доказову базу. Ретроспективні реєстри EuroSCAR і RegiSCAR демонструють дані щодо близько 1000 хворих. Так, EuroSCAR виявила нестатистично значуще зниження смертності на фоні застосування глюкокортикоїдів порівняно з підтримувальною терапією, в той час як RegiSCAR не показав такої переваги [9].
Аналогічно дані цих і кількох інших досліджень, що охоплюють понад 1000 хворих, не показали зниження смертності на фоні введення внутрішньовенних імуноглобулінів проти підтримувальної терапії [2, 6, 16, 24, 25, 26]. Дані дослідження RegiSCAR свідчать на користь циклоспорину порівняно з підтримувальною терапією, хоча цей висновок не був статистично значущим [23]. Останнє ретроспективне дослідження, що включає 174 хворих, не показало користі від циклоспорину над підтримувальною терапією, про який раніше не повідомлялося в літературі, а також значно підвищений ризик ниркової недостатності у пацієнтів, які отримували циклоспорин [18].
Існує декілька повідомлень про застосування інфліксимабу у формі однієї інфузії 5 мг/кг маси тіла, що зупинило некроліз епідермісу і призвело до швидкої повторної епітелізації [15, 22, 27, 29]. Кілька серій випадків описали подібні результати з однією підшкірною ін’єкцією етанерцепту 50 мг [4, 7, 14]. Справжні переваги та недоліки блокаторів фактора некрозу пухлин-альфа в лікуванні ТЕН важко об’єктивно оцінити, оскільки опублікованих досліджень на цю тему мало.
Висновки
ТЕН рідко асоціюється з таким препаратом, як гідроксихлорохін, що застосовується при лікуванні пацієнтів із аутоімунними захворюваннями, в тому числі є основним базисним препаратом у лікуванні СЧВ. Проте препарат виявляє різні побічні ефекти з боку шкіри. Незважаючи на досить невисоку частоту виникнення цих реакцій, важливо інформувати пацієнта про необхідність негайного звернення за медичною допомогою при появі будь-яких алергічних реакцій з боку шкіри, враховуючи торпідний та загрожуючий життю характер ТЕН.
Список використаної літератури
- 1. Assier-Bonnet H., Saada V., Bernier M. et al. (1996) Acute Generalized Exanthematous Pustulosis Induced by Hydroxychloroquine. Lett Dermatol., 193: 71–72.
- 2. Campione E., Marulli G.C., Carrozzo A.M. et al. (2003) High‐dose intravenous immunoglobulin for severe drug reactions: efficacy in toxic epidermal necrolysis. Acta Dermato‐Venereol., 83(6): 430432 [PUBMED: 14690337].
- 3. Creamer D., Walsh S.A., Dziewulski P. et al. (2016) U.K. guidelines for the management of Stevens – Johnson syndrome/toxic epidermal necrolysis in adults 2016. 174: 1194–1227 & J. Plast. Reconstr. Aesthet Surg., 69: e119–e153.
- 4. Famularo G., Dona B., Canzona F. et al. (2007) Etanercept for toxic epidermal necrolysis. Ann. Pharmacother., 41(6): 1083–1084 [PUBMED: 17456541].
- 5. Fanouriakis A., Kostopoulou M., Alunno A. et al. (2019) 2019 update of the EULAR recommendations for the management of systemic lupus erythematosus. Ann. Rheum. Dis., 78: 736–745.
- 6. Faye O., Roujeau J.C. (2005) Treatment of epidermal necrolysis with high‐dose intravenous immunoglobulins (IV Ig): clinical experience to date. Drugs, 65(15): 2085–2090 [PUBMED: 16225365].
- 7. Gubinelli E., Canzona F., Tonanzi T. et al. (2009) Toxic epidermal necrolysis successfully treated with etanercept. J. Dermatol., 36(3): 150–153 [PUBMED: 19335689]
- 8. Lebrun-Vignes B., Valery-Allanore L. (2015) Toxidermies. Rev. Med. Inter., 36: 256–270.
- 9. Lee H.Y., Dunant A., Sekula P. et al. (2012) The role of prior corticosteroid use on the clinical course of Stevens — Johnson syndrome and toxic epidermal necrolysis: a case-control analysis of patients selected from the multinational EuroSCAR and RegiSCAR studies. Br. J. Dermatol., 167(3): 555–562.
- 10. Metayer I., Balguerie X., Courvillke P. et al. (2001) Toxidermies photo-induites par I’hydroxychloroquine : 4 cas. Ann. Dermatol. Venereol., 128: 729–731.
- 11. Naziha K., Maha B.S., Dorsaf M. et al. (2010) Severe Acute Generalized Exanthematous Pustulosis Induced by Hydroxychloroquine Mimicking Toxic Epidermal Necrolysis. Egyt. Dermatol. O Line, 6(1): 1–7.
- 12. Nour Abou Assalie, Robert Durcan, Laura Durcan et al. (2017) Hydroxychloroquine-induced erythema multiforme. J. Clin. Rheumatol., 23(2): 127–128.
- 13. Paquet P., Flagothier C., Pierard-Franchimont C. et al. (2004) Les toxidermies paroxystiques graves. Rev. Med. Liege, 59(5): 286–292.
- 14. Paradisi A., Abeni D., Bergamo F. et al. (2014) Etanercept therapy for toxic epidermal necrolysis. J. Am. Acad. Dermatol., 71(2): 278–283 [PUBMED: 24928706].
- 15. Patmanidis K., Sidiras A., Dolianitis K. et al. (2012) Combination of infliximab and high‐dose intravenous immunoglobulin for toxic epidermal necrolysis: successful treatment of an elderly patient. Case Rep. Dermatol. Med., 915314 [PUBMED: 23259092].
- 16. Petri M., Orbai A.M., Alarcón G.S. et al. (2012) Derivation and validation of the Systemic Lupus International Collaborating Clinics classification criteria for systemic lupus erythematosus. Arthr. Rheum., 64(8): 2677–2686. doi:10.1002/art.34473.
- 17. Plaquenil (hydroxychloroquine sulphate) tablets (2006): Adverse reactions. Bridgewater (NJ): Sanofi, Oct. 5.
- 18. Poizeau F., Gaudin O., Cleach L. et al. (2018) Cyclosporine for epidermal necrolysis: absence of beneficial effect in a retrospective cohort of 174 patients ‐ exposed/unexposed and propensity‐score matched analyses. J. Invest. Dermatol., 138(6): 1293–1300 [PUBMED: 29369774].
- 19. Prins C., Kerdel F.A., Padilla R.S. et al. (2003) Treatment of toxic epidermal necrolysis with high‐dose intravenous immunoglobulins: multicenter retrospective analysis of 48 consecutive cases. Archiv. Dermatol.,139(1): 26–32 [PUBMED: 12533160].
- 20. Roujeau J.-C., Kelly J.-P., Naldi l. et al. (1995) Medication use and risk of Stevens-Johnson Syndrome or Toxic epidermal Necrolysis. New Engl. J. Мed., 33(24): 1600–1607.
- 21. Schmutz J.-L., Barbaud A., Tréchot P. (2008) Dress et hydroxychloroquine. Ann. Dermatol. Venereol., 135: 903.
- 22. Scott‐Lang V., Tidman M., McKay D. (2014) Toxic epidermal necrolysis in a child successfully treated with infliximab. Pediatric Dermatol., 31(4): 532–534 [PUBMED: 23072342].
- 23. Sekula P., Dunant A., Mockenhaupt M. et al. (2013) Comprehensive survival analysis of a cohort of patients with Stevens‐Johnson syndrome and toxic epidermal necrolysis. J. Invest. Dermatol., 133(5): 1197–1204 [PUBMED: 23389396].
- 24. Stella M., Cassano P., Bollero D. et al. (2001) Toxic epidermal necrolysis treated with intravenous high‐dose immunoglobulins: our experience. Dermatology, 203(1): 45–49 [PUBMED: 11549799].
- 25. Trent J.T., Kirsner R.S., Romanelli P. et al. (2008) Analysis of intravenous immunoglobulin for the treatment of toxic epidermal necrolysis using SCORTEN: the University of Miami experience. Archiv. Dermatol.,139(1): 39–43 [PUBMED: 12533162].
- 26. Viard I., Wehrli P., Bullani R. et al. (1998) Inhibition of toxic epidermal necrolysis by blockade of CD95 with human intravenous immunoglobulin. Science, 282(5388): 490–493 [PUBMED: 9774279].
- 27. Wojtkiewicz A., Wysocki M., Fortuna J. et al. (2008) Beneficial and rapid effect of infliximab on the course of toxic epidermal necrolysis. Acta Dermato‐Venereol., 88(4): 420–421 [PUBMED: 18709327].
- 28. Yao X., Ye F., Zhang M. et al. (2020) In vitro antiviral activity and projection of optimized dosing design of hydroxychloroquine for the treatment of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2).
- 29. Zárate‐Correa L.C., Carrillo‐Gómez D.C., Ramírez‐Escobar A.F. et al. (2013) Toxic epidermal necrolysis successfully treated with infliximab. J. Investig. Allergol. Clini. Immunol., 23(1): 61–63 [PUBMED: 23653980].
Развитие токсико-эпидермального некролиза на фоне лечения гидроксихлорохином системной красной волчанки
1Национальный медицинский университет им. А.А. Богомольца, Киев
2Александровская клиническая больница, Киев
Резюме. Введение. Гидроксихлорохин — это синтетический противомалярийный препарат; среди побочных эффектов со стороны кожи, как сообщают разные авторы, являются: тяжелый острый генерализованный экзантематозный пустулез (Acute generalized exanthematous pustulosis — AGEP), фотоиндуцированная токсидермия, сыпь с эозинофилией и системными симптомами (Drug reaction with eosinophilia and systemic symptoms — DRESS) и токсико-эпидермальный некролиз (ТЭН) [1, 10, 11, 17, 19, 21]. На сегодняшний день к этому препарату приковано особое внимание в связи с его потенциальным противовирусным действием, что является актуальным в лечении пациентов с тяжелым острым респираторным синдромом на фоне коронавируса (SARS-CoV-2) в условиях пандемии; хотя эти данные являются достаточно противоречивыми и неоднозначными, что требует дальнейших исследований [28]. Цель. С целью увеличения осведомленности и предупреждения возможных жизненно опасных последствий применения гидроксихлорохина предлагаем ревматологам и врачам общей практики клинический случай развития ТЭН на фоне применения гидроксихлорохина у больной с системной красной волчанкой (СКВ). Материалы и методы. В статье представлен клинический случай больной Т., у которой развился ТЭН на фоне лечения гидроксихлорохином, проходившей лечение в условиях ревматологического стационара по поводу СКВ. Результаты. Больной проведена системная терапия глюкокортикоидами и поддерживающая терапия в виде регидратации, местная обработка пораженных участков кожи, отмена препарата-«триггера». Несмотря на тяжелое течение ТЭН, после проводимой терапии пациентка была выписана с положительным результатом в виде полной эпителиализации кожи. Выводы. В статье представлен клинический пример успешного лечения ТЭН, проведен анализ клинических случаев возникновения ТЭН на фоне применения гидроксихлорохина в литературе. Рассмотрены важные практические клинические вопросы, касающиеся диагностики и ведения этих больных с акцентом на ключевые достижения в его лечении.
Ключевые слова: токсико-эпидермальный некролиз, гидроксихлорохин, системная красная волчанка.
Адреса для листування:
Кулик Мирослава Сергіївна
03055, Київ, просп. Перемоги 29, к. 28
E-mail: myroslavakulyk@gmail.com

Leave a comment