ДІАГНОСТИКА Й ОЦІНКА ЕФЕКТИВНОСТІ ЛІКУВАННЯ НЕСПЕЦИФІЧНОГО АОРТОАРТЕРІЇТУ (АРТЕРІЇТУ ТАКАЯСУ) ЗА ДОПОМОГОЮ ПОЗИТРОННО-ЕМІСІЙНОЇ ТОМОГРАФІЇ/КОМП’ЮТЕРНОЇ ТОМОГРАФІЇ (ПЕТ/КТ): КЛІНІЧНЕ СПОСТЕРЕЖЕННЯ
Чипко Т.М., Кметюк Я.В., Головач И.Ю., Лазоренко Е.А., Ашихмін А.В., Олексеенко Е.А.
Резюме. Наведено клінічне спостереження пацієнтки із синдромом системної запальної відповіді та численними неспецифічними скаргами, якій з діагностичною метою проведено позитронно-емісійну томографію/комп’ютерну томографію із 18F-фтордезоксиглюкозою (18F-ФДГ ПЕТ/КТ). Сканування з 18F-ФДГ показало інтенсивне накопичення радіофармпрепарату та підвищення метаболічної активності у всіх відділах аорти, у підключичних, загальних сонних, стегнових артеріях, що дозволило встановити діагноз неспецифічного аортоартеріїту (хвороби Такаясу). Обговорено можливості використання 18F-ФДГ ПЕТ/КТ для ранньої діагностики артеріїту, а також оцінки активності захворювання при проведенні медикаментозного лікування. Представлені дані 18F-ФДГ ПЕТ/КТ до початку лікування і через 6 міс.
Неспецифический аортоартериит (НАА) — заболевание группы системных васкулитов, характеризующееся поражением аорты и отходящих от нее сосудов, с развитием деструктивно-продуктивного сегментарного аортита и субаортального панартериита, которые приводят к деформации сосудистого просвета и, следовательно, к ишемическим расстройствам [3].
Относительная редкость данной патологии является одним из факторов, определяющим сложность и несвоевременность ее диагностики, неадекватность лечения, что приводит к ранней инвалидизации и высокому риску развития жизнеугрожающих осложнений у больных с НАА [1, 10].
Начало заболевания характеризуется неспецифическими общевоспалительными симптомами, такими как лихорадка, общее недомогание, слабость, утомляемость, что сопровождаются уменьшением массы тела. Позже прогрессирующее воспаление пораженных артерий приводит к возникновению сегментарных стенозов, окклюзий, дилатаций и/или аневризм сосудов, что, в свою очередь, обусловливает появление местной клинической симптоматики, характеризующейся исчезновением пульса, несимметричным уменьшением пульса или полным отсутствием артериального давления, перемежающей хромотой, наличием шумов над аортой, сонными артериями, а в отдельных случаях — возникновением острой потери зрения и инсульта [1, 7]. Необходимо отметить, что в связи с разнообразием участков поражения ход заболевания и его прогноз могут быть гетерогенными и достаточно неоднозначными. Важным также является то, что сегодня отсутствуют стандартные и надежные показатели, отражающие активность заболевания [8]. Системная воспалительная реакция не всегда свидетельствует о положительной корреляции с воспалительной активностью в стенке сосуда. Поэтому НАА, с одной стороны, может быть активным, несмотря на нормальный уровень скорости оседания эритроцитов (СОЭ) и С-реактивного белка (СРБ), а с другой — пациенты с очевидной клинической и лабораторной ремиссией могут демонстрировать гистологические признаки активного васкулита [16].
Таким образом, клинические симптомы артериита Такаясу связаны, с одной стороны, с неспецифическими симптомами системной воспалительной активности, с другой — являются проявлением прогрессирования ишемических изменений вследствие поражения различных отделов сосудистого русла [12]. Течение НАА может иметь прогрессирующий или интермиттирующий характер в зависимости от объема поражения сосудов, наличия осложнений и приверженности пациента лечению.
Важность ранней диагностики НАА является очевидной, поскольку позволяет начать лечение до периода необратимого поражения сосудов и развития стойких ишемических изменений со стороны внутренних органов и систем, а также предупредить или отсрочить проведение хирургического лечения. К сожалению, часто болезнь может прогрессировать до тех пор, пока поражение не будет определено ангиографически.
Важнейшим методом диагностики НАА является визуализация, которую используют как с целью установления диагноза и определения участков поражения, так и для мониторинга активности заболевания [4]. Признанным стандартом инструментальной диагностики НАА остается рентгеноконтрастная ангиография аорты и ее ветвей, что позволяет точно определить локализацию, степень и характер поражения сосудистого русла. Однако данный метод также имеет ряд недостатков: инвазивность, высокая лучевая нагрузка, низкая информативность на ранней (доокклюзивной) стадии НАА. Наконец, невозможность дифференцировать, например, воспалительное поражение от интраваскулярного тромба или кальцифицированной атеромы, что в конечном итоге не позволяет отличить острое внутристеночное воспаление от хронического стенотического поражения [11, 13].
В последнее время широкое распространение получили такие неинвазивные методы, как дуплексное сканирование (ДС) брахиоцефальных артерий, компьютерная томография (КТ), магнитно-резонансная томография (МРТ). МРТ с внутривенным усилением гадолинием обеспечивает адекватное качество изображений для оценки анатомии крупных сосудов и определения стеноза/аневризм [9]. Отмечается также повышенное поглощение гадолиния воспаленными сосудами, вероятно, вследствие повышенной проницаемости. Однако специфичность метода для дифференциации активного воспаления и отека в стенке сосуда остается также недостаточной [19]. Этот метод, как и ангиография, не способен визуализировать ранние этапы сосудистого воспаления и, наоборот, остаточный воспалительный процесс у пациентов с длительным течением болезни при необходимости контроля активности и эффективности лечения. Поэтому золотым стандартом диагностики НАА остается гистопатология, впрочем, в большинстве случаев она не может быть проведена.
В настоящее время ведется поиск технологий, обеспечивающих, прежде всего, адекватную верификацию воспаления стенки артерии, что чрезвычайно важно для диагностики ранней — доокклюзивной стадии НАА (pre-pulseless stadium). Перспективной в этом плане считается позитронно-эмиссионная томография (ПЭТ) с 18F-фтордезоксиглюкозой (18F-ФДГ). 18F-ФДГ ПЭТ/КТ — это неинвазивный диагностический метод визуализации метаболических процессов, основанный на оценке поглощения тканями радиофармпрепарата (РФП) ФДГ. Данный метод со времени введения в клинику активно использовался в онкологии для диагностики, стадирования и оценки эффективности лечения опухолей с высоким уровнем метаболизма глюкозы. Выявленное повышенное накопление РФП в тканях при воспалительных процессах у онкологических пациентов положило начало новому направлению диагностики и расширило сферу применения метода, позволив качественно и количественно оценивать степень локальных и системных воспалительных процессов в организме [2, 20]. Активированные лейкоциты усиливают экспрессию транспортных белков глюкозы, а в самих клетках значительно повышается содержание глюкозы и, соответственно, РФП — 18F-ФДГ, что дает возможность визуализировать воспаление при неинвазивной методике. ПЭТ позволяет визуализировать очаги воспаления в артериальной стенке независимо от степени стеноза артерии [18, 20]. В то же время радиоактивная метка дезоксиглюкозы определяет стенки воспаленных артерий и реально демонстрирует распространенность патологического процесса. 18F-ФДГ относится к ультракороткоживущим РФП. Дезоксиглюкоза метится позитронным эмиттером 18F, период полураспада которого составляет 109,77 мин. После внутривенного введения пациенту биораспределение препарата происходит аналогично обычной глюкозе до момента попадания в клетки. После фосфорилирования в клетке до 18F-ФДГ-6-фосфата препарат дальше не метаболизируется, а накапливается. Таким образом, позитронный эмиттер 18F дает возможность с помощью сканера определить концентрацию введенного препарата в той или иной точке пропорционально уровню глюкозы [2].
Совместная регистрация изображений, получаемых ПЭТ с 18F-ФДГ и мультиспиральной компьютерной томографии (МСКТ), дает возможность более точно описать анатомию и морфологию поражения, что особенно важно для принятия решения о характере реваскуляризации. Поглощение ФДГ (18F-ФДГ) связано с клинической активностью заболевания и маркерами воспаления, таким образом, ПЭТ/КТ отражает изменения клинической активности заболевания у пациентов с НАА. Оказалось также, что 18F-ФДГ ПЭТ/КТ обладает большей чувствительностью (92,6%) и специфичностью (91,7%) по сравнению с уровнем СРБ (чувствительность — 81,5%, специфичность — 66,7%) и СОЭ (74,1 и 58,3% соответственно) (р<0,05 соответственно) [11, 14]. Поэтому ПЭТ может быть полезным инструментом в оценке активности заболевания у больных НАА [15]. Это неоспоримое преимущество данного метода по сравнению с ДС, МРТ или ангиографией [13, 18].
В 2014 г. впервые в Украине опубликованы данные по использованию метода ПЭТ/КТ в диагностике НАА на ранней pre-pulseless стадии [4, 17]. В 2015 г. с помощью ПЭТ/КТ диагностирован еще один случай НАА. С помощью данного метода проведена оценка эффективности лечения, а также контроль активности сосудистого воспаления. Приводим описание данного случая.
Пациентка Б., 77 лет, 23.07.2015 г. обратилась в клинику с жалобами на выраженную слабость, похудение, сниженный аппетит, периодическую тошноту, разлитую и нелокализованную боль в животе, болезненное вздутие кишечника, боль в суставах и мышцах, головную боль, нарушение зрения, головокружение, шаткость при ходьбе, слабость в руках, зябкость рук, особенно в холодное время, повышение температуры тела до субфебрильных цифр, а также значительные отклонения в общем анализе крови — анемия, тромбоцитоз и повышение СОЭ до 82 мм/ч (по Вестергрену). Указанные жалобы беспокоят пациентку в течение последних 2 лет, характеризуются значительной гетерогенностью и разрозненностью, изменениями выраженности во времени, непостоянством. Спектр жалоб указывает на поражение различных систем и органов, а также на формирование недифференцированного неинфекционного общевоспалительного синдрома.
В анамнезе операция холецистэктомии по поводу калькулезного холецистита, после чего периодически беспокоили боль в эпигастрии и тяжесть в правом подреберье. В 2014 г. диагностирован базальноклеточный рак кожи грудной клетки справа, Т1N0M0, удален. У пациентки артериальная гипертензия, по поводу которой принимает антигипертензивные препараты.
При осмотре: нормального телосложения. ИМТ — 25,4 кг/м. Кожные покровы бледно-розовые, чистые, единичные старческие кератомы на лице и груди; тургор снижен. Периферические лимфоузлы, доступные пальпации, не увеличены, безболезненные, подвижные. Щитовидная железа не увеличена. Зев чистый. В легких на всем протяжении выслушивается везикулярное дыхание, ЧД — 18/мин. Границы сердца расширены влево. Сердечные тоны ритмичные, звучность снижена, акцент II тона над аортой и точкой Боткина — Эрба. Патологические шумы в области сердца не выслушиваются. ЧСС — 74 уд./мин. АТ — 140/80 мм рт. ст. Пульс на лучевой артерии сохранен, симметричный на обеих руках. Живот при пальпации мягкий, принимает участие в акте дыхания, незначительная чувствительность при пальпации в эпигастрии и мезогастрии. Печень по краю реберной дуги, безболезненная, край заокругленный, обычной плотности. Желчный пузырь удален. Поджелудочная железа недоступна для пальпации. Отрезки толстого кишечника пальпируются в виде плотно-эластичных тяжей, подвижные, спазмированные слева и несколько расширенные справа. Перистальтика кишечника удовлетворительная, ритмичная. Стул со склонностью к запорам; кал без патологических примесей. Почки не пальпируются. Мочеиспускание свободное, без дизурических явлений. Периферические отеки на нижних конечностях отсутствуют. Шаткость в позе Ромберга. Периферические суставы не деформированы, без воспалительных изменений, объем движений сохранен. Болезненность при пальпации и значительное ограничение движений в левом плечевом суставе. Мышечная сила сохранена. Мышечных артрофий/гипотрофий нет. Незначительная болезненность при пальпации мышц плечей и надплечий.
Лабораторные обследования:
Общий анализ крови от 23.07.2015 г. — эритроциты — 4,1·10/л, гемоглобин 106 г/л, лейкоциты — 4,1·10/л, тромбоциты — 388·10/л, палочкоядерные — 2%,сегментоядерные — 64%, эозинофилы — 1%, лимфоциты — 28%, моноциты — 5%, СОЭ — 45 мм/ч.
Коагулограмма от 23.07.2015 г. — протромбиновое время — 17 с, тромбиновое время — 17 с, фибрин 7,3 г/л, этаноловый тест негативный, β-нафтоловый тест (+++).
Биохимический анализ крови от 23.07.2015 г. — общий белок 79 г/л, мочевина 4,5 ммоль/л, креатинин 72 мкмоль/л, общий холестерин 6,3 ммоль/л, триглицериды 1,6 ммоль/л, β-липопротеиды 62 ед., общий билирубин 13,3 мкмоль/л, щелочная фосфатаза 242 ед./л, АлАТ 15 ед./л, АсАТ 16 ед./л, ГГТП 30 ед./л, КФК 63 ед./л, сывороточное железо 9,5 мкмоль/л, глюкоза крови 5,4 ммоль/л.
Общий анализ мочи без патологических отклонений.
Антинуклеарные антитела (ANA Detect) — 0,61 (>1,2 позитивный); LE-клетки (трижды) — не выявлены; антитела к двухцепочечной ДНК — 0,8 МЕ/мл (норма < 20 МЕ/мл), антитела к миелопероксидазе — негативные, антитела к протеиназе-3 — негативные. СРБ — 54,7 мг/л.
С учетом значительного повышения СОЭ и СРБ пациентке проведен онкологический поиск, в котором не выявлена причина общевоспалительного синдрома и лабораторных отклонений.
С целью выяснения причины общевоспалительного синдрома и поиска возможной опухоли, что не была определена другими методами исследования, проведено ПЭТ/КТ. Исследование проводили в соответствии со стандартным ПЭТ-протоколом с 18F-ФДГ в режиме «целого тела» («whole body») с внутривенным усилением с помощью 64-срезового комбинированного сканера Biograph 64 [5]. Эффективная доза ПЭТ — 5.4000001 мЗв, КТ — 25.9 мЗв.
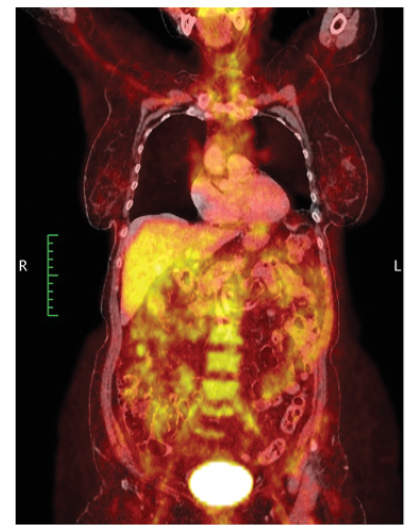
ПЭТ/КТ с контрастным усилением от 24.07.2016 г. Внутривенно введено 18F-ФДГ — 284.79999 МБк. При исследовании метаболически активной неопластической ткани не выявлено. Однако установлено повышение фиксации РФП стенками аорты, надаортальными, подвздошными и бедренными артериями (SUVmax от 3,15 до 4,8); стенка аорты утолщена до 0,4 см (SUVmax аорты = 4,6) (рис. 1–3). Согласно данным ПЭТ/КТ, у пациентки Б. наблюдалось выраженное поражение подключичных артерий со многочисленными стенозами, поражение восходящей аорты, дуги и нисходящей аорты, подвздошных и бедренных артерий. Наибольшее накопление РФП отмечено в подключичных артериях. Поражение различных артериальных сосудов объясняло разнообразные жалобы пациентки и появление симптомов поражения/выпадения функций. Так, поражение подключичных артерий ассоциировалось со слабостью в руках, зябкостью, миалгией верхних конечностей, артралгией, несмотря на сохранение пульса на периферических артериях рук. Поражение сонных артерий — с нарушениями зрения, головной болью, головокружением, шаткостью. Поражение абдоминального отдела аорты объясняло многочисленные гастроэнтерологические жалобы пациентки, прежде всего болевой синдром.
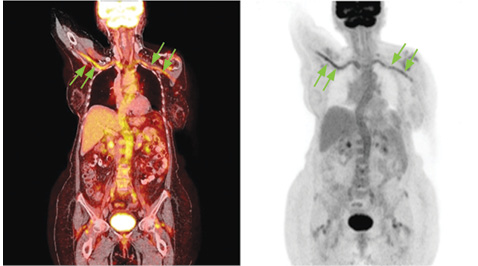
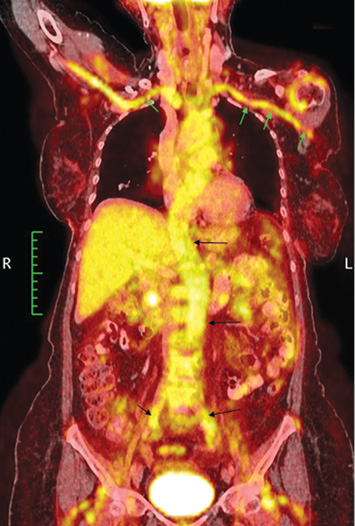
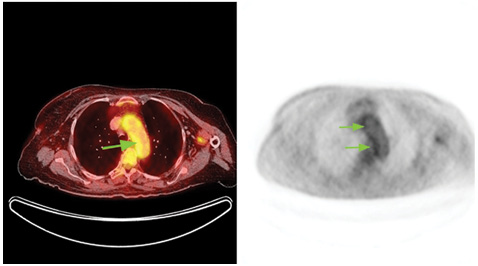
ДС экстра- и интракраниальных отделов брахиоцефальных сосудов зарегистрировало многочисленное стенозирующее поражение сонных артерий (табл. 1).
при дуплексном сканировании
| Параметры | Vps, sm/s | Ved, sm/s | RI | PI | D, mm | KИM, mm | Стеноз,% | |
|---|---|---|---|---|---|---|---|---|
| Общая сонная артерия | D | 63 | 14 | 0,7 | 1,6 | 5,7 | 0,9 | 55 |
| S | 51 | 14 | 0,7 | 1,5 | 5,4 | 1,0 | 40 | |
| Внутренняя сонная артерия | D | 31–110 | 8 | 1,7 | 65 | |||
| S | 60–101 | 14 | 1,7 | 60 | ||||
| Внешняя сонная артерия | D | 46–81 | 5 | 60 | ||||
| S | 53 | 3 | 40 | |||||
| Позвоночная артерия | D | 36–47 | 9 | 3,0 | 50 | |||
| S | 61–84 | 16 | 3,3 | |||||
D — диаметр; KИM — комплекс интима — медиа.
Заключение. Доля стеноза определена по методу ECST. Брахиоцефальные сосуды проходимы с обеих сторон. Выраженное стенозирующее поражение стенок артерий шеи. Стенозирование подключичной артерии слева до 55–60% по диаметру с типичным локальным гемодинамическим перепадом. Пролонгированный стеноз правой общей сонной артерии, начиная со средней трети и с переходом на дистальную часть (до 35–40%); гетерогенные пролонгированные с участками кальциноза бляшки зоны бифуркации общей сонной артерии (стеноз справа до 55%, слева — до 40%) с переходом на внутреннюю сонную артерию (пролонгированные стенозы с обеих сторон с выраженным гипоэхогенным компонентом, стенозирование справа от 55 до 65% по диаметру, слева — от 50 до 60% по диаметру) и внешнюю сонную артерию (пролонгированный стеноз справа от 55 до 60%, слева — локальный стеноз до 40%). Угловые изгибы обоих позвоночных артерий у входа в канал. Участок дефекта заполнения цветной картограммы позвоночной артерии справа в канале (не исключено стенозирование артерии до 45–50% по диаметру). Признаки повышения внутричерепного давления. Расширенные внутренние яремные вены с обеих сторон.
| VIS | OD = | 0,2 кор. с –1,75 sph = 1,0 |
| OS = | 0,2 кор. с –1,5 sph = 1,0 |
Жалобы на сужение полей зрения слева. При осмотре: глаза спокойные, в хрусталиках начальные помутнения. На глазном дне: OD — диск зрительного нерва бледно-розовый, границы четкие. Соотношение артерии/вены — ⅓. OS — диск зрительного нерва бледно-серый, границы четкие. Соотношение артерии/вены — ⅓. Диагноз: начальные признаки катаракты. Миопия средней степени OU. Нисходящая атрофия зрительного нерва OS.
При МРТ головного мозга выявлен лакунарный инфаркт головного мозга затылочной области (без анамнеза).
Активность и тяжесть болезни, а также диапазон клинических признаков были оценены с помощью индекса DEI-Тak [6].
Таким образом, у пациентки Б. согласно индексу DEI-Тak определяли высокую активность — 10 баллов из 19 (табл. 2).
| Синдром | Симптомы | Наличие |
|---|---|---|
| Системного поражения | Недомогание/уменьшение массы тела >2 кг, боль в мышцах/артралгия/артрит, головная боль, лихорадка |
+ |
| Поражение кожи | Гангрена, другие васкулиты кожи | – |
| Поражение слизистой оболочки | Сухость, язвы, раздражения | – |
| Поражение глаз | Утомляемость глаз, конъюнктивит, увеит, диплопия, постепенное снижение остроты зрения, образование аневризм, формирование анастомозов, гипертензивная ретинопатия | + |
| Поражение ЛОР-органов | Гранулематозное поражение слизистой оболочки, язвы, эрозии | – |
| Поражение легких | Персистирующий кашель, одышка/хрипы, нарушение дыхания, кровохарканье/кровотечение | – |
| Поражение сердечно-сосудистой системы | Шумы (на сонных артериях, вертебральных, подключичных, ренальных артериях, абдоминальные, в паху) | + |
| Асимметричность пульса и артериального давления | – | |
| Отсутствие пульсации; нарушение кровообращения | – | |
| Каротидиния, аортальная недостаточность | – | |
| Боль/шум, трения перикарда, ишемическая сердечная боль, застойная сердечная недостаточность | – | |
| Перикардит, кардиомиопатия, инфаркт миокарда/стенокардия | + | |
| Поражение сосудистого эндотелия | + | |
| Абдоминальный синдром | Острая боль в животе, перфорация кишечника/инфаркт, геморрагическая диарея | + |
| Поражение почек | Гипертензия: диастолическая >90 мм рт. ст., систолическая >140 мм рт. ст.; протеинурия (>1 г/сут), гематурия (>1 +/10 эритроциты/мл), креатинин (125–249 мкмоль/л), креатинин (250–499 мкмоль/л), креатинин (>500 мкмоль/л), повышение креатинина >30% или снижение клиренса креатинина >25% | + |
| Поражение нервной системы | Органические расстройства/деменция, судороги (гипертонические), инсульт, потеря сознания, поражение спинного мозга | + |
| Поражение половой системы | Импотенция, выкидыш | – |
| СОЭ | >20 мм/ч | + |
| СРБ | >5 мг/л | + |
Также были клинически переоценены жалобы и анамнез.
Пациентке был установлен диагноз:
Неспецифический аортоартериит (артериит Такаясу), подострое течение, активная фаза, активность III, тип IIa, доокклюзивная стадия, со стенозирующим поражением сонных, подключичных, подвздошных, бедренных артерий, нисходящей аорты, с нарушением зрения (атрофия зрительного нерва OS), поражением нервной системы (лакунарный инфаркт головного мозга в затылочной части) синдромом полиартралгии и полимиалгии, общевоспалительным синдромом.
Пациентке назначено следующее лечение:
I. Болезнь-модифицирующая терапия: метилпреднизолон 48 мг/сут (из расчета — преднизолон 1 мг на кг массы тела) + метотрексат 15 мг/нед + фолиевая кислота 5 мг 3 дня подряд после приема метотрексата.
Симптоматическая терапия: ацетилсалициловая кислота 100 мг/сут ежедневно; розувастатин 10 мг 1 раз в сутки после ужина; рамиприл 10 мг 1 раз в сутки; комбинированный препарат кальция 1000 мг и витамина D3 800 МЕ/сут; деносумаб 60 мг подкожно 1 раз в 6 мес.
II. При оценке состояния пациентки через 3 и 6 мес отмечали значительное улучшение состояния — исчезла боль в суставах и мышцах, а также в желудочно-кишечном тракте, нормализовалась температура тела, существенно уменьшились головокружения, исчезла головная боль, снизилось артериальное давление, что привело к снижению дозы рамиприла до 5 мг/сут, расширились поля зрения. Пациентка субъективно отмечала значительное улучшение состояния. На момент динамического наблюдения через 6 мес после назначения лечения отмечали неактивную фазу заболевания в соответствии с индексом DEI-Тak.
Лабораторные анализы также претерпели существенные позитивные изменения, прежде всего снижение активности.
Общий анализ крови от 12.01.2016 г. — эритроциты — 4,2·10/л, гемоглобин 157 г/л, лейкоциты — 5,2·10/л, тромбоциты — 237·10/л, палочкоядерные — 3%,сегментоядерные — 53%, эозинофилы — 2%, лимфоциты — 34%, моноциты — 8%, СОЭ — 5 мм/ч.
Биохимический анализ крови от 12.01.2016 г. — общий белок 70 г/л, мочевина 3,8 ммоль/л, креатинин 68 мкмоль/л, мочевая кислота 276 мкмоль/л, общий холестерин 5,5 ммоль/л, триглицериды 1,6 ммоль/л, общий билирубин 17,7 мкмоль/л, щелочная фосфатаза 248 ед./л, АлАТ 35 ед./л, АсАТ 41 ед./л, ГГТП 38 ед./л, КФК 17 ед./л, МВ-КФК 11%, сывороточное железо 19,7 мкмоль/л, общий кальций 2,53 ммоль/л, глюкоза крови 4,4 ммоль/л, фибриноген 2,88 г/л. СРБ — 1,2 мг/л.
С целью контроля активности заболевания и подтверждения эффективности лечения через 6 мес пациентке проведено повторное исследование ПЭТ/КТ (рис. 4, 5). ПЭТ/КТ-картина соответствовала выраженной позитивной динамике после лечения НАА за счет снижения метаболической активности стенок магистральных сосудов и уменьшения их толщины. Так, описанная ранее диффузная повышенная фиксация РФП стенками магистральных сосудов при данном исследовании не определялась. Толщина стенки аорты в поддиафрагмальном сегменте составляет 0,2 см (при предыдущем исследовании — 0,4 см). Метаболическая активность от стенки SUVmax = 2,36. Кроме этого, не выявлены стенотические сужения подключичных артерий, что визуализировались при предыдущем исследовании.
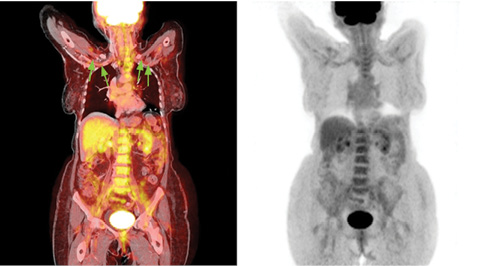
Представленный клинический случай демонстрирует уникальные возможности ПЭТ/КТ в диагностике системных васкулитов, особенно на ранних доокклюзивных стадиях (стадия сохраненного пульса), когда клиническая картина имеет неспецифический и гетерогенный характер. Клиническая картина НАА зависит от того, какие артерии вовлечены в воспалительный процесс и насколько их течение активное [8]. На ранних стадиях преобладают общевоспалительные симптомы без четких признаков топического поражения органов, которые проявляются при прогрессировании артериита и образовании гемодинамически значимого стеноза (>70% исходного диаметра артерии). На этой стадии возникают симптомы, свидетельствующие об ишемии органов, и более развернутая клиническая симптоматика [1]. При поражении нескольких сосудистых стволов клиническая картина характеризуется значительным разнообразием, что заставляет пациентов обращаться к врачам различных специальностей, которые могут быть недостаточно осведомлены о проблеме системных васкулитов. Именно применение ПЭТ/КТ позволяет избежать трудоемкого диагностического поиска по выявлению причины разнообразных жалоб пациентов и четко выявить симптомы артериита/аортита. Кроме этого, накопление РФП в стенке сосудов достоверно коррелирует с активностью НАА, поэтому является достоверным методом оценки эффективности назначенного лечения. Приведенное клиническое наблюдение продемонстрировало возможности ПЭТ/КТ в диагностике и мониторинге активности НАА.
Список использованной литературы
- 1. Гончарова Н.С., Самохвалова М.В., Пахомов А.В. и др. (2013) Артериит Такаясу. Обзор литературы. Артериальная гипертензия, 19(6): 478–486.
- 2. Кметюк Я.В. (2014) Опис та шляхи оптимізації процесу ПЕТ/КТ-обстеження у Всеукраїнському центрі радіохірургії Клінічної лікарні «Феофанія» Державного управління справами. Укр. радіолог. журн., 22 (3): 70–78.
- 3. Покровский А.В., Зотиков А.Е., Юдин В.И. (2002) Диагностика и лечение неспецифического аортоартериита. Руководство для практикующих врачей. Ирис, Москва, 224 с.
- 4. Сміян С.І., Головач І.Ю., Коморовський Р.Р. та ін. (2014) Випадок ранньої «pre-pulseless» діагностики неспецифічного аортоартеріїту за допомогою позитронно-емісійної томографії/комп’ютерної томографії. Укр. ревматол. журн., 3(57): 47–53.
- 5. Щербіна О.В., Кметюк Я.В., Москалець О.І. та ін. (2013) ПЕТ-КТ в Україні: перший досвід. Зб. наук. праць співробітників НМАПО ім. П.Л. Шупика, 22(1): 365–369.
- 6. Aydin S.Z., Yilmaz N., Akar S. et al. (2010) Assessment of disease activity and progression in Takayasu’s arteritis with Disease Extent Index-Takayasu. Rheumatology (Oxford), 49(10): 1889–1893.
- 7. Bicakcigil M., Aksu K., Kamali S. et al. (2009) Takayasu’s arteritis in Turkey — clinical and angiographic features of 248 patients. Clin. Exp. Rheumatol., 27(52): 59–64.
- 8. Direskeneli H., Aydın S.Z., Merkel P.A. (2011) Assessment of disease activity and progression in Takayasu’s arteritis. Clin. Exp. Rheumatol., 29(64): 86–91.
- 9. Flamm S.D., White R.D., Hoffman G.S. (1998) The clinical application of «edema-weighted» magnetic resonance imaging in the assessment of Takayasu’s arteritis. Int. J. Cardiol., 66 (Suppl 1): S151–S159.
- 10. Johnston S.L., Lock R.G., Gompels M.M. (2002) Takayasu arteritis: a review. J Clin Pathol., 55 (7): 481–486.
- 11. Karapolat I., Kalfa M., Keser G. et al. (2013) F18-FDG PET/ CT findings with current clinical disease status in patients with Takayasu’s arteritis. Clin. Exp. Rheumatol., 31 (suppl. 1): S15–S21.
- 12. Keser G., Direskeneli H., Aksu K. (2014) Management of Takayasu arteritis: a systematic review. Rheumatology (Oxford), 53(5): 793–801.
- 13. Kobayashi Y., Ishii K., Oda K. et al. (2005) Aortic wall inflammation due to Takayasu arteritis imaged with 18F-FDG PET coregistered with enhanced CT. J. Nucl. Med., 46(6): 917–922.
- 14. Kötter I., Henes J.C., Wagner A.D. et al. (2012) Does glucocorticosteroid-resistant large-vessel vasculitis (giant cell arteritis and Takayasu arteritis) exist and how can remission be achieved? A critical review of the literature. Clin. Exp. Rheumatol., 30 (Suppl. 1): S114–S129.
- 15. Lee K.H., Cho A., Choi Y.J. et al. (2012) The role of (18)F-fluorodeoxyglucose-positron emission tomography in the assessment of disease activity in patients with takayasu arteritis. Arthritis Rheum., 64(3): 866–875.
- 16. Salvarani C., Cantini F., Boiardi L. et al. (2003) Laboratory investigations useful in giant cell arteritis and Takayasu’s arteritis. Clin. Exp. Rheumatol., 21(32): 23–28.
- 17. Smiyan S., Holovach I., Komorovsky R. et al. (2014) Role of PET/CT in the diagnosis of large vessels vasculitis in a patients with systemic inflammatory response syndrome. Eur. J. Rheumatol., 4: 174–175.
- 18. Tezuka D., Haraguchi G., Ishihara T. et al. (2012) Role of FDG PET-CT in Takayasu arteritis: sensitive detection of recurrences. JACC Cardiovasc. Imaging, 5(4): 422–429.
- 19. Tso E., Flamm S.D., White R.D. et al. (2002) Takayasu arteritis: utility and limitations of magnetic resonance imaging in diagnosis and treatment. Arthritis Rheum., 46: 1634–1642.
- 20. Webb M., Chambers A., AL-Nahhas A. et al. (2004) The role of 18F-FDG PET in characterising disease activity in Takayasu arteritis. Eur. J. Nucl. Med. Mol. Imaging, 31: 627–634.
Адрес для переписки:
Чипко Татьяна Мироновна
03680, Киев, ул. Академика Заболотного, 21
Клиническая больница «Феофания» ГУД,
отделение ревматологии
и внутренней патологии
E-mail: chipko.t@yandex.ua

Leave a comment