Вплив прегабаліну на ефективність лікування хворих на ревматоїдний артрит, асоційований із фіброміалгією
Перебетюк Л.С., Станіславчук М.А.
Резюме. У дослідженні оцінювали вплив нейромодулятора прегабаліну на ефективність терапії у хворих на ревматоїдний артрит (РА), асоційований з фіброміалгією (РАФМ). У 12-тижневому дослідженні взяли участь 90 хворих на РА жінок (середній вік — 50,8±12,1 року), з них у 46 виявлено фіброміалгію (РАФМ). Усі хворі отримували метотрексат (10–15 мг/тиж), глюкокортикоїди в низьких дозах (≤10 мг за преднізолоном), нестероїдні протизапальні препарати. Частина (24 із 46) пацієнток із РАФМ отримували прегабалін (по 150 мг 2 рази на добу). Ефективність лікування оцінювали через 12 тиж терапії за динамікою клініко-лабораторних маркерів активності РА (DAS28, CDAI), функціональною здатністю пацієнтів (HAQ) та визначали частку респондерів за критеріями ACR20, АCR50, ACR70. Під впливом основного лікування у осіб із РАФМ спостерігали регрес запального процесу (кількість набряклих суглобів, швидкість осідання еритроцитів, рівень С-реактивного білка зменшились на 25,2; 22,5 та 39,3%; p<0,05), але не забезпечувалось ефективного зменшення вираженості больового синдрому та клінічної активності захворювання за DAS28, CDAI та HAQ. Через 12 тиж лікування серед пацієнток із РА без фіброміалгії виявлено 52,3; 15,9; 6,8% респондерів за ACR20, АCR50 та ACR70, а серед хворих на РАФМ — лише 22,7; 4,5 та 0,0% (р<0,05). Прийом прегабаліну істотно підвищував ефективність терапії в осіб із РАФМ: потенціював зниження DAS28, CDAI та HAQ (на 19,2; 32,2 та 31,2%) та значно підвищував шанси досягти рівня ACR20 (OR 4,39; 95% СІ 1,27–15,3) через 12 тиж. Отже, фіброміалгія у хворих на РА є незалежним предиктором резистентності до лікування. Застосування прегабаліну зменшує вираженість больового синдрому і суттєво підвищує ефективність хворобо-модифікуючої протиревматичної терапії у осіб із РАФМ.
ВСТУП
Ревматоїдний артрит (РА) — одне з найпоширеніших інвалідизуючих захворювань, що має не лише медичне, а й соціальне значення (Коваленко В.М. та співавт., 2011; Ma V.Y. et al., 2014). РА часто поєднується з іншими патологічними станами, які не лише модифікують його перебіг, але й суттєво погіршують клінічну відповідь пацієнтів на лікування (Яременко О.Б., Микитенко А.М., 2015). Одним із таких станів є фіброміалгія (ФМ), поширеність якої у хворих на РА варіює від 6,6 до 48% (Wolfe F., Michaud K., 2004; Ranzolin A. et al., 2009; Abbasi L., Haidri F.R., 2014; Haliloglu S. et al., 2014; Joharatnam N. et al., 2015). ФМ розглядають як імовірний чинник підвищення тяжкості перебігу і тривалості лікування РА у зв’язку з потенціюванням больового синдрому, поглибленням фізичної, психологічної та соціальної дизадаптації хворих (Ranzolin A. et al., 2009; Tavares R. et al., 2012; Wolfe F. et al., 2014; Joharatnam N. et al., 2015). Найбільш значну проблему у пацієнтів із РА становить біль, який навіть при успішній хворобо-модифікуючій протиревматичній терапії (ХМПРТ) із застосуванням біологічних препаратів залишається на рівні 20–40 балів за візуально-аналоговою шкалою (ВАШ) (Strand V. et al., 2012). Серед 2795 хворих на РА із частково або повністю контрольованими перебігом захворювання понад 60% осіб були не задоволені своїм станом у зв’язку із больовим синдромом, а 80% — відзначали тяжкий і середній біль упродовж останніх 2 міс (Taylor P. et al., 2010). Хворі на РА за наявності ФМ часто необґрунтовано отримують комбіновану ХМПРТ, яка не забезпечує зменшення вираженості болю та клінічної активності захворювання за DAS28 (Naranjo A. et al., 2002; Abbasi L., Haidri F.R., 2014).
Згідно з даними Кокранівського огляду, застосування нейромодуляторів при РА полегшує прояви больового синдрому (Richards B.L. et al., 2012). Однак цей досвід обмежується нефопамом, прийом якого викликав значні побічні ефекти у хворих на РА (Richards B.L. et al., 2012). Тому питання щодо підвищення ефективності лікування хворих на РА за умов коморбідності з ФМ залишається актуальним. За рекомендаціями FDA (2010) для фармакотерапії при ФМ дозволено лише три препарати, з яких найбільш ефективним та безпечним виявився прегабалін (Moore R.A. et al., 2009). Доведена висока ефективність прегабаліну при ФМ та патологічних станах із нейропатичним болем за відсутності серйозних побічних ефектів. Досвід застосування прегабаліну у хворих на РА відсутній, не вивчений його вплив на ефективність ХМПРТ. Тому метою роботи була оцінка впливу нейромодулятора прегабаліну на ефективність стандартної терапії у хворих на РА, асоційований із ФМ (РАФМ).
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
Проведено 12-тижневе відкрите контрольоване дослідження, в яке увійшли 90 хворих на РА жінок (середній вік — 50,8±12,1 року), які перебували на стаціонарному лікуванні в ревматологічному відділенні Вінницької обласної клінічної лікарні ім. М.І. Пирогова. Діагноз РА встановлювали за критеріями ACR/EULAR (2010). Усі пацієнти дали інформовану згоду на участь у дослідженні. Дослідження схвалене Комітетом з біоетики Вінницького національного медичного університету ім. М.І. Пирогова. 57,8% хворих були серопозитивними за ревматоїдним фактором (РФ) та 60,0% — за антитілами до циклічного цитрулінованого пептиду (АЦЦП). У дослідження включали лише пацієнтів із середньою та високою активністю РА (DAS28 >3,2). У 46 хворих РА поєднувався з ФМ. Діагноз ФМ встановлено на основі критеріїв ACR1990 та mACR2010, які потребують наявності щонайменше 11 із 18 специфічних чутливих точок (ЧТ) та 13 (із 31) балів за шкалою фіброміалгічності (ШФ) (Wolfe F. et al., 1990; 2011).
Хворих на РА розподілили на три групи, репрезентативні за віком, тривалістю захворювання, рентгенологічною стадією, функціональним класом, активністю запального процесу: до 1-ї групи увійшли 44 хворих на ізольований РА, до 2-ї та 3-ї групи — 22 та 24 хворих на РАФМ (табл. 1). Усі хворі на РА отримували лікування згідно з клінічним протоколом «Ревматоїдний артрит» (наказ Міністерства охорони здоров’я України від 11.04.2014 р. № 263), яке включало метотрексат у дозі 10–15 мг/тиж; глюкокортикоїди у стабільній дозі, яка не перевищувала 10 мг/добу за преднізолоном; нестероїдні протизапальні препарати у стабільній дозі. Хворі 3-ї групи додатково отримували прегабалін по 150 мг 2 рази на добу. Період відкритого контрольованого лікування становив 12 тиж. Ефективність лікування оцінювали за динамікою клініко-лабораторних маркерів активності РА: кількістю болючих та набряклих суглобів (КБС, КНС), швидкістю осідання еритроцитів (ШОЕ), С-реактивним білком (СРБ), клінічних індексів DAS28, CDAI, функціональною здатністю пацієнтів (HAQ) та визначали кількість респондерів за ACR20, АCR50 та ACR70. Динаміку симптомів ФМ контролювали за показниками ШФ (Wolfe F. et al., 2011).
Вірогідність відмінностей за середніми величинами оцінювали за допомогою t-критерію Стьюдента (для парних або незалежних груп даних), при порівнянні частоти змін користувалися точним методом Фішера та критерієм χ. Оцінювали відношення шансів (OR) та 95% довірчий інтервал (СІ). Вірогідними вважали відмінності при р<0,05.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Групи хворих на ізольований РА та РАФМ були репрезентативними за вихідними показниками активності запального процесу (КНС, ШОЕ, СРБ), але, незважаючи на це, відрізнялися за вираженістю больового синдрому, показниками тяжкості перебігу захворювання та порушеннями фізичних функцій (див. табл. 1). Зокрема, КБС, ВАШ болю, DAS28, CDAI та HAQ були достовірно вищими (в 1,2–1,5 раза) у хворих на РАФМ, ніж у осіб з ізольованим РА. Більш високі показники DAS28, CDAI та HAQ у пацієнтів із РАФМ відзначали й в інших дослідженнях (Ranzolin A. et al., 2009; Tavares R. et al., 2012; Wolfe F. et al., 2014; Joharatnam N. et al., 2015).
| Показник | Група хворих | |||
|---|---|---|---|---|
| 1-ша РА(n=44) | 2-га РАФМ (n=22) | 3-тя РАФМ + прегабалін (n=24) | ||
| Вік, років | M±σ | 50,2±11,6 | 52,3±11,6 | 50,5±13,9 |
| Тривалість РА, міс | M±σ | 87,8±57,9 | 88,6±55,0 | 95,5±66,7 |
| АЦЦП+ | n (%) | 29 (65,9) | 13 (59,1) | 12 (50,0) |
| РФ + | n (%) | 29 (65,9) | 13 (59,1) | 10 (41,7) |
| Рентгенологічна стадія ІІ–ІІІ | n (%) | 38 (86,4) | 18 (81,8) | 19 (79,2) |
| Порушення функціонального стану ІІ ступеня | n (%) | 41(93,2) | 19 (86,4) | 23 (95,8) |
| ШОЕ, мм/год | M±σ | 34,6±10,7 | 29,9±13,4 | 30,8±9,93 |
| СРБ, мг/л | M±σ | 16,8±12,3 | 16,2±15,0 | 14,5±8,13 |
| КНС | M±σ | 5,70±2,32 | 5,36±2,66 | 5,38±2,75 |
| КБС | M±σ | 8,36±2,48 | 11,8±2,70** | 12,6±3,08** |
| ВАШ болю, мм | M±σ | 49,1±11,3 | 64,9±12,0** | 67,5±12,6** |
| DAS28 | M±σ | 5,27±0,51 | 5,70±0,65* | 5,79±0,60* |
| СDAI | M±σ | 23,0±5,09 | 27,8±5,75** | 28,7±6,45** |
| HAQ | M±σ | 1,55±0,44 | 1,80±0,40* | 1,87±0,38* |
| ШФ | M±σ | 9,09±1,89 | 17,8±3,20** | 18,4±3,36** |
| ЧТ | M±σ | 6,70±1,81 | 12,4±2,87** | 12,1±2,71** |
*p<0,05; **p<0,01 відносно 1-ї групи.
Через 12 тиж стандартної терапії у хворих на ізольований РА відзначено достовірну позитивну динаміку клініко-лабораторних маркерів активності запального процесу: КБС та КНС зменшилися на 23,4 та 30,7%, ШОЕ та СРБ — на 25,0 та 35,5% (табл. 2). Під впливом лікування у хворих на ізольований РА достовірно зменшувалася вираженість больового синдрому за ВАШ (на 23,0%), реєстрували достовірне зниження активності захворювання за DAS28 та СDAI (на 13,5 та 25,6%), покращувався функціональний стан за HAQ (на 22,1%).
Коморбідність ФМ з РА негативно відображалася на ефективності стандартної терапії: через 12 тиж у хворих на РАФМ зберігалися скарги на суглобовий больовий синдром, незважаючи на достовірне зниження активності запального процесу. Так, у осіб 2-ї групи під впливом стандартного лікування КНС, ШОЕ та СРБ вірогідно знизилися на 25,2; 21,5 та 39,3%, в той час як КБС та ВАШ болю — лише на 12,5 та 11,4%. У хворих на РАФМ 2-ї групи динаміка DAS28, СDAI та HAQ під впливом стандартної терапії становила лише 8,36; 15,1 та 11,1% і була в 1,6–1,7 раза меншою (p<0,05), ніж у хворих 1-ї групи.
| Показник | Група хворих | |||
|---|---|---|---|---|
| 1-ша РА(n=44) | 2-га РАФМ(n=22) | 3-тя РАФМ + прегабалін (n=24) | ||
| КБС | до включення | 8,36±2,48 | 11,8±2,70 | 12,6±3,08 |
| через 12 тиж | 6,45±2,47 | 10,3±2,85 | 8,75±3,72 | |
| динаміка, % | –23,4±20,2 | –12,5±15,3 | –31,1±22,5 | |
| КНС | до включення | 5,70±2,32 | 5,36±2,66 | 5,38±2,75 |
| через 12 тиж | 4,07±2,18 | 3,86±1,78 | 3,33±2,18 | |
| динаміка, % | –30,7±22,6 | –25,2±16,2 | –39,0±25,8 | |
| ШОЕ,мм/год | до включення | 34,6±10,7 | 29,9±13,4 | 30,8±9,93 |
| через 12 тиж | 26,3±10,8 | 22,5±9,39 | 20,5±8,68 | |
| динаміка ,% | –25,0±17,5 | –21,5±16,8 | –32,7±20,3 | |
| СРБ,мг/л | до включення | 16,8±12,3 | 16,2±15,0 | 14,5±8,13 |
| через 12 тиж | 11,5±9,94 | 10,6±9,66 | 9,74±6,03 | |
| динаміка, % | –35,5±24,5 | –39,3±28,9 | –34,2±27,4 | |
| ВАШ болю, мм | до включення | 49,1±11,3 | 64,9±12,0 | 67,5±12,6 |
| через 12 тиж | 37,2±11,9 | 57,5±15,8 | 29,1±9,82 | |
| динаміка, % | –23,0±18,9 | –11,4±17,3 | –56,1±13,5 | |
| DAS28 (ШОЕ) | до включення | 5,27±0,51 | 5,70±0,65 | 5,79±0,60 |
| через 12 тиж | 4,58±0,85 | 5,21±0,65 | 4,68±1,00 | |
| динаміка, % | –13,5±12,5 | –8,36±7,80 | –19,2±15,4 | |
| СDAI | до включення | 23,0±5,09 | 27,8±5,75 | 28,7±6,45 |
| через 12 тиж | 17,3±5,76 | 23,3±4,74 | 19,4±7,38 | |
| динаміка, % | –25,6±17,3 | –15,1±13,2 | –32,2±20,9 | |
| HAQ | до включення | 1,55±0,44 | 1,80±0,40 | 1,87±0,38 |
| через 12 тиж | 1,21±0,47 | 1,58±0,36 | 1,27±0,47 | |
| динаміка, % | –22,1±22,8 | –11,1±13,6 | –31,2±23,9 | |
*p<0,05; **p<0,01 відносно стану до включення; p<0,05 відносно динаміки показника у 1-й групі; p<0,05 відносно динаміки показника у 2-й групі.
Включення прегабаліну в схему лікування істотно підвищувало ефективність лікування: через 12 тиж у хворих 3-ї групи (які додатково отримували прегабалін) поряд зі зниженням активності запального синдрому суттєво зменшилася і вираженість больового синдрому. Зокрема, КБС зменшилася на 31,1%, КНС — на 39,0%, ШОЕ та СРБ — на 32,7 та 34,2%, істотно знизилася (на 56,1%) ВАШ болю. Загалом динаміка маркерів больового синдрому у хворих 3-ї групи достовірно перевищувала таку у хворих 2-ї групи у 2,2–2,8 раза. У хворих на РАФМ, які отримували прегабалін, через 12 тиж реєстрували достовірне зниження DAS28, СDAI та HAQ на 19,2; 32,2 та 31,2%. Оскільки активність запального процесу під впливом ХМПРТ знижувалася в усіх групах майже еквівалентно, то більш значна динаміка DAS28, СDAI та HAQ у хворих 3-ї групи може пояснюватись ефективним зменшенням вираженості больового синдрому під впливом прегабаліну.
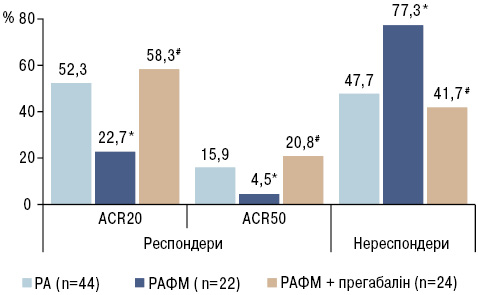
Для порівняння ефективності різних схем фармакотерапії РА в кожній групі визначили частку респондерів ACR20; ACR50; АCR70 (рис. 1). За умов стандартної терапії серед хворих на ізольований РА через 12 тиж виявилося 23 (52,3%) респондери за ACR20, з них 7 (15,9%) респондерів за ACR50 та 3 (6,8%) респондерів за ACR70, що в цілому узгоджується із даними літератури щодо ефективності базисної терапії метотрексатом у зазначені терміни (Zintzaras E. et al., 2008). Стандартна терапія у
хворих на РАФМ забезпечила досягнення ACR20 лише у 5 (22,7%) осіб, ACR50 — у 1 (4,5%) хворого, а ACR70 не досяг жоден пацієнт. Додавання до терапії прегабаліну забезпечило досягнення критеріїв ACR20; ACR50; ACR70 у 58,3; 20,8 та 12,5% хворих на РАФМ. Отже, у хворих на РАФМ ефективність стандартної терапії майже у 3,5 раза нижча, ніж у хворих на ізольований РА (OR=3,48; 95% СІ 1,13; 10,7). Включення у схему лікування прегабаліну підвищувало ефективність лікування у хворих на РАФМ і збільшувало шанси досягнення ACR20 через 12 тиж у >4 рази (OR=4,39; 95% СІ 1,27–15,3).
Регрес запального процесу під впливом стандартного лікування (без прегабаліну) у хворих на РАФМ не асоціювали зі зменшенням фіброміалгічних феноменів (табл. 3). Водночас прийом прегабаліну достовірно сприяв зменшенню вираженості ознак фіброміалгічності (за критеріями mACR2010) у хворих на РАФМ: через 12 тиж індекс поширеності болю (ІПБ) знизився на 34,1%; шкала тяжкості симптомів (ШТС) — на 25,7%, загальна тяжкість психологічних симптомів — на 31,2% та соматичні симптоми — на 11,1%. Якщо у хворих на РАФМ до прийому прегабаліну ІПБ та ШТС становили 9,0 [8,0; 10,0] та 9,0 [8,0; 10,0], то наприкінці 12-го тижня — 6,0 [5,0; 8,0] та 7,0 [5,8; 8,0] відповідно (p<0,05). У 3-й групі хворих на РАФМ виявилося 17 (70,8%) осіб, у яких через 3 міс прийому прегабаліну кількість позитивних ЧТ зменшилась (на 1–3) порівняно із початковим станом, що може свідчити про зменшення центральної сенситизації, в той час як у 6 (27,3%) осіб 2-ї групи кількість ЧТ навіть збільшилася (на 1–2). Хворі на РАФМ, які отримували прегабалін, відзначали зменшення вираженості втоми, розбитості вранці, покращення сну, рідше відзначали біль внизу живота (рис. 2).
Прегабалін добре переносився пацієнтами і не викликав значних побічних ефектів. Наприкінці 12-го тижня 2 (8,3%) хворих відзначали гіпосалівацію, 2 (8,3%) — підвищення апетиту та 3 (12,5%) — сонливість, які пов’язували із прийомом прегабаліну, що узгоджується з даними літератури. За даними R. Moore та співавторів (2009), найбільш типовими побічними ефектами прегабаліну (в дозі 600 мг/добу) були сонливість (15–25%) та запаморочення (27–46%), а серйозних побічних ефектів виявлялося не більше, ніж у групі плацебо.
під впливом різних варіантів лікування (M±σ)
| Показник | Група хворих | |||
|---|---|---|---|---|
| 1-ша РА(n=44) | 2-га РАФМ(n=22) | 3-тя РАФМ + прегабалін (n=24) | ||
| ШФ | до включення | 9,09±1,89 | 17,8±3,20 | 18,4±3,36 |
| через 12 тиж | 8,39±1,93 | 17,3±3,22 | 12,4±2,92 | |
| динаміка, % | –7,74±10,5 | –2,88±7,67 | –31,0±16,8 | |
| ІПБ | до включення | 5,02±1,42 | 9,00±2,56 | 9,54±3,08 |
| через 12 тиж | 4,57±1,32 | 8,73±2,60 | 5,88±2,23 | |
| динаміка, % | –7,86±14,2 | –3,01±7,14 | –34,1±23,8 | |
| ШТС | до включення | 4,07±1,23 | 8,82±1,44 | 8,83±1,31 |
| через 12 тиж | 3,82±1,28 | 8,55±1,65 | 6,54±1,53 | |
| динаміка, % | –7,31±19,2 | –2,99±10,4 | –25,7±14,3 | |
| ЧТ | до включення | 6,70±1,81 | 12,4±2,87 | 12,1±2,71 |
| через 12 тиж | 6,25±1,70 | 12,2±3,13 | 11,0±2,67 | |
| динаміка, % | –6,16±9,56 | –1,56±10,8 | –9,51±7,43 | |
*p<0,05 та **p<0,01 відносно стану до включення; p<0,05 та p<0,01 відносно динаміки у 1-й групі; p<0,05 та p<0,01 відносно динаміки у 2-й групі.
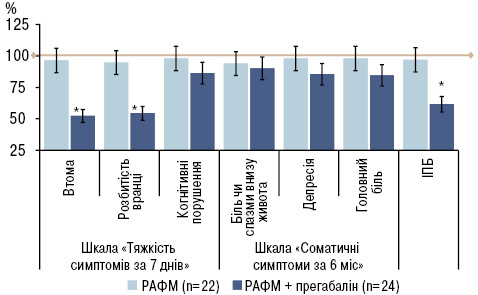
Таким чином, включення до комплексу лікування хворих на РАФМ нейромодулятора прегабаліну дозволяє не лише зменшити вираженість клінічних проявів больового синдрому, ознак фіброміалгічності, але й суттєво підвищити ефективність терапії РА в цілому.
ВИСНОВКИ
1. Наявність ФМ у хворих на РА — незалежний предиктор недостатньої клінічної відповіді на стандартну терапію, яка через 12 тиж забезпечила досягнення рівня ACR20 у 52,3% пацієнтів з ізольованим РА і лише у 22,7% хворих на РАФМ (OR 3,48; 95% СІ 1,13–10,7).
2. Стандартна терапія забезпечує регрес запального синдрому у хворих на РАФМ (КНС, ШОЕ, СРБ знизилися на 25,2; 22,5 та 39,3%, як і у хворих на ізольований РА), але не викликала ефективного зменшення вираженості больового синдрому. 12-тижневий прийом прегабаліну (по 150 мг 2 рази на добу) достовірно підвищує ефективність лікування: зменшує вираженість суглобового больового синдрому за ВАШ (на 56,1±13,5%) та збільшує досягнення ACR20 (OR 4,39; 95% СІ 1,27–15,3) у хворих на РАФМ.
3. Застосування прегабаліну сприяє регресу центрального больового синдрому та психосоматичних розладів у хворих на РАФМ, що підтверджується достовірним зниженням показників ШФ.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- Коваленко В.Н., Головач И.Ю., Борткевич О.П. (2011) Индивидуализация лечения ревматоидного артрита: курс на достижение оптимальных результатов. Укр. ревматол. журн., 3(45): 5–15.
- Яременко О.Б., Микитенко А.М. (2015) Влияние коморбидности и системных проявлений ревматоидного артрита на эффективность и переносимость лечения синтетическими базисными препаратами. Укр. ревматол. журн., 1(59): 28–35.
- Abbasi L., Haidri F.R. (2014) Fibromyalgia complicating disease management in rheumatoid arthritis. J. Coll. Physicians Surg. Pak., 24(6): 424–427.
- Haliloglu S., Carlioglu A., Akdeniz D. et al. (2014) Fibromyalgia in patients with other rheumatic diseases: prevalence and relationship with disease activity. Rheumatol. Int., 34(9): 1275–1280.
- Joharatnam N., McWilliams D.F., Wilson D. et al. (2015) A cross-sectional study of pain sensitivity, disease-activity assessment, mental health, and fibromyalgia status in rheumatoid arthritis. Arthritis Res. Ther., 17(1): 11.
- Ma V.Y., Chan L., Carruthers K.J. (2014) Incidence, prevalence, costs, and impact on disability of common conditions requiring rehabilitation in the United States: stroke, spinal cord injury, traumatic brain injury, multiple sclerosis, osteoarthritis, rheumatoid arthritis, limb loss, and back pain. Arch. Phys. Med. Rehabil., 95(5): 986–995.
- Moore R.A., Straube S., Wiffen P.J. et al. (2009) Pregabalin for acute and chronic pain in adults. Cochrane Database Syst. Rev., (3):CD007076. doi: 10.1002/14651858.CD007076.pub2.
- Naranjo A., Ojeda S., Francisco F. et al. (2002) Fibromyalgia in patients with rheumatoid arthritis is associated with higher scores of disability. Ann. Rheum. Dis., 61(7): 660–661.
- Ranzolin A., Brenol J.C., Bredemeier M. et al. (2009) Association of concomitant fibromyalgia with worse disease activity score in 28 joints, health assessment questionnaire, and short form 36 scores in patients with rheumatoid arthritis. Arthritis. Rheum., 61(6): 794–800.
- Richards B.L., Whittle S.L., Buchbinder R. (2012) Neuromodulators for pain management in rheumatoid arthritis. Cochrane Database Syst. Rev., 1: CD008921. doi: 10.1002/14651858.CD008921.pub2.
- Strand V., Burmester G.R., Ogale S. et al. (2012) Improvements in health-related quality of life after treatment with tocilizumab in patients with rheumatoid arthritis refractory to tumour necrosis factor inhibitors: results from the 24-week randomized controlled RADIATE study. Rheumatology (Oxford), 51(10): 1860–1869.
- Tavares R., Pope J.E., Tremblay J.L. et al. (2012) Time to disease-modifying antirheumatic drug treatment in rheumatoid arthritis and its predictors: a national, multicenter, retrospective cohort. J. Rheumatol., 39(11): 2088–2097.
- Taylor P., Manger B., Alvaro-Gracia J. et al. (2010) Patient perceptions concerning pain management in the treatment of rheumatoid arthritis. J. Int. Med. Res., 38(4): 1213–1224.
- Wolfe F., Clauw D.J., Fitzcharles M.A. et al. (2011) Fibromyalgia criteria and severity scales for clinical and epidemiological studies: a modification of the ACR Preliminary Diagnostic Criteria for Fibromyalgia. J. Rheumatol., 38(6): 1113–1122.
- Wolfe F., Michaud K. (2004) Severe rheumatoid arthritis (RA), worse outcomes, comorbid illness, and sociodemographic disadvantage characterize ra patients with fibromyalgia. J. Rheumatol., 31(4): 695–700.
- Wolfe F., Michaud K., Busch R.E. et al. (2014) Polysymptomatic distress in patients with rheumatoid arthritis: understanding disproportionate response and its spectrum. Arthritis Care Res. (Hoboken), 66(10): 1465–1471.
- Wolfe F., Smythe H.A., Yunus M.B. et al. (1990) The Americаn College Of Rheumatology 1990 Criteria for the Classification of Fibromyalgia. Report of the Multicenter Criteria Committee. Arthr. Rheum., 33(2): 160–172.
- Zintzaras E., Dahabreh I.J., Giannouli S. et al. (2008) Infliximab and methotrexate in the treatment of rheumatoid arthritis: a systematic review and meta-analysis of dosage regimens. Clin. Ther., 30(11): 1939–1955.
ВЛИЯНИЕ ПРЕГАБАЛИНА НА ЭФФЕКТИВНОСТЬ ЛЕЧЕНИЯ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ, АССОЦИИРОВАННЫМ С ФИБРОМИАЛГИЕЙ
Резюме. В исследовании оценивали влияние нейромодулятора прегабалина на эффективность терапии у больных ревматоидным артритом (РА), ассоциированным с фибромиалгией (РАФМ). В 12-недельном исследовании участвовали 90 больных РА женщин (средний возраст — 50,8±12,1 года), из них у 46 выявлена фибромиалгия (РАФМ). Все больные получали метотрексат (10–15 мг/нед), глюкокортикоиды в низких дозах (≤10 мг по преднизолону), нестероидные противовоспалительные препараты. Часть (24 из 46) пациенток с РАФМ получали прегабалин (по150 мг 2 раза в сутки). Эффективность лечения оценивали через 12 нед терапии по динамике клинико-лабораторных маркеров активности РА (DAS28, CDAI), функциональной способностью пациентов (HAQ) и определяли долю респондеров по критериям ACR20, АCR50, ACR70. Под влиянием основного лечения у лиц с РАФМ наблюдали регресс воспалительного процесса (количество отечных суставов, скорость оседания эритроцитов, уровень С-реактивного белка уменьшились на 25,2; 22,5 и 39,3%; p<0,05), но не обеспечивалось эффективного уменьшения выраженности болевого синдрома и клинической активности заболевания по DAS28, CDAI и HAQ. Через 12 нед лечения среди пациенток с РА без фибромиалгии выявлено 52,3; 15,9; 6,8% респондеров по ACR20, АCR50 и ACR70, а среди больных РАФМ — только 22,7; 4,5 и 0,0% (р<0,05). Прием прегабалина существенно повышал эффективность терапии у лиц с РАФМ: потенцировал снижение DAS28, CDAI и HAQ (на 19,2; 32,2 и 31,2%) и значительно повышал шансы достичь уровня ACR20 (OR 4,39; 95% CI 1,27–15,3) через 12 нед. Итак, фибромиалгия у больных РА является независимым предиктором резистентности к лечению. Применение прегабалина уменьшает выраженность болевого синдрома и существенно повышает эффективность болезнь-модифицирующей противоревматической терапии у лиц с РАФМ.
ревматоидный артрит, фибромиалгия, лечение, прегабалин.
Адреса для листування:
Станіславчук Микола Адамович
21018, Вінниця, вул. Пирогова, 56
Вінницький національний медичний
університет ім. М.І. Пирогова
E-mail: mstanislav53@yahoo.com

Leave a comment