Подагра: рік у огляді 2025 р.
Редакція «Українського ревматологічного журналу»
Резюме. Частота подагри неухильно зростає протягом останніх десятиліть, тоді як її лікування все ще залишається недостатньо ефективним. Накопичується дедалі більше доказів мультифакторної етіології цього захворювання, що включає генетичну схильність, вплив факторів довкілля та дисбіоз кишкової мікробіоти. Сучасні досягнення у біомолекулярних і комп’ютерних науках дали змогу отримати значно більше генетичних, епігенетичних, транскриптомних, протеомних і метаболомних даних щодо гіперурикемії та молекулярних механізмів, пов’язаних із подагрою. Крім того, взаємозв’язок подагри із серцево-судинними, метаболічними та нирковими захворюваннями може відкрити нові терапевтичні мішені для протизапальної та уратзнижувальної терапії. Мета цього огляду: представити найновіші дані щодо досліджень подагри, епідеміології, генетики, молекулярних механізмів, діагностичних підходів та сучасних терапевтичних досягнень.
DOI: 10.32471/rheumatology.2707-6970.20541
Зростання інтересу до досліджень подагри може пояснюватися кількома факторами: постійним зростанням поширеності цього захворювання у світі, накопиченням доказів щодо супутніх коморбідних станів, а також відкриттям нових патогенетичних механізмів, які можуть лежати в основі інших хвороб, у патогенезі яких переважає запалення.
Також суттєво, що багато нових лікарських засобів, схвалених для лікування подагри, потенційно можуть бути випробувані й при рідкісних запальних або аутоімунних захворюваннях.
Еволюція глобальної епідеміології та можливості для діагностики
Подагра — це метаболічне захворювання, поширеність якого у світі значно зросла протягом останніх десятиліть [1, 2]. Систематичний аналіз глобального тягаря подагри, проведений у 2024 р., що охопив 35 країн, показав, що у 2020 р. близько 55 млн людей у світі мали це захворювання [3–5]. Стандартизована за віком поширеність становила близько 660 випадків на 100 тис. населення, що відповідає зростанню на 22,5% за останні 30 років.
У глобальному масштабі поширеність подагри у 2020 р. була приблизно втричі вищою серед чоловіків, ніж серед жінок, і чітко зростала з віком [1, 2]. Водночас не слід недооцінювати вплив статі на діагностику захворювання [3].
За прогнозами, до 2050 р. кількість пацієнтів із подагрою може зрости до 96 млн осіб, причому очікується поступове зміщення основного тягаря захворювання з країн із високим рівнем доходу до країн із низьким і середнім рівнем доходу [4].
Серед факторів, що найбільше впливають на кількість років життя з інвалідністю (YLD), пов’язаних із подагрою, ключову роль відіграють підвищений індекс маси тіла та порушення функції нирок, на які припадає відповідно 34 і 12% цього показника [4].
Аналіз даних дослідження Глобального тягаря хвороб (Global Burden of Disease 2021) для осіб віком 55 років і старше показав стандартизовану за віком поширеність 2505,4 випадку на 100 тис. населення [2].
У різних країнах темпи зростання поширеності подагри суттєво відрізняються. Найбільш суттєве підвищення зареєстровано у США (90,6%), далі йдуть Австралія (45,9%) та Канада (30,3%). Найменше зростання зафіксовано в Італії, де показник поширеності підвищився лише на 6,6%, а стандартизована захворюваність — на 2,8% [5].
Що стосується діагностики, окрім виявлення кристалів моноурату натрію (МУН) у синовіальній рідині, діагностика подагри ґрунтується також на використанні візуалізаційних методів, зокрема рентгенографії, ультразвукового дослідження (УЗД), комп’ютерної томографії (КТ), двохенергетичної КТ (ДЕКТ) та магнітно-резонансної томографії (МРТ). Ці методи також відіграють важливу роль у клінічному моніторингу пацієнтів і прогнозуванні перебігу захворювання [6].
Так, згідно з рекомендаціями Європейського альянсу ревматологічних асоціацій (European Alliance of Associations for Rheumatology — EULAR) 2023 р. щодо використання методів візуалізації при кристал-індукованих артропатіях, УЗД та ДЕКТ рекомендуються як основні методи візуалізації при діагностиці подагри. Вони можуть використовуватися як для виявлення відкладення кристалів, так і для оцінки запалення під час подальшого спостереження пацієнтів [6]. Зокрема, ДЕКТ підтверджує свою здатність прогнозувати майбутні загострення [7]. УЗД виявилася корисною для специфічної оцінки відкладення уратів всередині та навколо сухожиль (тобто чотириголового м’яза стегна, надколінка та ахіллового м’яза), особливо на ранніх стадіях. Нещодавні дослідження подагри зосереджені на ідентифікації потенційних діагностичних біомаркерів, таких як розчинні маркери крові (наприклад E-кадгерин) [8], мікроРНК [9], деякі хемокіни (наприклад IP10, інтерлейкін (ІЛ)-8) та фактори росту (наприклад ендотелію судин А (VEGF-A)) у сироватці крові та синовіальній рідині за допомогою високопродуктивної протеоміки [10].
1. Дослідження «Глобальний тягар хвороб» показує зростання поширеності подагри на 22,5% за останні 30 років [1].
2. Україна має стабільні показники захворюваності, поширеності та років життя, скоригованих з урахуванням інвалідності (disability-adjusted life years — DALY) за період 1990–2021 рр., подібно до багатьох інших країн регіону [11]. Так, річна відсоткова зміна (annual percentage change — EAPC) цих показників за зазначений період становила:
- захворюваності — 0,87 (0,77–0,98);
- розповсюдженості — 0,90 (0,78–1,01);
- DALY — 0,91 (0,80–1,03).
3. Люди похилого віку, ймовірно, несуть найбільший тягар хвороб [2].
Генетичні аспекти гіперурикемії та подагри
Останніми роками дослідження генетичних детермінант подагри значно розширилися завдяки використанню великих біобанків і сучасних геномних технологій. Такі гени, як SLC2A9 (GLUT9), ABCG2 та SLC22A12 (URAT1), залишаються центральними для контролю уратів та схильності до подагри [9]. Великомасштабні геномні дослідження асоціацій (genome-wide association studies — GWAS) дозволили ідентифікувати численні генетичні варіанти, пов’язані з рівнем сечової кислоти в сироватці крові та ризиком розвитку подагри.
Нещодавній метааналіз, що охопив дані понад 2,6 млн осіб різного походження, виявив 351 генетичний локус, асоційований із концентрацією сечової кислоти [9]. До клінічно значущих генів належать CTBP1, SKIV2L, WWP2, які беруть участь у регуляції рівня уратів, а також асоційовані із серцево-судинними захворюваннями та артеріальною гіпертензією. Крім того, дослідження виявило високу генетичну кореляцію рівнів уратів між європейськими та східноазійськими популяціями, але з певними відмінностями: у європейців виявили більше збагачення генетичними сигналами у тканинах серцево-судинної системи, тоді як у азійських популяціях — тканинах імунної та респіраторної систем (наприклад слизовій оболонці носа). Це підкреслює важливість врахування генетичного різноманіття при розробці терапевтичних підходів [9].
Додатковий аналіз у японській когорті також підтвердив генетичну основу подагри, ідентифікувавши 9 значущих локусів (зокрема NFAT5, IGF1R, BICC1) з відношенням шансів у межах 1,12–1,30. Особливо примітним є ген NFAT5, який виявився залученим у петлю зворотного зв’язку, що посилює продукцію сечової кислоти через альдозоредуктазу, що відкриває нові потенційні терапевтичні мішені при подагрі та гіперурикемії. Створена на основі цих локусів шкала генетичного ризику продемонструвала площу під кривою (AUC) відповідних значень близько 0,75, що підтверджує потенційну корисність інструменту для прогнозування схильності до подагри та розвитку підходів геноморієнтованої прецизійної медицини [9].
Генетичні дослідження також дозволили краще зрозуміти запальні процеси, що лежать в основі патофізіології подагри. Зокрема, нещодавні GWAS-дослідження виявили ключові сигнальні шляхи, серед яких активація інфламасоми NLRP3, епігенетичне ремоделювання та регуляція клітинної осмолярності [12]. Серед важливих генів FADS2 бере участь у метаболізмі ліпідів та запальній відповіді, тоді як IL1R1 та IL6R кодують рецептори цитокінів, що відіграють центральну роль у запаленні при подагрі.
Крім того, дослідження подагри з початком у підлітковому віці виявило 2 нові локуси — RCOR1 та FSTL5-MIR4454, підкресливши їхню участь у запальних процесах незалежно від рівня уратів [10]. Функціональні аналізи показали, що RCOR1, регулятор імунних та запальних реакцій, зумовлює розвиток подагричного запалення через посилену продукцію інтерлейкінів, зокрема, ІЛ-1β. Ці відкриття забезпечують перспективи для таргетної терапії, спрямованої на зменшення вираженості запалення та запобігання прогресуванню захворювання.
Аналіз імунної інфільтрації додатково продемонстрував підвищений рівень активованих CD4-T-клітин, γδ-T-клітин та інших імунних клітин у пацієнтів із подагрою, що підкреслює можливі терапевтичні мішені при поєднанні подагри та атеросклерозу. Взаємодію між запаленням та імунною активацією також досліджували Wang та співавтори [13], які за допомогою аналізу мереж коекспресії генів (weighted gene co-expression network analysis) ідентифікували 76 генів із підвищеною експресією та 28 генів зі зниженою експресією при подагрі. Серед ключових генів-вузлів були CXCL8, CXCL1 та CXCL2, пов’язані із взаємодіями цитокінів та їхніх рецепторів, що підкреслює їхню роль у міграції імунних клітин та розвитку запалення. Функціональна валідація на зразках пацієнтів і в клітинній моделі подагри THP-1 підтвердила їхній потенціал як діагностичних біомаркерів та терапевтичних мішеней.
Подальший внесок у розуміння патогенезу подагри зробили Major та співавтори, які використали метод менделівської рандомізації та продемонстрували можливу причинну роль клонального гемопоезу невизначеного потенціалу (CHIP) у розвитку подагри [12]. Це відкриття привернуло увагу до генів TET2 та DNMT3A, що є ключовими регуляторами епігенетичних модифікацій та ремоделювання хроматину. CHIP зумовлений соматичними мутаціями в гемопоетичних стовбурових клітинах і зумовлює системне запалення та активації імунної системи, потенційно посилюючи запальну відповідь на кристали МУН при подагрі. Це відкриття створює нові можливості для терапевтичного втручання, зокрема шляхом таргетування епігенетичних механізмів та CHIP-асоційованих запальних процесів, щоб модулювати прогресування і тяжкість захворювання.
Поєднання метаболомних і генетичних даних може забезпечити глибше розуміння патофізіології подагри. Дослідження з використанням менделівської рандомізації ідентифікували 55 метаболітів крові, деякі з них (наприклад гексаноїлглутамін, маноза та співвідношення фосфати / маноза) були пов’язані з ризиком розвитку подагри, що підкреслює їхній потенціал як біомаркерів [14]. Разом із цими метаболітами автори ідентифікували ще три метаболічні шляхи — метаболізм D-глутаміну і D-глутамату, біосинтез аргініну та метаболізм бутирату, — які потенційно залучені у патогенез подагри за результатами інтегративних аналізів. Ці шляхи можуть зумовлювати підвищення продукції сечової кислоти, системне запалення та зміни функції нирок, що підкреслює їхню роль у етіології захворювання. Отримані результати дають нові уявлення про метаболічні тригери подагри та можуть відкрити перспективні терапевтичні мішені для модифікації перебігу та тяжкості хвороби.
Нові підходи, зокрема одноклітинна транскриптоміка (single-cell transcriptomics) та аналіз eQTL, ще більше уточнили наше розуміння динаміки експресії генів при подагрі. Ці методи дозволили ідентифікувати клітинноспецифічні патерни регуляції генів, особливо в імунних клітинах (наприклад макрофагах і клітинах T-хелперах), які відіграють ключову роль у розвитку подагричних нападів. Аналіз eQTL також дозволив пов’язати такі гени, як TRIM46 та KRTCAP2, зі змінами імунної відповіді, що підкреслює складну взаємодію між генетичними факторами та активацією імунної системи [15].
Хоча ці досягнення свідчать про значний прогрес, впровадження генетичних відкриттів у клінічну практику все ще залишається складним завданням. Подальші дослідження мають бути спрямовані на інтеграцію генетичних, транскриптомних і метаболомних даних з метою виявлення терапевтичних мішеней, придатних для клінічного застосування.
1. Гени, пов’язані із запаленням (зокрема NLRP3, IL1R1, IL6R) та епігенетичними механізмами, відіграють важливу роль у патофізіології подагри і можуть бути мішенями для зменшення вираженості запалення та уповільнення прогресування захворювання [12].
2. Дані метаболоміки, включно з такими метаболітами крові, як гексаноїлглутамін, а також метаболічними шляхами, зокрема біосинтезом аргініну, можуть доповнювати генетичні дослідження, пропонуючи нові біомаркери та потенційні терапевтичні мішені [14].
Погляд на патогенетичні механізми
Кристали МУН діють як ендогенні сигнали небезпеки, що запускають активацію інфламасоми NLRP3 і, зрештою, призводять до вивільнення IЛ-1β та IЛ-18. Подальша активація інфламасоми індукує сигнальні шляхи, які забезпечують вивільнення прозапальних цитокінів і хемокінів, що, своєю чергою, залучають нейтрофіли. Цей каскад завершується підтриманням запалення та ушкодженням тканин [15, 16].
Протягом останнього року кілька дослідницьких груп зосередили свої зусилля на кращому розумінні механізмів, пов’язаних з активацією інфламасоми NLRP3 у пацієнтів із подагрою.
Lee та співавтори [17] встановили, що ядерний рецепторний коактиватор 6 (NCOA6), який бере участь в олігомеризації NLRP3 та ASC, значною мірою експресується в макрофагах запаленої ділянки синовіальної оболонки. Крім того, експресія NCOA6 підвищувалася в моноцитах здорових донорів після введення кристалів МУН. Також показано, що NCOA6 взаємодіє з мотивами гідролізу аденозинтрифосфату (АТФ) у домені NACHT білка NLRP3, сприяючи олігомеризації комплексу NLRP3-ASC і тим самим індукуючи продукцію ІЛ-1β [17].
Активація інфламасоми NLRP3 також може регулюватися змінами рівня нікотинамідаденіндинуклеотиду (NAD+) у клітині — важливого кофактора багатьох ферментативних реакцій, що споживають NAD+. Внутрішньоклітинний рівень NAD+ значною мірою залежить від екологічних стимулів і різноманітних клітинних стресорів, а виснаження NAD+, індуковане кластером диференціації 38 (CD38), забезпечує сигнал праймінгу для активації інфламасоми [16].
Alabarse та співавтори встановили, що в макрофагах експресія CD38 індукується кристалами МУН через активацію транскрипційних факторів NF-κB та STAT і асоціюється зі зниженням рівня NAD+, а також із індукцією ІЛ-1β та CXCL1. Крім того, баланс NAD+/NADH пов’язаний із сигналізацією сиртуїнів, залежних від NAD+, і зниження співвідношення NAD+/NADH пов’язане з мітохондріальною дисфункцією через пригнічення активності SIRT3. За допомогою RNA-seq-аналізу автори показали, що CD38 контролює декілька шляхів запалення, модульованих кристалами МУН, зокрема металоредуктазу STEAP4, яка зумовлює оксидативний стрес, активацію NF-κB та посилену диференціацію моноцитів / макрофагів у остеокласти [18].
Нещодавні дослідження продемонстрували, що патогенез подагри включає позаклітинний АТФ (пАТФ), який через активацію рецептора P2X7R відіграє ключову роль в активації інфламасоми NLRP3. Значення цього механізму в патогенезі подагри через регуляцію CD39 вивчали Luo та співавтори [19]. CD39 — це фермент, який може вести до деградації пАТФ, запобігаючи таким чином активації інфламасоми та одночасно підвищуючи продукцію аденозину, що, своєю чергою, викликає протизапальну відповідь. Дійсно, дефіцит CD39 був пов’язаний з активацією інфламасоми NLRP3 у моделі подагри in vivo та in vitro. Автори також встановили, що у пацієнтів із подагрою експресія CD39 підвищена на моноцитах і нейтрофілах, що може свідчити про його участь у пригніченні запальної реакції [19].
Різні агоністи NLRP3, включаючи кристали МУН, можуть спричиняти вихід калію (K+) через канал TWIK2, що є важливим механізмом активації інфламасоми NLRP3. Song та співавтори [20] продемонстрували, що інгібування TWIK2 ефективно зменшує вивільнення ІЛ-1β з макрофагів, оброблених кристалами МУН, що підкреслює важливість цього механізму у запуску активації інфламасоми NLRP3.
Крім того, встановлено, що сигнал, опосередкований виходом K+, бере участь в убіквітинуванні білка SIRT3 і підтриманні мітохондріального гомеостазу. У макрофагах, стимульованих кристалами МУН, інгібування TWIK2 зменшує убіквітинування SIRT3 та покращує функцію мітохондрій шляхом зниження експресії мітохондріальної E3-убіквітинлігази MARCH5 [20].
Нарешті, порушення механізмів, що регулюють активацію інфламасоми NLRP3, може бути однією з причин гіперзапалення у пацієнтів із подагрою. Ehirchiou та співавтори [21] дослідили молекулярні механізми негативного контролю активації інфламасоми NLRP3, у яких бере участь інтегрин CD11b. Дефіцит CD11b у макрофагах, стимульованих кристалами МУН, призводив до підвищеної продукції ІЛ-1β. Відсутність CD11b також впливала на метаболічні шляхи, що призводило до зниження споживання кисню та підвищення гліколізу (аеробного гліколізу) — характерної ознаки активації інфламасоми NLRP3 [21].
Активація інфламасоми NLRP3 також регулюється позаклітинною осмолярністю та явищем зменшення об’єму клітини; зокрема, вихід іонів хлориду (Cl−) розглядається як важливий етап ASC-опосередкованої олігомеризації NLRP3. Chirayath та співавтори [22] описали новий патофізіологічний механізм MSU-індукованого запалення, пов’язаний із аніонними каналами LRRC8 (leucine-rich repeat-containing 8) та регуляцією клітинного об’єму. LRRC8 активуються за умов низької осмолярності та запускають процес регуляторного зменшення об’єму клітини, виводячи Cl− та осмоліти для відновлення нормального об’єму клітини. Автори встановили, що вплив кристалів МУН запускає активацію інфламасоми через активацію каналів LRRC8. Подальше вивільнення АТФ активує пуринергічні рецептори P2Y2 та P2Y6, що врешті призводить до активації інфламасоми через внутрішньоклітинну кальцієву сигналізацію [22].
Кілька досліджень також розглядали роль клітинної смерті, зокрема піроапоптозу (pyroptosis) та утворення позаклітинних нейтрофільних пасток (NETs) у патогенезі подагри [23]. Так, NETs — це мережа хроматину та антимікробних білків, що вивільняються нейтрофілами. Активне вивільнення NETs, відоме як NETosis, є формою загибелі нейтрофілів, яка відрізняється від некрозу та апоптозу. При подагрі NETs, індуковані кристалами МУН, можуть сприяти завершенню запалення, інкапсулюючи кристали МУН та деградуючи цитокіни й хемокіни [24].
Проте повідомлялося, що надмірне утворення NETs може, навпаки, збільшувати вираженість запалення. Із індукцією NETs також пов’язаний такий процес, як піроапоптоз — форма запальної клітинної смерті, опосередкована активацією інфламасом, що призводить до утворення пор у плазматичній мембрані за участю білків родини газдермінів (gasdermin — GSDM) [24].
Chen та співавтори [24] дослідили також роль фізико-хімічних властивостей кристалів МУН у запуску клітинної смерті та формуванні NETs. Встановлено, що розмір кристалів МУН впливає на піроапоптоз нейтрофілів і макрофагів кісткового мозку, індукований через активацію інфламасоми NLRP3. Крім того, розмір кристалів також визначає утворення NETs та агрегованих NETs (aggNETs) [24].
Tan та співавтори [25] досліджували формування NETs та його зв’язок із прогресуванням подагричного запалення. У моделі in vitro автори встановили, що NETs, індуковані кристалами МУН, сприяють активації інфламасоми NLRP3, активації макрофагів та їхній поляризації у фенотип M1. NETs також були пов’язані з метаболічними змінами у макрофагах через гексокіназу-2, ключовий фермент гліколізу. Інгібування NETs сприяло реверсії поляризації макрофагів і зменшенню вираженості запалення як in vitro, так і in vivo [25].
Нарешті, Xu та співавтори [26] описали роль рецептора, активованого проліфератором пероксисом γ (PPARγ), у зменшенні прогресування подагри шляхом пригнічення активації інфламасоми NLRP3. Автори припустили, що порушення функції PPARγ пов’язане з піроапоптозом, опосередкованим NLRP3, та секрецією прозапальних цитокінів. Встановлено, що механізм убіквітинування та деградації PPARγ, опосередкований білком BRD4 та MDM2, посилюється при подагрі. Зокрема, BRD4 транскрипційно активує MDM2, що призводить до убіквітинування та деградації PPARγ, що, своєю чергою, запускає активацію інфламасоми та піроапоптоз [26].
Виявлено нові механізми активації інфламасоми NLRP3 при подагрі. Кристали МУН індукують її активацію через ядерний коактиватор NCOA6, виснаження NAD+, дефіцит CD11b та CD39, пов’язаний із порушенням деградації зАТФ, а також через регуляцію клітинного об’єму за участю аніонних каналів LRRC8 [15–19, 21, 22].
Порушення механізмів піроапоптозу та індукція NETs відіграють важливу роль у прогресуванні подагри. NETs сприяють активації інфламасоми NLRP3 та поляризації макрофагів. І піроапоптоз, і індукція NETs пов’язані із секрецією цитокінів, що підтримують запальний каскад, характерний для подагри [23, 24].
Дисбіоз кишкової мікробіоти
Все більше доказів свідчать про те, що зміни в мікробіоті кишечнику, які включають бактерії, гриби, віруси та археї, можуть впливати на виникнення та прогресування подагри [25]. В одному дослідженні подагри, остеоартриту та здорових контрольних груп виявлено, що вірусне співтовариство кишечнику у пацієнтів із подагрою мало характерні зміни у різноманітності та таксономії, що дає нове розуміння етіології захворювання, потенційного лікування та стратегій профілактики [26]. Інше дослідження показало, що мікробіота кишечнику у пацієнтів із подагрою має знижене багатство та різноманітність порівняно зі здоровими донорами та впливає на патогенез подагри, зокрема на метаболізм пуринів, екскрецію уратів та активацію інфламасоми NLRP3 [26, 27].
Шляхом аналізу РНК-секвенування мікробіому та метаболоміки Лю та співавтори ідентифікували 11 мікробних таксонів, які суттєво впливали на патогенез подагри, змінюючи регуляцію імунної системи та метаболізм хазяїна. У цьому дослідженні Bacteroides faecis відігравали захисну роль, регулюючи прозапальні моноцити CD16+ [28]. Нещодавні дослідження вказують на зв’язок між гіперурикемією (спричиненою зниженням ниркової екскреції сечової кислоти та недостатньою кишковою екскрецією сечової кислоти) та дисбіозом кишечнику [29]. Кишкова флора регулює метаболізм сечової кислоти переважно через анаеробний катаболізм пуринів грамнегативними бактеріями, такими як Alistipes indistinctus, рівень яких виявився виснаженим у суб’єктів із гіперурикемією. Використовуючи комплексний метагеномний та метаболомічний аналіз, китайське дослідження [29] повідомило, що Alistipes indistinctus може посилювати екскрецію уратів та полегшувати гіперурикемію шляхом регулювання рівнів гіпурової кислоти. Це підвищує транскрипцію підродини G члена 2 АТФ-зв’язувальної когорти (ABCG2) та сприяє її локалізації в щітковій облямівці мембрани ентероцитів.
У світлі цих знахідок деякі пілотні дослідження вивчали використання пробіотиків для покращення метаболізму сечової кислоти та зменшення запалення суглобів. Це може запропонувати багатообіцяючу допоміжну терапевтичну стратегію для ведення гіперурикемії та подагри [33]. У кількох моделях гіперурикемії та/або подагри на щурах [30–32] відновлення здорової мікробіоти кишечнику шляхом введення пробіотиків (наприклад Priestia megaterium ASC-1, Terminalia chebula, відвар Guizhi Shaoyao Zhimu) дозволило знизити рівень сечової кислоти та запальну відповідь, а також у деяких випадках покращити метаболічний профіль [30–32]. Нещодавні дослідження на моделях гусей, проведені Y. Fu, Kim D. та іншими, підкреслили ефективність пробіотиків Lactobacillus та S. thermophilus IDCC 2201 у запобіганні гіперурикемії шляхом прямої деградації сечової кислоти або нуклеозидів [33, 34].
Що стосується клінічних досліджень, то поєднане введення Lactobacillus paracasei GY-1 та колхіцину пацієнтам із нападами подагри було ефективним у зниженні кишкової токсичності колхіцину. Окрім відновлення балансу кишкової мікробіоти, Lactobacillus paracasei GY-1 посилив терапевтичний ефект колхіцину шляхом зниження рівнів прозапальних цитокінів (ІЛ-1β, фактор некрозу пухлин (ФНП)-α) та підвищення рівня протизапального цитокіну ІЛ-10 [35].
1. Дисбіоз кишечнику може викликати або посилювати подагру, впливаючи на метаболізм пуринів, екскрецію уратів та запалення. Навпаки, нещодавні дані свідчать про те, що відновлення здорової мікробіоти може полегшити гіперурикемію [29].
2. На основі численних досліджень на тваринах використання пробіотиків може стати додатковим варіантом лікування на додаток до традиційної фармакологічної терапії [30–32].
3. У людей пробіотики здатні посилювати клінічну та біогуморальну відповідь на колхіцин і зменшувати його шлунково-кишкові побічні ефекти [35].
Як традиційне лікування подагри може модифікувати результати коморбідних станів
Подагра традиційно асоціюється з ожирінням [36], кардіометаболічними коморбідностями та вищими показниками загальної та серцево-судинної смертності [37]. Існують докази, які свідчать про те, що після нападу подагри зростає ризик серйозних серцево-судинних подій, включаючи смерть [37, 38], особливо у жінок та осіб молодшого віку [37]. Більше того, подагра може підвищувати ризик термінальної стадії ниркової недостатності навіть у пацієнтів без попередньої хронічної хвороби нирок (ХХН), як продемонстровано у великому загальнонаціональному дослідженні в Південній Кореї [38].
Нещодавні дослідження підкреслили важливість скринінгу пацієнтів із подагрою на кардіометаболічні коморбідності [39], включаючи, наприклад, комплексний аналіз глікемічного та ліпідного профілів [40], УЗД сонних артерій [41] та/або оцінку еластичності печінки [42]. Хоча останнім часом опублікована значна кількість досліджень щодо ведення подагри, основою лікування залишається купірування гострої фази та подальше зниження рівня уратів у сироватці крові за допомогою уратзнижувальної терапії (УЗТ) [43]. Незважаючи на наявність ефективних методів лікування, подагра залишається захворюванням, яке лікується незадовільно [43]. Дійсно, основну причину слід шукати в занепокоєнні щодо безпеки через лікарську взаємодію та побічні ефекти, і лише рідко — в неефективності [43]. Тому існує постійна потреба в нових препаратах, здатних обійти ці проблеми безпеки.
При загостреннях подагри наріжним каменем лікування є нестероїдні протизапальні препарати (НПЗП), колхіцин та глюкокортикоїди. Біологічне лікування, таке як блокатори анти-IЛ-1, резервується для особливо резистентних пацієнтів та осіб з непереносимістю [43], а також для пацієнтів із персистуючою активністю запального процесу із утворенням тофусів.
Після гострої фази рекомендується профілактика колхіцином при введенні УЗТ або зміні її дози для зниження ризику нападу подагри. Дійсно, нещодавно колхіцин продемонстрував протизапальні механізми [44], окрім дестабілізації мікротрубочок у нейтрофілах. Він здатний тонко регулювати активацію тромбоцитів, адгезію макрофагів, ендотеліальну експресію, а також збірку та активацію NLRP3 [44]. З цієї причини колхіцин був успішно протестований та застосований у первинній та вторинній серцево-судинній профілактиці, підтверджуючи свою переносимість у пацієнтів із множинними коморбідностями [45, 46].
Наприклад, дослідження низьких доз колхіцину (дослідження LoDoCo2), у якому взяли участь 5522 пацієнти з хронічною ішемічною хворобою серця, довело відмінну безпеку та продемонструвало значне зниження частоти спонтанного інфаркту міокарда, ішемічної реваскуляризації коронарних артерій та смертей від серцево-судинних захворювань через 2,4 року [46]. Це та подібні дослідження сприяли нещодавньому включенню колхіцину до невеликої кількості ліків, схвалених Управлінням з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration — FDA) для серцево-судинної профілактики [45].
Як зазначено вище, довгострокове лікування подагри покладається на УЗТ, включаючи інгібітори ксантиноксидази (ІКО) — алопуринол та фебуксостат — урикозурики та уриказу. Оскільки підвищений кардіометаболічний ризик, ймовірно, пов’язаний зі специфічними патологічними механізмами гіперурикемії [47], очікується зміна показників коморбідності та ускладнень у пацієнтів, які отримують УЗТ. Однак дискусія з цього приводу триває. Метааналіз рандомізованих контрольованих досліджень (РКВ) [48] показав, що УЗТ не знижує серцево-судинного ризику, тоді як більш сучасні обсерваційні дослідження в умовах реальної практики свідчать про те, що УЗТ може чинити сприятливий вплив на коморбідні стани [36] та рівень смертності. Загальнонаціональне китайське дослідження, проведене серед пацієнтів із цукровим діабетом 2-го типу, які отримували лікування з приводу безсимптомної гіперурикемії, виявило, що УЗТ знижує загальну та серцево-судинну смертність [49].
Інше менше за масштабом дослідження припустило, що інгібітори ксантиноксидоредуктази (КОР), включаючи алопуринол та фебуксостат, можуть виявляти захисний ефект щодо секреторної здатності інсуліну у людей [50], підтверджуючи попередні результати на експериментальних тваринах. Дійсно, відомо, що інгібітори ксантиноксидази пом’якшують оксидативний стрес і стабілізують функцію мітохондрій. Тож активність плазмової КОР була запропонована як біомаркер метаболічних розладів [51]. Ці плейотропні ефекти УЗТ можуть виявлятися і при ХХН [52]. Фактично метааналіз впливу УЗТ на ХХН показав, що алопуринол асоціюється з покращенням швидкості клубочкової фільтрації (ШКФ), але без значущого співвідношення доза-відповідь і з дуже мінливим ефектом у різних дослідженнях та серед пацієнтів у межах одного дослідження [53]. Відсутність прямої пропорційності можна пояснити або гетерогенністю популяції, або наявністю інших нефропротекторних ефектів, окрім зниження рівня уратів у сироватці крові.
Зв’язок між гіперурикемією та лікуванням кардіометаболічних захворювань можна вважати двоспрямованим. Зокрема, дослідження менделівської рандомізації показало, що цукрознижувальний ефект метформіну асоційований зі зниженим ризиком гіперурикемії — але не подагри — і цей зв’язок суттєво залежав від індексу маси тіла (ІМТ) [54]. Інгібітори натрій-глюкозного котранспортера 2-го типу (іНГТ2) — це клас препаратів, схвалених для лікування цукрового діабету 2-го типу та хронічної серцевої недостатності з визначними перевагами щодо прогресування ХХН та ризику смертності. До цього класу належать, зокрема, дапагліфлозин і емпагліфлозин. У post hoc-аналізі рандомізованих контрольованих досліджень емпагліфлозин [47, 55] був пов’язаний з нижчим рівнем уратів у сироватці крові та зниженням частоти наслідків, пов’язаних із подагрою, тоді як дапагліфлозин затримував початок нового лікування гіперурикемії та подагри (тобто УЗТ та колхіцину) [56]. Цікаво, що терапевтична користь емпагліфлозину значно посилювалася за рахунок зниження рівня уратів у сироватці крові, що означає, що модифікація рівня уратів сприяла видатній серцево-судинній користі. Крім того, популяційні дослідження в умовах реальної практики свідчать про те, що іНГТ2 можуть допомогти знизити рівень уратів у сироватці крові та частоту нападів подагри у пацієнтів із різними коморбідностями [57] (рисунок).
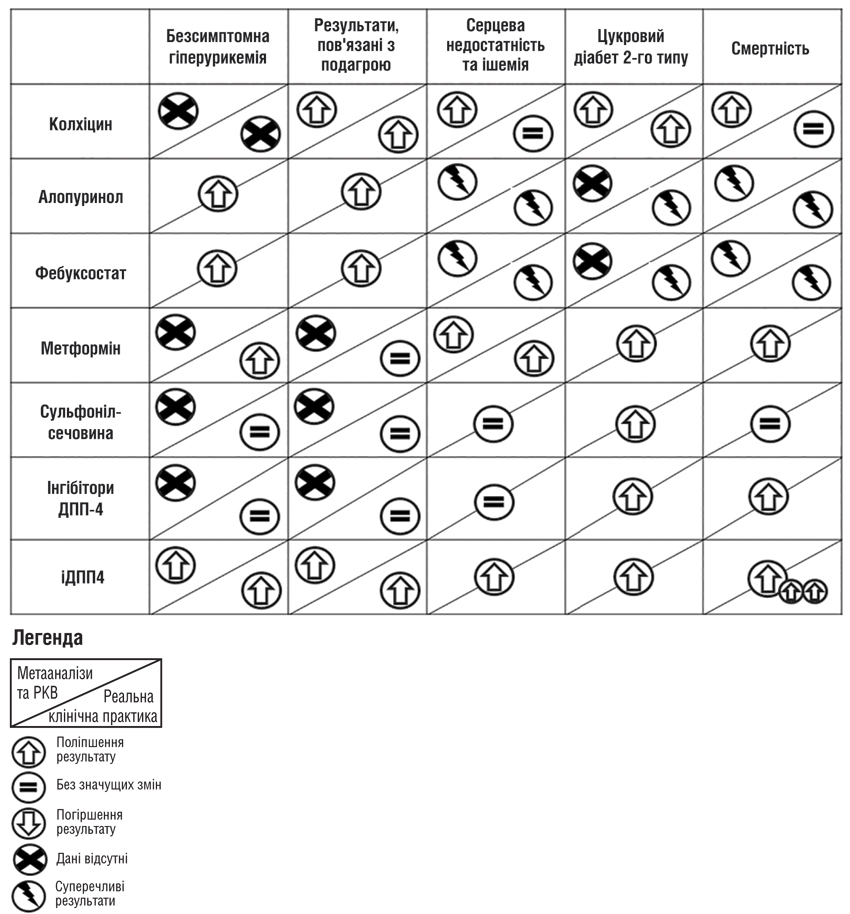
Рисунок. Зведені дані щодо наявних доказів ефективності терапії при гіперурикемії / подагрі, цукровому діабеті та серцево-судинних захворюваннях.
Інші протидіабетичні препарати, такі як сульфонілсечовина [58] та інгібітори дипептидилпептидази-4 (іДПП4) [59], не продемонстрували здатності знижувати рівень уратів у сироватці крові та ризик подагри. Таким чином, терапевтичний вибір у пацієнтів із подагрою має бути адаптований до кожного конкретного типу коморбідності (цукровий діабет 2-го типу, серцева недостатність та/або ХХН), враховуючи ризик розвитку гіперурикемії.
1. Хоча FDA нещодавно схвалено колхіцин для первинної та вторинної серцево-судинної профілактики [45], переваги алопуринолу та фебуксостату щодо серцево-судинних захворювань та смертності, контролю цукрового діабету 2-го типу та стабілізації ХХН також знаходяться у фокусі уваги [53].
2. Протидіабетичні препарати, включаючи метформін та інгібітори іНГТ2, довели свою ефективність у зниженні рівня уратів у сироватці крові та ризику наслідків, пов’язаних із подагрою [54, 55].
Терапевтичні новинки
Накопичені дані про патогенез подагри та біомолекулярну функцію її традиційного лікування вказують на інфламасому NLRP3 як на можливу терапевтичну мішень [15, 59]. Зокрема, нові малі молекули, що безпосередньо впливають на внутрішньоклітинну NLRP3, є біодоступними при пероральному прийомі та мають перевагу у здатності долати гематоенцефалічний бар’єр [59]. Хоча жоден із вищезазначених препаратів на сьогодні не схвалений, тривають розширені клінічні дослідження при подагрі та/або інших захворюваннях, зумовлених інфламасомою [59]. Серед них дослідження фази II/III дапансутрилу (OLT1177) показали хороші анальгезивні властивості без значних побічних ефектів [60].
Інновації були запропоновані також у сфері УЗТ (таблиця). Пеглотиказа — це комерційно доступний у ряді країн препарат для лікування тяжкої / рефрактерної подагри. За результатами дослідження MIRROR, FDA нещодавно схвалила поєднане введення пеглотикази з метотрексатом [61].
| Препарат та категорія | Механізм дії | Шлях введення | Фаза | Коментарі |
|---|---|---|---|---|
| Гостра подагра та профілактика | ||||
| SSGJ-613 | Моноклональне антитіло до ІЛ-1β | Підшкірний | I/II | Очікуються результати |
| Дапансутрил (Dapansutrile / OLT1177®) | Інгібітор інфламмасоми NLRP3 | Пероральний | II, III | Хороший анальгезивний ефект зі сприятливим профілем безпеки |
| Гіпоурикемічна терапія | ||||
| Дотинурад (Dotinurad) | Урикозуричний препарат (SURI) | Пероральний | III* | Поліпшення функції нирок при низькому ризику утворення ниркових каменів |
| Веринурад (Verinurad) | Урикозуричний препарат (SURI) | Пероральний | II/III | Підвищення рівня креатиніну при монотерапії; слід застосовувати в комбінації з інгібіторами ксантиноксидази |
| AR-882 | Урикозуричний препарат (SURI) | Пероральний | III | Ефективний без значущих небажаних явищ |
| Епамінурад (Epaminurad) | Урикозуричний препарат (SURI) | Пероральний | III | Очікуються результати |
| Рузинурад (Ruzinurad) | Урикозуричний препарат (SURI) | Пероральний | III | Ефективність як гіпоурикемічного засобу, іноді викликає напади подагри |
| Архалофенат (Arhalofenate) | Неселективний урикозуричний інгібітор URAT1 | Пероральний | II | Препарат подвійної дії. Перший засіб, що діє і як гіпоурикемічний, і як протизапальний. Помірна активність в обох напрямках |
| Тигуліксостат (Tigulixostat) | Непуриновий інгібітор ксантиноксидази | Пероральний | III | Висока гіпоурикемічна активність у низьких дозах. Незначне підвищення рівня креатинфосфокінази |
| ALL-346 | Генно-інженерна кишкова уриказа | Пероральний | II | Завдяки кишковому механізму дії підходить для застосування при ХХН |
| SEL-212 | Пегільована уриказа + SVP-R | Внутрішньовенний (раз на місяць) | III | Знижений ризик імуногенності порівняно з пеглотиказою |
Існує помітна розбіжність між країнами щодо дозволу на застосування урикозуричних препаратів. США рекомендують обережне застосування пробенециду та бензбромарону через ризик утворення каменів у нирках та гепатотоксичність відповідно. Кілька препаратів додатково досліджувалися останніми роками через проблеми з безпекою та можливі відкликання [61]. Новий селективний інгібітор резорбції сечової кислоти, дотинурад, схвалений у Японії у 2020 р., а в інших країнах тривають дослідження фази III. На сьогодні він продемонстрував обнадійливі результати щодо покращення функції нирок та зниження ризику утворення каменів [61]. Завдяки механізму дії — селективному інгібуванню транспортера уратів 1 (УРАT1) у проксимальних канальцях нирок — його застосування було запропоновано при метаболічному синдромі, ХХН та серцево-судинних захворюваннях. Результати випробувань фази II веринураду — ще одного інгібітора УРАТ1 — опубліковані, вони продемонстрували, що він може значно знижувати рівень уратів у сироватці крові у пацієнтів із подагрою; він також досліджувався при ХХН щодо його потенційних нефропротекторних ефектів. Однак веринурад не досяг своєї первинної кінцевої точки у дослідженні щодо зниження мікроальбумінурії та стабілізації ШКФ у пацієнтів із ХХН [60]. Архалофенат спочатку розроблявся як сенсибілізатор інсуліну при цукровому діабеті 2-го типу, що інгібує як реабсорбцію уратів, так і запалення, пов’язане з подагрою. Фактично він селективно інгібує як УРАТ1, так і OAT4 у проксимальних канальцях нирок, а також втручається у шлях PPARγ, знижуючи вивільнення IЛ-1β, IЛ-6 та активацію інфламасоми. Таким чином, архалофенат є першим препаратом, здатним знижувати не лише рівень уратів у сироватці крові, але й ризик нападу подагри [60]. Серед інших цікавих препаратів — ІКО тігуліксостат, уриказа SEL-212 (пегільована) та ALLN-346 [61] (таблиця).
1. Інгібітори NLRP3 — це пероральні малі молекули, що діють на цитоплазматичну інфламасому, які продемонстрували перспективні анальгезивні властивості [60].
2. Пеглотиказа — уриказа, схвалена на цей час для лікування рефрактерної та тяжкої подагри, має вводитися разом із метотрексатом для запобігання серйозним побічним ефектам [61].
13. Дослідження урикозуриків є дуже активними і зосереджені на селективних інгібіторах ниркової резорбції сечової кислоти. Серед досліджуваних препаратів дотинурад схвалений у Японії, і його застосування запропоновано при ХХН, серцево-судинних та метаболічних захворюваннях [62].
На завершення варто зазначити, що 2025 р. став знаковим у розумінні подагри як системного захворювання, де патогенетичні механізми тісно переплітаються з функцією нирок, станом серцево-судинної системи та метаболізмом мікробіоти. Інтеграція нових терапевтичних стратегій, таких як інгібітори NLRP3-інфламасоми та селективні урикозурики нового покоління, разом із персоніфікованим підходом до коморбідних пацієнтів, відкриває реальні перспективи не лише для ефективного контролю рівня сечової кислоти, а й для суттєвого зниження глобального тягаря асоційованих хвороб.
Список використаної літератури
- 1. Cross M., Ong K.L., Culbreth G.T. et al. (2024) Global, regional, and national burden of gout, 1990–2020, and projections to 2050: a systematic analysis of the Global Burden of Disease Study 2021. Lancet Rheumatol.; 6(8): e507–e517.
- 2. Li Y., Chen Z., Xu B. et al. (2024) Global, regional, and national burden of gout in elderly 1990–2021: an analysis for the global burden of disease study 2021. BMC Public Health; 24(1): 3298.
- 3. Lorenzin M., Ughi N., Ariani A. et al. (2022) Impact of disease duration and gender on the sensitivity and specificity of 2015 ACR/EULAR classification criteria for gout. Clin. Exp. Rheumatol.; 40(7): 1368–77.
- 4. Jatuworapruk K. (2024) Gout prevalence is rising in low-income and middle-income countries: are we ready? Lancet Rheumatol.; 6(8): e494–e495.
- 5. Punjwani S., Jani C., Liu W. et al. (2024) Burden of gout among different WHO regions, 1990–2019: estimates from the global burden of disease study. Sci. Rep.; 14(1): 15953.
- 6. Mandl P., D’Agostino M.A., Navarro-Compán V. et al. (2024) 2023 EULAR recommendations on imaging in diagnosis and management of crystal-induced arthropathies in clinical practice. Ann. Rheum. Dis.; 83(6): 752–59.
- 7. Fukuda T., Subramanian M., Noda K. et al. (2024) The comprehensive role of dual-energy CT in gout as an advanced diagnostic innovation. Skeletal. Radiol.; Dec 17.
- 8. Zhao Q., Xiong Y., Man X. et al. (2023): Serum soluble E-cadherin is a new potential marker for assessing the severity of gout. Clin. Exp. Rheumatol.; 41(5): 1170–78.
- 9. Cho C., Kim B., Kim D.S. et al. (2024): Large-scale cross-ancestry genome-wide meta-analysis of serum urate. Nat. Commun.; 15(1): 3441.
- 10. Ji A., Sui Y., Xue X. et al. (2025) Novel genetic loci in early-onset gout derived from whole-genome sequencing of an adolescent gout cohort. Arthritis Rheumatol.; 77(1): 107–15.
- 11. Shi K., Guo Y., You T. (2025) Global burden of gout in age groups 10 to 54 years from 1990 to 2021: Trend of the global burden of disease study. Medicine (Baltimore); 104(48): e46231.
- 12. Major T.J., Takei R., Matsuo H. et al. (2024): A genome-wide association analysis reveals new pathogenic pathways in gout. Nat Genet; 56(11): 2392-406.
- 13. Wang X., Yang B., Xiong T. et al. (2024) Identification of potential biomarkers of gout through weighted gene correlation network analysis. Front. Immunol.; 15: 1367019.
- 14. Zeng W., Hu M., Zhou L. et al. (2024): Exploring genetic links between blood metabolites and gout susceptibility. Clin Rheumatol; 43(12): 3901-12.
- 15. Tian Y., He X., Li R. et al. (2024) Recent advances in the treatment of gout with NLRP3 inflammasome inhibitors. Bioorg. Med. Chem.; 112: 117874.
- 16. Martinon F., Pétrilli V., Mayor A. et al. (2006) Gout-associated uric acid crystals activate the NALP3 inflammasome. Nature; 440(7081): 237–41.
- 17. Lee K.G., Hong B.K., Lee S. et al. (2024) Nuclear receptor coactivator 6 is a critical regulator of NLRP3 inflammasome activation and gouty arthritis. Cell Mol. Immunol.; 21(3): 227–44.
- 18. Alabarse P.G., Oliveira P., Qin H. et al. (2024) The NADase CD38 is a central regulator in gouty inflammation and a novel druggable therapeutic target. Inflamm. Res.; 73(5): 739–51.
- 19. Luo C., Liu X., Liu Y. et al. (2024) Upregulation of CD39 during gout attacks promotes spontaneous remission of acute gouty inflammation. Inflammation; 47(2): 664–77.
- 20. Song D., Zhou X., Yu Q. et al. (2024) ML335 inhibits TWIK2 channel-mediated potassium efflux and attenuates mitochondrial damage in MSU crystal-induced inflammation. J. Transl. Med.; 22(1): 785.
- 21. Ehirchiou D., Bernabei I., Pandian V.D. et al. (2024) The integrin CD11b inhibits MSU-induced NLRP3 inflammasome activation in macrophages and protects mice against MSU-induced joint inflammation. Arthritis Res. Ther.; 26(1): 119.
- 22. Chirayath T.W., Ollivier M., Kayatekin M. et al. (2024) Activation of osmo-sensitive LRRC8 anion channels in macrophages is important for micro-crystallin joint inflammation. Nat. Commun.; 15(1): 8179.
- 23. Chen T., Zhou J., Dang W. (2024) Mechanism of neutrophil extracellular traps in the pathogenesis of gout. Clin. Exp. Rheumatol.; 42(11): 2272–79.
- 24. Chen C., Wang J., Guo Y. et al. (2024): Monosodium urate crystal-induced pyroptotic cell death in neutrophil and macrophage facilitates the pathological progress of gout. Small; 20(23): 2308749.
- 25. Tang C., Li L., Jin X. et al. (2024) Investigating the impact of gut microbiota on gout through mendelian randomization. Orthop. Res. Rev.; 16: 125–36.
- 26. Chen C.M., Yan Q.L., Guo R.C. et al. (2024) Distinct characteristics of the gut virome in patients with osteoarthritis and gouty arthritis. J. Transl. Med.; 22(1): 564.
- 27. Lou Y., Liu B., Jiang Z. et al. (2024) Assessing the causal relationships of gut microbial genera with hyperuricemia and gout using two-sample Mendelian randomization. Nutr. Metab. Cardiovasc. Dis.; 34(4): 1028–35.
- 28. Liu X., Feng Z., Zhang F. et al. (2024) Causal effects of gut microbiota on gout and hyperuricemia: insights from genome-wide Mendelian randomization, RNA-sequencing, 16S rRNA sequencing, and metabolomes. Biosci. Rep.; 44(11).
- 29. Xu Y.X., Liu L.D., Zhu J.Y. et al. (2024) Alistipes indistinctus-derived hippuric acid promotes intestinal urate excretion to alleviate hyperuricemia. Cell Host Microbe; 32(3): 366–81.
- 30. Zhu W., Bi S., Fang Z. et al. (2024) Priestia megaterium ASC-1 isolated from pickled cabbage ameliorates hyperuricemia by degrading uric acid in rats. Microorganisms; 12(4): 832.
- 31. Liu W., Zhang M., Tan J. et al. (2024) Integrated data mining and animal experiments to investigate the efficacy and potential pharmacological mechanism of a traditional tibetan functional food Terminalia chebula retz. in hyperuricemia. J. Inflamm. Res.; 17: 11111–28.
- 32. Bian M., Zhu C., Nie A. et al. (2024) Guizhi Shaoyao Zhimu Decoction ameliorates gouty arthritis in rats via altering gut microbiota and improving metabolic profile. Phytomedicine; 131: 155800.
- 33. Fu Y., Chen Y.S., Xia D.Y. et al. (2024) Lactobacillus rhamnosus GG ameliorates hyperuricemia in a novel model. Npj. Biofilms Microbiomes; 10(1): 25.
- 34. Kim D., Moon J.S., Kim J.E. et al. (2024) Evaluation of purine-nucleoside degrading ability and in vivo uric acid lowering of Streptococcus thermophilus IDCC 2201, a novel antiuricemia strain. PLoS One; 19(2): e0293378.
- 35. Zeng J., Li Y., Zou Y. et al. (2024) Intestinal toxicity alleviation and efficacy potentiation through therapeutic administration of Lactobacillus paracasei GY-1 in the treatment of gout flares with colchicine. Food Funct.; 15(3): 1671–88.
- 36. Cai N., Chen M., Feng P. et al. (2024) Relationships between obesity and prevalence of gout in patients with type 2 diabetes mellitus: a cross-sectional population-based study. BMC Endocr. Disord.; 24(1): 137.
- 37. Ferguson L.D., Molenberghs G., Verbeke G. et al. (2024) Gout and incidence of 12 cardiovascular diseases: a case–control study including 152 663 individuals with gout and 709 981 matched controls. Lancet Rheumatol.; 6(3): e156–e167.
- 38. Jung I., Lee D.Y., Chung S.M. et al. (2024) Impact of chronic kidney disease and gout on end-stage renal disease in type 2 diabetes: population-based cohort study. Endocrinol. Metab.; 39(5): 748–57.
- 39. Vedder D., Heslinga M., Wijbrandts C.A. et al. (2023) Cardiovascular risk management in gout patients: do patients benefit from screening in secondary care? Clin. Exp. Rheumatol.; 41(9): 1762–67.
- 40. Si K., Wei C., Xu L. et al. (2023) Association between serum free fatty acid levels and tophus in patients with gout: a cross-sectional study. Clin. Exp. Rheumatol.; 41(3): 711–17.
- 41. Dang W., Hu J., Luo H. et al. (2023) The prevalence and independent risk factors of elevated common carotid artery intima-media thickness and carotid plaque in patients with gout. Clin. Exp. Rheumatol.; May 12.
- 42. Schlesinger N., Patel A., Rustgi V.K. et al. (2024) Increased frequency of hepatic steatosis and fibrosis in patients with gout detected by transient elastography. Clin. Exp. Rheumatol.; 42(1): 86–91.
- 43. Punzi L., Galozzi P., Luisetto R. et al. (2024) Gout: one year in review 2023. Clin. Exp. Rheumatol.; 42(1): 1–9.
- 44. Bulhões F.V. De, Assis G.E., Caze A.B. et al. (2024) The action of colchicine in patients with metabolic syndrome and obesity: perspectives and challenges. Metabolites; 14(11): 629.
- 45. AGEPHA Pharma USA, LLC (2023) U.S. FDA Approves First Anti-Inflammatory Drug for Cardiovascular Disease. us.agephapharma.com/blog/2023/06/20/us-fda-approves-first-anti-inflammatory-drug-for-cardiovascular-disease.
- 46. Bayram Y.E., Bardakci M.I., Albayrak G.A. (2024) Improved kidney function is associated with Colchicine treatment in COVID-19 patients. BMC Nephrol.; 25(1): 405.
- 47. Doehner W., Anker S.D., Butler J. et al. (2022) Uric acid and sodium-glucose cotransporter-2 inhibition with empagliflozin in heart failure with reduced ejection fraction: the EMPEROR-reduced trial. Eur. Heart J.; 43(36): 3435–46.
- 48. Xu H., Liu Y., Meng L. et al. (2021) Effect of uric acid-lowering agents on patients with heart failure: a systematic review and meta-analysis of randomised controlled trials. Front. Cardiovasc. Med.; 8: 639392.
- 49. Chen R., Nie S., Zhou S. et al. (2024) Association between urate-lowering therapy initiation and all-cause mortality in patients with type 2 diabetes and asymptomatic hyperuricemia. Diabetes Metab. Syndr.Clin. Res. Rev.; 18(6): 103043.
- 50. Kitamura A., Kurajoh M., Miki Y. et al. (2024) Association of xanthine oxidoreductase inhibitor use with insulin secretory capacity in patients with type 2 diabetes. J. Diabetes Investig.; 15(10): 1500–9.
- 51. Furuhashi M., Matsumoto M., Tanaka M. et al. (2018) Plasma xanthine oxidoreductase activity as a novel biomarker of metabolic disorders in a general population. Circ. J.; 82(7): 1892–99.
- 52. Sharbaf F.G., Bakhtiari E., Faghihi T. et al. (2024) Efficacy and safety of allopurinol on chronic kidney disease progression: a systematic review and meta-analysis. J. Pediatr. Pharmacol. Ther.; 29(4): 359–67.
- 53. Casanova A.G., Morales A.I., Vicente-Vicente L. et al. (2024) Effect of uric acid reduction on chronic kidney disease. Systematic review and meta-analysis. Front Pharmacol.; 15: 1373258.
- 54. Dai H., Hou T., Wang Q. et al. (2024) The effect of metformin on urate metabolism: findings from observational and Mendelian randomization analyses. Diabetes Obes. Metab.; 26(1): 242–50.
- 55. Tesfaye H., Wang K.M., Zabotka L.E. et al. (2024) Empagliflozin and risk of incident gout: analysis from the EMPagliflozin Comparative Effectiveness and SafEty (EMPRISE) cohort study. J. Gen. Intern. Med.; 39(10): 1870–79.
- 56. Butt J.H., Docherty K.F., Claggett B.L. et al. (2023) Association of dapagliflozin use with clinical outcomes and the introduction of uric acid–lowering therapy and colchicine in patients with heart failure with and without gout: a patient-level pooled meta-analysis of DAPA-HF and DELIVER. JAMA Cardiol.; 8(4): 386.
- 57. Mccormick N., Yokose C., Lu N. et al. (2024) Sodium-glucose cotransporter-2 inhibitors vs sulfonylureas for gout prevention among patients with type 2 diabetes receiving metformin. JAMA Intern. Med.; 184(6): 650.
- 58. Brønden A., Christensen M.B., Glintborg D. et al. (2023) Effects of DPP-4 inhibitors, GLP-1 receptor agonists, SGLT-2 inhibitors and sulphonylureas on mortality, cardiovascular and renal outcomes in type 2 diabetes: A network meta-analyses-driven approach. Diabet Med.; 40(8): e15157.
- 59. Coll R.C., Schroder K. (2025) Inflammasome components as new therapeutic targets in inflammatory disease. Nat. Rev. Immunol.; 25(1): 22–41.
- 60. Klück V., Jansen T.L.T.A., Janssen M. et al. (2020) Dapansutrile, an oral selective NLRP3 inflammasome inhibitor, for treatment of gout flares: an open-label, dose-adaptive, proof-of-concept, phase 2a trial. Lancet Rheumatol.; 2(5): e270–e280.
- 61. Kaufmann D., Chaiyakunapruk N., Schlesinger N. (2024) Optimizing gout treatment: A comprehensive review of current and emerging uricosurics. Joint Bone Spine; 92(2): 105826.
- 62. Heerspink H.J.L., Stack A.G., Terkeltaub R. et al. (2024) Combination treatment with verinurad and allopurinol in CKD: a randomized placebo and active controlled trial. J. Am. Soc. Nephrol. JASN; 35(5): 594–606.

Leave a comment