Сучасні підходи до профілактики та лікування глюкокортикоїд-індукованого остеопорозу
Проценко Г.О.1, Афанасьєва І.О.2, Неміш І.Л.3
- 1ДУ «ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска НАМН України»
- 2Національний медичний університет імені О.О. Богомольця
- 3Буковинський державний медичний університет
Резюме. Глюкокортикоїд (ГК)-індукований остеопороз — одне з найпоширеніших ускладнень тривалої терапії ГК, що супроводжується зниженням мінеральної щільності кісткової тканини та високим ризиком патологічних переломів. На основі аналізу сучасних клінічних рекомендацій з урахуванням стану проблеми в Україні та даних клінічної фармакології пропонуємо практичний підхід, який може стати у нагоді лікарям у профілактиці та лікуванні ГК-індукованого остеопорозу. Запропонована стратегія включає оптимізацію дози ГК з підтриманням мінімально ефективного рівня терапії, модифікацію способу життя (регулярна фізична активність, відмова від куріння та надмірного вживання алкоголю), нутритивну підтримку, а також фармакотерапію, підібрану відповідно до рівня ризику переломів. Важливим елементом стратегії є вживання комбінованих засобів, таких як Остеоцитрат та Остеоцитрат МАКС, які містять кальцій, магній, цинк у формі цитрату, вітамін D3 та вітамін K2. Кальцій цитрат відрізняється найвищою біодоступністю серед кальцієвих солей, добре всмоктується незалежно від прийому їжі та кислотності шлункового соку. Вітамін D3 у складі препарату сприяє оптимальному засвоєнню кальцію, а вітамін K2 забезпечує його ефективне включення у кісткову тканину, запобігаючи відкладанню в судинах. Магній підтримує структуру кісток та нервово-м’язову функцію, а цинк стимулює формування та мінералізацію кісткової тканини. Завдяки синергічній дії компонентів засіб сприяє підвищенню міцності кісток та профілактиці остеопоротичних переломів, водночас не підвищуючи ризику утворення ниркових каменів та відкладення кальцію в судинних стінках. Таким чином, вживання засобів Остеоцитрат або Остеоцитрат МАКС у поєднанні з корекцією способу життя та сучасною фармакотерапією є найбільш ефективною стратегією зниження ризику остеопоротичних переломів у пацієнтів, які тривало отримують ГК.
DOI: 10.32471/rheumatology.2707-6970.20102
 Синтетичні глюкокортикоїди (ГК) широко застосовуються у лікуванні різноманітних захворювань. Це зумовлено їхніми потужними протизапальними та імуносупресивними властивостями, що сприяють ефективному контролю симптомів хвороб [1, 2]. Водночас попри свою терапевтичну дію, ГК можуть незалежно від шляху їх введення (перорально, надшкірно, інгаляційно, інтраназально, інтраокулярно, внутрішньосуглобово) можуть викликати системні ефекти (вплив на кістково-м’язову, серцево-судинну, ендокринну, гастроінтестинальну системи, орган зору та ін.), особливо при високих або повторних дозах. Проте навіть тривале призначення низьких доз ГК може призвести до серйозних побічних ефектів — від помірних (наприклад збільшення маси тіла, підвищення артеріального тиску, підвищення рівня глюкози у крові, катаракта, глаукома, міопатія) до інвалідизуючих станів (остеопороз із переломами,тяжкі інфекції) і загрозливих для життя ускладнень [1–3]. Зокрема, одним із поширених ускладнень є ГК-індукований остеопороз, який відмічається у 0,7–1,2% дорослого населення [4, 5]. До факторів ризику розвитку цього захворювання належать похилий вік, менопаузальний період у жінок, висока доза та тривалість терапії ГК, низька мінеральна щільність кісткової тканини (МЩКТ) поперекового відділу хребта, наявність переломів в анамнезі, а також супутніх захворювань [1].
Синтетичні глюкокортикоїди (ГК) широко застосовуються у лікуванні різноманітних захворювань. Це зумовлено їхніми потужними протизапальними та імуносупресивними властивостями, що сприяють ефективному контролю симптомів хвороб [1, 2]. Водночас попри свою терапевтичну дію, ГК можуть незалежно від шляху їх введення (перорально, надшкірно, інгаляційно, інтраназально, інтраокулярно, внутрішньосуглобово) можуть викликати системні ефекти (вплив на кістково-м’язову, серцево-судинну, ендокринну, гастроінтестинальну системи, орган зору та ін.), особливо при високих або повторних дозах. Проте навіть тривале призначення низьких доз ГК може призвести до серйозних побічних ефектів — від помірних (наприклад збільшення маси тіла, підвищення артеріального тиску, підвищення рівня глюкози у крові, катаракта, глаукома, міопатія) до інвалідизуючих станів (остеопороз із переломами,тяжкі інфекції) і загрозливих для життя ускладнень [1–3]. Зокрема, одним із поширених ускладнень є ГК-індукований остеопороз, який відмічається у 0,7–1,2% дорослого населення [4, 5]. До факторів ризику розвитку цього захворювання належать похилий вік, менопаузальний період у жінок, висока доза та тривалість терапії ГК, низька мінеральна щільність кісткової тканини (МЩКТ) поперекового відділу хребта, наявність переломів в анамнезі, а також супутніх захворювань [1].
Патогенез ГК-індукованого остеопорозу
Патогенез ГК-індукованого остеопорозу включає як прямі ефекти ГК на клітини кісткової тканини, так і непрямий системний вплив. Прямий вплив ГК пов’язаний з активацією гамма-рецептора-2, активованого пероксисомними проліфераторами (PPARγ2) та пригніченням сигнального шляху Wnt/β-катеніну. Перший механізм зумовлює диференціацію мезенхімальних клітин у адипоцити замість остеобластів, зменшує кількість остеобластів і посилює апоптоз остеобластів і остеоцитів. Другий механізм пов’язаний з підвищенням рівня склеростину, який блокує Wnt-сигналінг, що додатково гальмує остеобластогенез. Доведено, що відсутність склеростину у тварин зберігає цілісність кісткової тканини навіть на тлі надлишку ГК. ГК також підвищують резорбцію кістки, стимулюючи продукцію макрофагального колонієстимулювального фактора (M-CSF) та рецептор-активатора ядерного фактора κB ліганду (RANKL) і знижуючи рівень остеопротегерину, що веде до збільшення кількості та підвищення активності остеокластів. З часом цей ефект знижується через втрату остеобластів та остеоцитів. Непрямі механізми включають розвиток гіпогонадизму, зниження фізичної активності, абсорбції кальцію в кишечнику та збільшення його втрати через нирки, а також зниження продукції інсуліноподібного фактора росту-1 (IGF-1) і білків, що його зв’язують. До цього додається вплив основного запального захворювання, при якому призначають ГК: запальні цитокіни самі по собі зумовлюють резорбцію, і при рецидивах захворювання, незважаючи на терапію, ризик втрати кістки зростає. Надлишок ГК також викликає міопатію, знижуючи м’язову силу і підвищуючи ризик падінь [6]. Унаслідок цього якість кісткової тканини стрімко погіршується, і вже протягом 3–6 міс після початку лікування можуть з’явитися остеопоротичні зміни. У 30–50% пацієнтів, які довготривало приймають ГК, можливі патологічні переломи, спричинені підвищеною крихкістю кісток [1].
Лікування пацієнтів з ГК-індукованим остеопорозом
Згідно із сучасними міжнародними рекомендаціями, ведення пацієнтів, які отримують ГК, має включати як своєчасну оцінку ризику переломів, так і корекцію факторів, пов’язаних з основним захворюванням. Європейські настанови 2024 р. наголошують, що попередню оцінку ризику переломів слід регулярно проводити у всіх пацієнтів, які, ймовірно, отримуватимуть пероральні ГК протягом 3 міс і більше. Такий підхід є обов’язковим для жінок і чоловіків віком від 50 років, а також для осіб із підвищеним ризиком — зокрема за наявності в анамнезі переломів крихких кісток чи супутніх захворювань і терапії, асоційованої з остеопорозом [7]. Водночас у рекомендаціях Японського товариства досліджень кісток та мінералів 2023 р. підкреслюється, що першочергове значення має ефективне лікування основного захворювання, яке зумовило необхідність призначення ГК, адже це безпосередньо впливає на прогноз і темпи втрати кісткової маси [1]. Так, перевагу варто надавати призначенню мінімально необхідної дози ГК, застосовуючи стероїдзберігаючі препарати, як-от метотрексат чи азатіоприн, або ж альтернативні шляхи введення ГК (наприклад інгаляційно чи місцево), якщо це доцільно. У підтримці ремісії, за можливості, варто надавати перевагу нестероїдним протизапальним препаратам (НПЗП). Водночас важливо зберігати контроль над основним захворюванням, адже ефективне пригнічення запального процесу дозволяє уникнути негативного впливу хронічного запалення на кісткову тканину, а також запобігти іншим ускладненням, зумовленим високою активністю хвороби [6]. Для максимальної ефективності лікування важливо змінити спосіб життя: займатися фізичними вправами, не курити, не зловживати алкоголем, а також подбати про достатнє надходження кальцію та вітаміну D — через їжу або спеціальні добавки [1].
Роль кальцію цитрату та супутніх мікронутрієнтів у профілактиці й лікуванні ГК-індукованого остеопорозу
Кальцій відіграє ключову роль у формуванні та мінералізації кісткової тканини, що є особливо важливим для підтримки здоров’я скелета. Проте для забезпечення підтримки кальцієвого балансу в організмі важливим є як його надходження з продуктами чи добавками, так і ефективне його всмоктування в шлунково-кишковому тракті. Цей процес визначається функціональним станом травної системи, характером кальцієвих сполук у раціоні, а також рівнем вітаміну D. Однак у людей віком старше 65 років і пацієнтів з остеопорозом здатність кишечнику до всмоктування кальцію знижена. Через це вони не можуть компенсувати його нестачу навіть за умов достатнього надходження з їжею. За відсутності ефективної абсорбції організм підтримує рівень кальцію в крові за рахунок вивільнення його з кісткової тканини. Такий механізм з часом спричиняє втрату кісткової маси та підвищує ризик розвитку остеопорозу. Дані літератури свідчать, що прийом препаратів кальцію тривало та регулярно у достатній дозі сповільнює темпи резорбції кісткової тканини та знижує ризик переломів остеопоротичних кісток. Проте серед численної кількості солей кальцію варто звернути увагу на кальцій цитрат, який найлегше засвоюється та має найвищу біодоступність порівняно з іншими формами кальцію (карбонатом, лактатом, глюконатом та трифосфатом). Попри те, засвоєння кальцію цитрату не залежить від часу прийому їжі та стану шлунково-кишкового тракту, що є важливим для людей похилого віку та з ахлоргідрією [8]. У дослідженні A.M. Kenny та співавторів (2004) встановлено, що застосування кальцію цитрату супроводжувалося зниженням маркерів резорбції кісток, таких як вільний дезоксипіридинолін — на 19%, N-телопептид у сечі — на 30%, С-телопептид — на 31%, N-телопептид у сироватці крові — на 8% порівняно з карбонатом кальцію у жінок у постменопаузальний період [9]. Дослідження H.J. Hell та співавторів (2001) показало, що кальцію цитрат має вищу біодоступність порівняно з карбонатом кальцію, забезпечуючи значно вищу пікову концентрацію кальцію в сироватці крові та в сечі, а також більш виражене зниження рівня паратиреоїдного гормону, що робить його кращим вибором для прийому під час їди [10]. Тобто застосування кальцію цитрату завдяки вищій біодоступності супроводжується більш вираженими антирезорбтивними властивостями, що характеризується зниженням маркерів резорбції кісток та паратгормону в крові. Окрім цього, кальцію цитрат відіграє захисну роль у профілактиці каменеутворення в нирках. Він не підвищує ризику утворення каменів, зменшує перенасичення сечі солями кальцію шляхом утворення розчинних комплексів з іонами кальцію, пригнічує ріст та агрегацію кристалів, а також знижує ризик каменеутворення завдяки залуженню сечі при екскреції цитрат-іонів [11].
Вітамін D доповнює цю дію, оскільки є ключовим фактором підтримання МЩКТ. Його хронічний дефіцит призводить до вторинного гіперпаратиреозу, посиленого кісткового обміну та прогресуючої втрати кісткової маси, що підвищує ризик переломів [12]. Доведено, що поєднаний прийом кальцію (особливо у формі цитрату) та вітаміну D підвищує МЩКТ та знижує частоту переломів [13]. Результати Кокранівського метааналізу показали, що у пацієнтів, які приймають ГК, така терапія є більш ефективною, ніж плацебо або лише кальцій, оскільки при її використанні відмічається уповільнення втрати кісткової маси у поперековому відділі хребта та передпліччі. Це пояснюється тим, що ГК переважно посилюють резорбцію трабекулярної кісткової тканини, яка становить основну частину цих ділянок, на відміну від шийки стегнової кістки, де домінує кортикальна кістка [14]. Враховуючи доведену ефективність, низьку вартість та безпеку у вітчизняних рекомендаціях зазначається, що дорослим, які приймають ГК, рекомендовано оптимальне загальне добове споживання кальцію 1000–1200 мг разом із вживанням добавок вітаміну D у дозі 800–1000 МО/добу та білка 1–1,2 г/кг/добу (рівень узгодженості 6,9; сила рекомендації А) (рис. 1) [15].
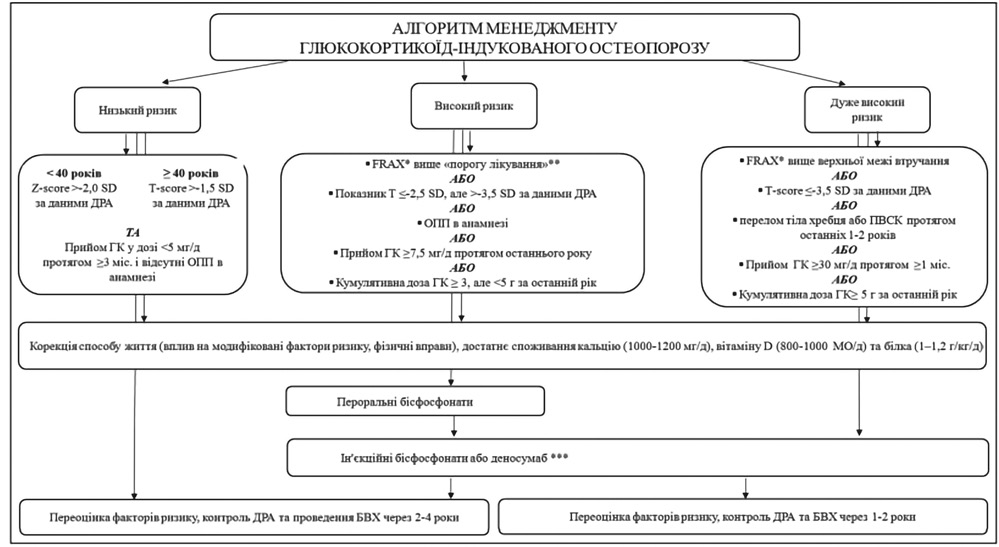
Примітки: ОПП — остеопоротичні переломи; ДРА — двохенергетична рентгенівська денситометрія; FRAX (fracture risk assessment tool) — 10-річна ймовірність основних ОПП; БВХ — бокова візуалізація хребта; SD — стандартне відхилення; *розрахунок FRAX з урахуванням дози ГК; **показник FRAX після переоцінки з урахуванням показників ДРА; ***1-ша лінія терапії за умови дуже високого ризику, 2-га лінія терапії за умови високого ризику ОПП.
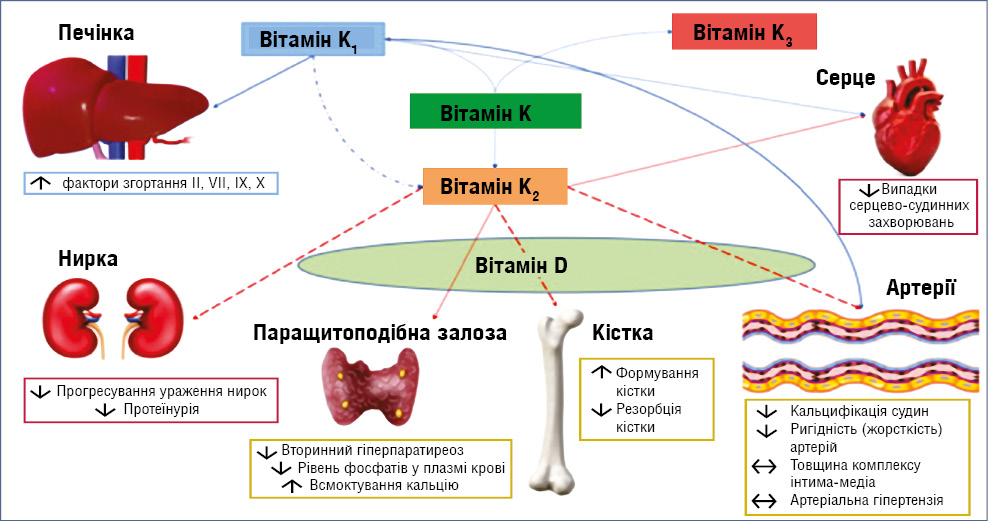
На окрему увагу заслуговують добавки вітаміну K2, які можуть покращувати якість кісткової тканини та знижувати ризик переломів у пацієнтів з остеопорозом, підвищуючи ефект кальцію та вітаміну D. Тісний взаємозв’язок між вітаміном D та різними формами вітаміну K (рис. 2) [16] має важливе значення для регуляції функції паращитоподібної залози, підтримки цілісності кісткової тканини та стану артерій; при цьому вітамін K2 особливо важливий для збереження здоров’я кісток і профілактики остеопорозу. Він підвищує γ-карбоксилювання остеокальцину — основного неколагенового білка кістки, завдяки чому остеокальцин ефективніше зв’язує кальцій з гідроксиапатитом, сприяючи формуванню кісткової тканини та запобігаючи відкладенню кальцію й фосфату у м’яких тканинах. Крім того, вітамін K2 є кофактором γ-карбоксилювання матричного Gla-білка, переводячи його з неактивної форми в активну, яка запобігає кальцифікації м’яких тканин. Підвищений рівень неактивного матричного Gla-білка у крові свідчить про дефіцит вітаміну K та пов’язаний з накопиченням кальцію у судинах, жорсткістю артерій і атеросклерозом [17]. Метааналіз 19 рандомізованих контрольованих досліджень показав, що у жінок з остеопорозом лікування вітаміном K2 значно підвищує МЩКТ хребців як у середньо- (6 міс), так і в довгостроковій перспективі (≥1 року) [20]. Дані систематичного огляду (рівень доказовості I) свідчать, що вітамін K2 запобігає переломам хребців на 60%, переломам стегна — на 77% та позахребцевим переломам — на 81% у пацієнтів японського походження [21]. Результати досліджень K. Ebina та співавторів (2013) і M.S. Abdel-Rahman та співавторів (2015) продемонстрували позитивний вплив вітаміну K2 на зниження активності маркерів запалення та деструкції у пацієнтів з ревматоїдним артритом (РА). Зокрема, додавання вітаміну K2 у дозі 45 мг/добу протягом 3 міс у хворих на РА та зниженою МЩКТ супроводжувалося полегшенням перебігу захворювання та зниженням рівня С-реактивного білка (СРБ) і матриксної металопротеїнази-3 (ММП-3) [20]. Аналогічно, застосування вітаміну K2 у дозі 100 мкг/добу асоціювалося зі зниженням рівня СРБ, ММП-3, швидкості осідання еритроцитів (ШОЕ), недокарбоксильованого остеокальцину, а також активності захворювання у пацієнтів з РА [21].
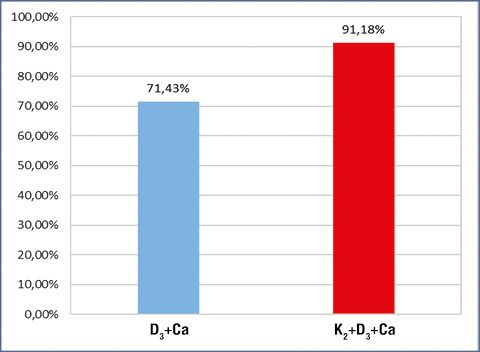
Дані іншого дослідження свідчать, що додавання вітаміну K2 до стандартної терапії кальцієм і вітаміном D3 у пацієнтів, які перенесли операцію на хребті з приводу поперекового міжтілового спондилодезу та заднього поперекового міжтілового спондилодезу, покращує консолідацію хребців на 21,6% та запобігає подальшому зниженню МЩКТ протягом 6 міс (рис. 3) [22]. У 6-місячному рандомізованому дослідженні за участю жінок у постменопаузальний період віком старше 60 років додавання вітаміну K2 до терапії вітаміном D та кальцієм зумовило значуще підвищення МЩКТ L3 та зниження рівня недостатньо карбоксильованого остеокальцину [23].
Іншим ключовим елементом організму є магній, близько 50–60% якого міститься у кістковій тканині, близько 1% — у позаклітинному просторі. Його дефіцит негативно впливає на кістки як безпосередньо — знижуючи їхню жорсткість, стимулюючи остеокластогенез і пригнічуючи остеобластогенез, так і опосередковано — через порушення регуляції паратгормону, вітаміну D, збільшення вираженості запалення та оксидативного стресу [17]. Дані обсерваційного дослідження Ініціативи з охорони здоров’я жінок продемонстрували, що споживання магнію понад 422,5 мг/добу асоціювалося з вищою МЩКТ стегна та всього тіла порівняно з <206,5 мг/добу [24]. Проте варто зазначити, що на сучасному ринку представлено різні форми магнію, серед яких на особливу увагу заслуговує магнію цитрат. Він має вищу біодоступність порівняно з неорганічними формами магнію, що робить його більш ефективним для поповнення дефіциту цього мікроелемента, особливо у випадках зниженого всмоктування при захворюваннях кишечнику [25].
Подібним чином цинку цитрат характеризується вищою біодоступністю порівняно з цинком сульфатом та цинком оксидом, що забезпечує кращу абсорбцію та ефективніше підвищення рівня цинку в організмі, особливо у пацієнтів із порушенням функцій шлунково-кишкового тракту або підвищеними потребами в цьому мікроелементі [26, 27]. У японському дослідженні показано, що у пацієнтів літнього віку з остеопорозом та дефіцитом цинку додавання до стандартної терапії 25 мг цинку 2 рази на добу протягом 12 міс зумовлювало підвищення його рівня в сироватці крові та значне зростання МЩКТ поперекового відділу хребта, стегна та шийки стегнової кістки. Тобто, на думку авторів, цинк стимулює формування та мінералізацію кісткової тканини остеобластами та пригнічує її резорбцію остеокластами, що потенційно знижує ризик переломів у пацієнтів похилого віку [28].
Сьогодні на фармацевтичному ринку України представлені засоби Остеоцитрат, рекомендований при остеопорозі, та Остеоцитрат МАКС, який доцільно вживати у період відновлення після переломів. Обидва продукти містять кальцій, магній та цинк (у формі цитрату), вітамін D3, вітамін K2, проте Остеоцитрат МАКС вирізняється підвищеною дозою вітаміну D3, що сприяє більш інтенсивній підтримці процесів регенерації кісткової тканини. Кальцію цитрат разом з іншими колагеноутворювальними мінералами (магнієм, цинком) у складі продукту легко засвоюється незалежно від прийому їжі. Вітамін D3 сприяє оптимальному всмоктуванню кальцію в кишечнику, а вітамін K2 — його транспорту з крові в кісткову тканину. Магній цитрат додатково підтримує нервово-м’язову функцію та структуру кістки, а цинку цитрат стимулює формування й мінералізацію кісткової тканини. Завдяки такій комбінації засіб спрямований на підвищення міцності кісток і зв’язкового апарату, водночас не підвищуючи ризику утворення ниркових каменів та відкладення кальцію в судинних стінках.
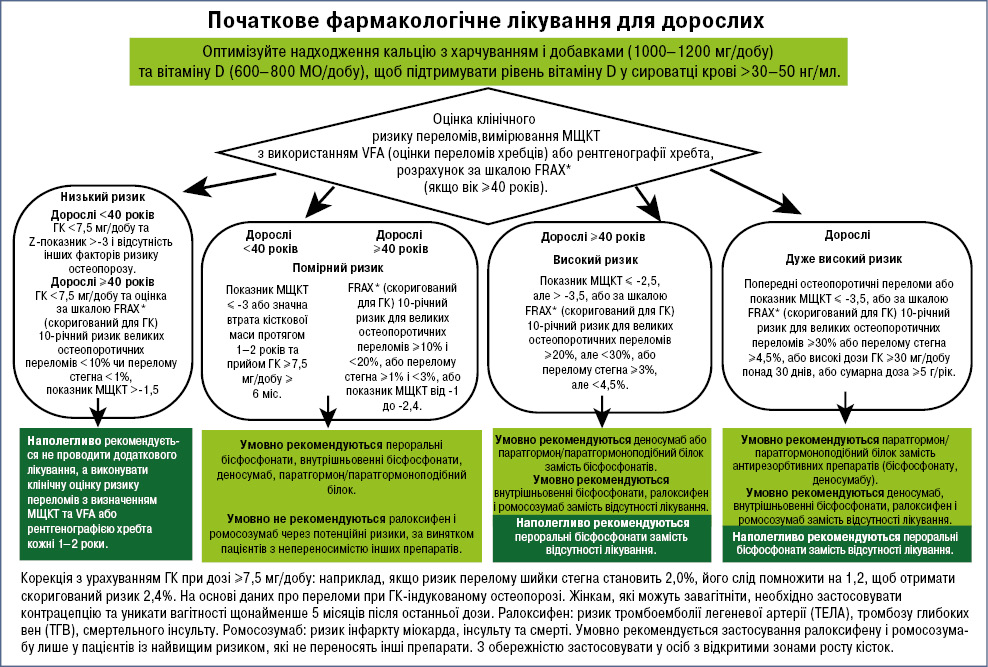
Узгоджуються з цими принципами й американські рекомендації, які деталізують підхід до стратифікації ризику й вибору оптимальної терапії для пацієнтів, що отримують ГК (рис. 4) [29].
Згідно з Національними рекомендаціями (рис. 1), для дорослих пацієнтів, які отримують ГК понад 3 міс та мають високий чи дуже високий ризик остеопоротичних переломів за FRAX, рекомендується розглядати питання ініціації антиостеопоротичного лікування. Вибір препарату слід здійснювати індивідуально, враховуючи рівень ризику, можливі побічні ефекти, наявність супутніх захворювань та переваги пацієнта (рівень узгодженості 6,9, сила рекомендації А). Для осіб із високим ризиком зазвичай рекомендовано починати терапію з пероральних бісфосфонатів [15], ефективність яких доведено у підвищенні МЩКТ поперекового відділу хребта та стегнової кістки, а також у зниженні ризику переломів хребців і позахребцевих переломів (рівень доказовості A; ступінь рекомендації 1) [1]. До схвалених для цього показання препаратів належать пероральний алендронат (5 або 10 мг щоденно, або 70 мг 1 раз на тиждень), ризедронат (5 мг щоденно або 35 мг 1 раз на тиждень) та внутрішньовенна золедронова кислота (5 мг 1 раз на рік) [5]. У випадках низької прихильності до лікування чи за наявності протипоказань можливим є застосування парентеральних бісфосфонатів або деносумабу (рівень узгодженості 6,9, сила рекомендації А). Якщо ж ризик переломів оцінюється як дуже високий, ініціацію терапії доцільно проводити переважно з парентеральних форм бісфосфонатів чи деносумабу (рівень узгодженості 6,8, сила рекомендації А) (рис. 1). Агоністи рецепторів паратиреоїдного гормону (ПТГ) також показані пацієнтам з високим ризиком, оскільки здатні підвищувати МЩКТ поперекового відділу хребта та знижувати частоту переломів хребців при лікуванні ГК (рівень доказовості B; ступінь рекомендації 1). Селективні модулятори рецепторів естрогену (selective estrogen receptor modulators — SERM) хоч і не мають доказів ефективності у зниженні ризику переломів хребців та позахребцевих переломів у жінок у постменопаузальний період з ГК-індукованим остеопорозом, проте можуть підвищувати МЩКТ у поперековому відділі хребта та стегновій кістці (рівень доказовості C; ступінь рекомендації 2), тому їх застосування можливе як додатковий варіант. Щодо антисклеростинових антитіл, через відсутність клінічних досліджень їхньої ефективності в профілактиці та лікуванні ГК-індукованого остеопорозу, офіційних рекомендацій наразі не надано [1].
Варто зазначити, що в основі будь-якого підходу до профілактики та лікування остеопорозу лежить забезпечення потреби організму у кальції та інших важливих мікронутрієнтах, адже саме їх дефіцит створює умови для активації резорбції кісткової тканини та знижує ефективність будь-якої фармакологічної терапії.
Таким чином, комплексний підхід до профілактики та лікування ГК-індукованого остеопорозу, що поєднує корекцію способу життя, оптимальну нутритивну підтримку та сучасну фармакотерапію, є найбільш ефективною стратегією зниження ризику остеопоротичних переломів у пацієнтів, які тривало отримують ГК.
Список використаної літератури
- 1. Tanaka Y., Soen S., Hirata S. et al. (2024) The 2023 Guidelines for the management and treatment of glucocorticoid-induced osteoporosis. J. Bone Miner. Metab., 42(2): 143–154. doi: 10.1007/s00774-024-01502-w.
- 2. Rice J.B., White A.G., Scarpati L.M. et al. (2017) Long-term Systemic Corticosteroid Exposure: A Systematic Literature Review. Clin. Ther., 39(11): 2216–2229. doi: 10.1016/j.clinthera.2017.09.011.
- 3. Anastasilaki E., Paccou J., Gkastaris K. et al. (2023) Glucocorticoid-induced osteoporosis: an overview with focus on its prevention and management. Hormones, 22: 611–622. doi: 10.1007/s42000-023-00491-1.
- 4. McDonough A.K., Curtis J.R., Saag K.G. (2008) The epidemiology of glucocorticoid-associated adverse events. Curr. Opin. Rheumatol., 20: 131–137. doi: 10.1097/BOR.0b013e3282f51031.
- 5. Chiodini I., Falchetti A., Merlotti D. et al. (2020) Updates in epidemiology, pathophysiology and management strategies of glucocorticoid-induced osteoporosis. Expert Rev. Endocrinol. Metab., 15: 283–298. doi: 10.1080/17446651.2020.1772051.
- 6. Compston J. (2018) Glucocorticoid-induced osteoporosis: an update. Endocrine, 61: 7–16. doi: 10.1007/s12020-018-1588-2.
- 7. Paccou J., Yavropoulou M.P., Naciu A.M. et al. (2024) Prevention and treatment of glucocorticoid-induced osteoporosis in adults: recommendations from the European Calcified Tissue Society. European Journal of Endocrinology, 191(6): G1–G17. doi: 10.1093/ejendo/lvae146.
- 8. Поворознюк В.В., Григор’єва Н.В. (2006) Препарати кальцію та вітаміну D у профілактиці та лікуванні остеопорозу. Раціональна фармакотерапія, 1(1).
- 9. Kenny A.M., Prestwood K.M., Biskup B. et al. (2004) Comparison of the effects of calcium loading with calcium citrate or calcium carbonate on bone turnover in postmenopausal women. Osteoporos Int., 15(4): 290–4. doi: 10.1007/s00198-003-1567-0.
- 10. Heller H.J., Greer L.G., Haynes S.D. et al. (2000) Pharmacokinetic and pharmacodynamic comparison of two calcium supplements in postmenopausal women. J. Clin. Pharmacol., 40(11): 1237–44.
- 11. Caudarella R., Vescini F. (2009) Urinary citrate and renal stone disease: the preventive role of alkali citrate treatment. Arch. Ital. Urol. Androl., 81(3): 182-7.
- 12. Polzonetti V., Pucciarelli S., Vincenzetti S. et al. (2020) Dietary intake of vitamin D from dairy products reduces the risk of osteoporosis. Nutrients, 12(6): 1743.
- 13. Bolland M.J., Avenell A., Baron J.A. et al. (2010) Effect of calcium supplements on risk of myocardial infarction and cardiovascular events: Meta-analysis. Br. Med. J., 341: c3691.
- 14. Homik J., Suarez-Almazor M.E., Shea B. et al. (2000) Calcium and Vitamin D for Corticosteroid-Induced Osteoporosis. Cochrane Database Syst. Rev., 2: CD000952. doi: 10.1002/14651858.CD000952.
- 15. Grygorieva N., Kovalenko V., Коrzh М. et al. (2024) Ukrainian guidelines for the prevention and treatment of glucocorticoid-induced osteoporosis. Pain, Joints, Spine, 14(3): 107–132. doi: 10.22141/pjs.14.3.2024.426.
- 16. Bellone F., Cinquegrani M., Nicotera R. et al. (2022) Role of Vitamin K in Chronic Kidney Disease: A Focus on Bone and Cardiovascular Health. Int. J. Mol. Sci., 23: 5282. doi: 10.3390/ijms23095282.
- 17. Hariri E., Kassis N., Iskandar J.P. et al. (2021) Vitamin K2-a neglected player in cardiovascular health: a narrative review. Open Heart., 8(2): e001715. doi: 10.1136/openhrt-2021-001715.
- 18. Huang Z.B., Wan S.L., Lu Y.J. et al. (2015) Does vitamin K2 play a role in the prevention and treatment of osteoporosis for postmenopausal women: a meta-analysis of randomized controlled trials, Osteoporos. Int., 26(3): 1175–1186, doi: 10.1007/s00198-014-2989-6.
- 19. Cockayne S., Adamson J., and Lanham-New S. (2006) Vitamin K and the prevention of fractures: systematic review and meta-analysis of randomized controlled trials, Archives of Internal Medicine., 166(12): 1256–1261. doi: 10.1001/archinte.166.12.1256.
- 20. Ebina K., Shi K., Hirao M. et al. (2013) Vitamin K2 administration is associated with decreased disease activity in patients with rheumatoid arthritis. Mod. Rheumatol., 23(5): 1001–7. doi: 10.1007/s10165-012-0789-4.
- 21. Abdel-Rahman M.S., Alkady E.A., Ahmed S. (2015) Menaquinone-7 as a novel pharmacological therapy in the treatment of rheumatoid arthritis: A clinical study. Eur. J. Pharmacol., 761: 273–8. doi: 10.1016/j.ejphar.2015.06.014.
- 22. Zhang W., Li L., Zhou X. et al. (2022) Concurrent Treatment with Vitamin K2 and D3 on Spine Fusion in Patients with Osteoporosis-Associated Lumbar Degenerative Disorders. Spine (Phila Pa 1976), 47(4): 352–360. doi: 10.1097/BRS.0000000000004309.
- 23. Je S.H., Joo N.S., Choi B.H. et al. (2011) Vitamin K supplement along with vitamin D and calcium reduced serum concentration of undercarboxylated osteocalcin while increasing bone mineral density in Korean postmenopausal women over sixty-years-old. J. Korean Med. Sci., 26(8): 1093–8. doi: 10.3346/jkms.2011.26.8.1093.
- 24. Castiglioni S., Cazzaniga A., Albisetti W. (2013) Magnesium and osteoporosis: current state of knowledge and future research directions, Nutrients, 5: 3022–3033. doi: 10.3390/nu5083022.
- 25. Громова О.А., Торшин И.Ю., Юргель И.С. (2009). Ретроспектива фармакокинетических исследований магниевых препаратов. Трудный пациент, 7 (6-7): 42–46.
- 26. Schlegel P., Windisch W. (2006) Bioavailability of zinc glycinate in comparison with zinc sulphate in the presence of dietary phytate in an animal model with Zn labelled rats. J. Anim. Physiol. Anim. Nutr. (Berl)., 90(5–6): 216–22. doi: 10.1111/j.1439-0396.2005.00583.x.
- 27. Wegmüller R., Tay F., Zeder C., et al. (2014) Zinc absorption by young adults from supplemental zinc citrate is comparable with that from zinc gluconate and higher than from zinc oxide. J. Nutr., 144(2): 132–6. doi: 10.3945/jn.113.181487.
- 28. Nakano M., Nakamura Y., Miyazaki A. (2021). Zinc Pharmacotherapy for Elderly Osteoporotic Patients with Zinc Deficiency in a Clinical Setting. Nutrients, 13(6): 1814. doi: 10.3390/nu13061814.
- 29. Humphrey M.B., Russell L., Danila M.I. et al. (2023) 2022 American College of Rheumatology Guideline for the Prevention and Treatment of Glucocorticoid-Induced Osteoporosis. Arthritis Rheumatol., 75(12): 2088–2102. doi: 10.1002/art.42646.
Відомості про авторів
Проценко Галина Олександрівна — докторка медичних наук, професорка, головна наукова співробітниця відділу некоронарних хвороб серця, ревматології та терапії ДУ «ННЦ «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д. Стражеска НАМН України», м. Київ.
ORCID ID: 0000-0001-9328-4839
Афанасьєва Інна Олександрівна — доцентка, кандидатка медичних наук, доцентка кафедри клінічної фармакології та клінічної фармації Національного медичного університету імені О.О. Богомольця, м. Київ.
E-mail: afanasevainna@meta.ua
ORCID ID: 0000-0002-2759-3948
Неміш Ірина Любомирівна — докторка філософії, кафедра внутрішньої медицини Буковинського державного медичного університету, м. Чернівці.
E-mail: iranemish@ukr.net
Надійшла до редакції/Received: 21.08.2025
Прийнято до друку/Accepted: 22.10.2025

Leave a comment