Хвороба відкладення пірофосфату кальцію: сучасний стан проблеми
Коваленко В.М.1, Дубкова А.Г.2, Крилова А.С.2, Гіреш Й.Й.1, Сілантьєва Т.С.2
- 1ДУ «Національний науковий центр «Інститут кардіології, клінічної та регенеративної медицини імені академіка М.Д.Стражеска НАМН України»
- 2Національний університет охорони здоров’я України імені П.Л. Шупика, Київ
Резюме. Хвороба відкладення пірофосфату кальцію є поширеною причиною гострого та хронічного артриту, викликаного відкладенням кристалів пірофосфату кальцію в суглобах і м’яких тканинах, що призводить до запалення та пошкодження суглобів. Вона має широкий спектр клінічних проявів і часто становить проблему для діагностики та лікування, оскільки зазвичай уражує пацієнтів літнього віку із супутніми захворюваннями. Мета: зробити огляд літератури та висвітлити сучасні аспекти лікування та моніторингу хвороби відкладення кристалів пірофосфату кальцію дигідрату. Методи дослідження: проведено пошук у друкованих і електронних виданнях, наукових пошукових базах Medline та PubMed із застосуванням методів аналізу, порівняння та узагальнення інформаційних даних. Відповідні статті, що стосуються хвороби відкладення кристалів пірофосфату кальцію дигідрату, ідентифіковані й розглянуті. Результати. У статті подано нові класифікаційні критерії хвороби відкладення кристалів пірофосфату кальцію дигідрату, опубліковані у 2023 р. Авторами огляду розглянуто сучасні рекомендації Американського коледжу ревматології (American College of Rheumatology — ACR) і Європейського альянсу ревматологічних асоціацій (European Alliance of Associations for Rheumatology — EULAR) з діагностики та лікування. У статті обговорюються питання медикаментозної терапії хвороби відкладення кристалів пірофосфату кальцію дигідрату. Проаналізовано нові дані щодо призначення біологічної терапії та напрямки лікування. Висновки. Хвороба відкладення кристалів пірофосфату кальцію дигідрату — актуальна проблема сучасної ревматології, яка має багато питань та напрямків, що потребують подальшого дослідження. Сучасній терапії артриту, зумовленого відкладенням кристалів пірофосфату кальцію, не вистачає надійних доказів, але очікується, що нові класифікаційні критерії цієї хвороби 2023 р. сприятимуть проведенню додаткових клінічних досліджень цієї поширеної кристалічної артропатії з чітко визначеними когортами пацієнтів, що дасть змогу отримати високоякісні докази для ведення цього стану у майбутньому.
DOI: 10.32471/rheumatology.2707-6970.94.18319
Хвороба відкладення пірофосфату кальцію — це артрит, спричинений кристалами пірофосфату кальцію. Донедавна вона називалася «псевдоподагрою». Цей термін походить від раннього опису цього захворювання у пацієнтів із гострим подагричним артритом, у яких кристали синовіальної рідини були стійкими до перетворення уриказою, а самі пацієнти, таким чином, не мали подагри. Синдром «псевдоподагри» вперше описаний Коном у 1962 р., який дослідив гострі напади синовіту, спровоковані кристалами ПФК [1]. Майже одночасно була опублікована серія випадків 27 пацієнтів в Угорщині, в яких виявили хронічний епізодичний запальний олігоартрит, що уражував головним чином коліна [2]. Ці пацієнти мали спільні рентгенологічні дані, а їх ранні описи прогнозували широкий спектр клінічних проявів, які зараз характеризують хворобу відкладення кристалів пірофосфату кальцію. Проблеми номенклатури переслідують цю хворобу з моменту її початкового опису. Різні громіздкі терміни, такі як «хвороба відкладення дигідрату пірофосфату кальцію», стали загальновживаними. У 2011 р. група Європейського альянсу ревматологічних асоціацій (European Alliance of Associations for Rheumatology — EULAR) рекомендувала, щоб термін «гострий кристалічний артрит відкладення пірофосфату кальцію» стосувався гострого запального артриту, який раніше був відомий як псевдоподагра, а термін «хронічний кристалічний артрит відкладення пірофосфату кальцію» використовувався для позначення інших типів артритів, пов’язаних з кристалами пірофосфату кальцію [3]. Термін «хондрокальциноз» належить до загального рентгенологічного прояву захворювання і не означає артриту клінічно.
Тому відкладення кристалів пірофосфату кальцію (Calcium Pyrophosphate Deposition — CPPD) — загальний термін, що охоплює усі патологічні стани, асоційовані з відкладенням кристалів пірофосфату кальцію в тканинах. Хвороба відкладення кристалів пірофосфату кальцію дигідрату (синонім — пірофосфатна артропатія) — захворювання, яке зумовлене утворенням та відкладенням у сполучній тканині кристалів пірофосфату кальцію дигідрату, варіант ектопічної кальцифікації гіалінового й фіброзного хряща (міжхребцевого диска, лобкового симфізу, менісків) з розвитком запалення. Хондрокальциноз — кальцифікація хряща, рентгенологічний феномен, не обов’язково пов’язаний з пірофосфатною артропатією (табл. 1).
Таблиця 1. Деякі клінічні варіанти перебігу пірофосфатної артропатії згідно з рекомендаціями EULAR 2011 [3]
| Клінічні варіанти | Характеристика |
|---|---|
| Псевдоподагра
(Pseudogout Type A) |
Для цього варіанта є характерним нападоподібний розвиток запалення суглобів (як при подагричному артриті). Зазвичай уражується один або кілька суглобів (на 1-му місці знаходяться колінні суглоби). Можуть відзначатися підвищення температури тіла, лейкоцитоз, підвищення швидкості осідання еритроцитів (ШОЕ). Напад гострого артриту триває 1–2 тиж і цілком купірується. Частота рецидивів нападів становить від 1–2 на рік до декількох протягом місяця. При повторних нападах завжди, крім інших, уражується суглоб, з якого починалася хвороба. Найхарактернішим є інтермітуючий перебіг з періодами загострення і зникнення симптомів. Прогресування з тяжким ураженням суглобів відзначається відносно рідко. Рентгенологічні зміни поступово збільшуються, хондрокальциноз стає більш вираженим і поширеним. Можливий кальциноз м’яких тканин, синовіальних сумок і сухожиль. На противагу подагрі переважно уражуються колінні суглоби. |
| Псевдоревматоїдний артрит
(Pseudo-Rheumatoid Arthritis Type B) |
Можливе стійке запалення декількох (іноді багатьох) суглобів кистей і стоп. При цьому ерозії кісток, ревматоїдний фактор у крові і деформація суглобів відсутні. |
| Псевдоостеоартрит з атаками
(Pseudoosteoarthritis with attacks Type C) |
Відзначаються біль у суглобах при рухах, дефігурація суглобів, обмеження рухів. Ознаки запалення (з випотом у порожнину суглобів) приєднуються часто або наявні постійно. Звичайно вони мало виражені. Під час нападів можливе незначне запалення багатьох суглобів. Уражуються 2–4 суглоби і, насамперед — колінні, променево-зап’ясткові, кульшові. Рідше уражуються гомілковостопні, ліктьові, п’ястково-фалангові (II і III пальців) суглоби. При рентгенологічному дослідженні виявляють ознаки, характерні для остеоартриту, а також хондрокальциноз менісків, гіалінового хряща, кальциноз капсули, синовіальної мембрани. Варто враховувати, що запалення суглобових тканин більш виражене при хондрокальцинозі порівняно з остеоартритом. На пізніх стадіях хвороби уражуються сухожилля і періартикулярні тканини. |
| Псевдоостеоартрит без атак (Pseudoosteoarthritis without attacks Type D) | Подібний до перебігу остеоартриту без загострень. |
| Асимптоматична (Asymptomatic Type E) | Без симптомів |
| Псевдонейропатична артропатія (Pseudo-neuropathic Type F) | У деяких випадках розвивається деструкція одного або декількох (рідше) великих суглобів. Зміни подібні до так званих нейропатичних артропатій (сирингомієлія, спинна сухотка). |
| Chondrocalcinosis | Хондрокальциноз |
Епідеміологія. Оцінки відрізняються, але хвороба відкладання кристалів пірофосфату кальцію уражує 4–7% дорослого населення в Європі та США. На жаль, наше поточне розуміння поширеності хвороби відкладення кристалів пірофосфату кальцію базується в основному на рентгенографічно виявленому хондрокальцинозі, а не на клінічно виявленому артриті. А наявність хондрокальцинозу, ймовірно, ідентифікують лише у близько 40% пацієнтів із клінічно значущим захворюванням. Тому питання про поширеність пірофосфатної артропатії є досить умовним.
Більшість пацієнтів, уражених гострим артритом з відкладенням пірофосфату кальцію, віком старше 65 років. 30–50% пацієнтів — віком старше 85 років [4]. Перехресне дослідження, яке включало 2157 випадків хвороби відкладення кристалів пірофосфату кальцію у ветеранів США, повідомило про точкову поширеність 5,2 на 1000 із середнім віком 68 років і 95% поширеності серед чоловіків [5]. Хвороба відкладення кристалів пірофосфату кальцію рідко виникає у пацієнтів віком до 60 років [6].
Патогенез [7]. Вважається, що хвороба відкладення пірофосфату кальцію спричинена дисбалансом між виробництвом пірофосфату та рівнями пірофосфатаз в ураженому хрящі. Оскільки пірофосфат відкладається в синовіальній оболонці та прилеглих тканинах, він поєднується з кальцієм, утворюючи кристали пірофосфату кальцію. Кристали пірофосфату кальцію рідко утворюються в нехрящових тканинах. Таким чином, клітини та високоспеціалізований позаклітинний матрикс хряща явно зумовлюють розвиток хвороби. Хондроцити конститутивно генерують перицелюлярні везикули розміром з екзосому, які називаються «суглобовими хрящовими везикулами», які слугують важливими місцями утворення кристалів у хрящі. Хондроцити також виробляють високі рівні позаклітинного неорганічного пірофосфату, який є критичним для утворення кристалів. У хрящі більша частина неорганічного пірофосфату утворюється з позаклітинного аденозинтрифосфату (АТФ).
Позаклітинний АТФ метаболізується до неорганічного пірофосфату ферментами з нуклеозидтрифосфат-пірофосфогідролазною активністю, такими як ектонуклеотидпірофосфатаза, тоді як лужна фосфатаза та інші пірофосфатази розкладають неорганічний пірофосфат. Крім того, фактори росту, цитокіни та деякі фармакологічні засоби модулюють рівні неорганічного пірофосфату в хрящі.
Кристали пірофосфату кальцію викликають запалення в синовіальному просторі, але також зумовлюють несприятливі біомеханічні наслідки та прямі катаболічні ефекти на тканини суглобів завдяки виробленню простагландину E2 і матриксних металопротеїназ. Ці фактори в кінцевому підсумку призводять до дегенерації хряща, про що свідчить відкладення кристалів пірофосфату кальцію у хрящі in situ. Вони ініціюють запалення, активуючи компоненти інфламасоми NLRP3 і створюючи позаклітинні пастки нейтрофілів. Відкладення кристалів пірофосфату кальцію у суглобовому хрящі також змінюють механічні властивості хряща, що може спричинити або прискорити пошкодження суглобів.
Клінічні форми. Виділяють три основні форми пірофосфатної артропатії: генетичну (сімейну), вторинну і первинну (ідіопатичну, спорадичну) [8]. Описані також форми хвороби, зумовлені травмою або хірургічним втручанням (табл. 2).
Інструментальні методи діагностики
Рентгенографія суглобів [9]
Таблиця 2. Основні форми пірофосфатної артропатії
| Форми | Їх характеристика |
|---|---|
| Сімейна (генетична) | Для неї є характерною рання (на 4-му десятилітті) поява симптомів хвороби, їх значна вираженість, генералізоване ураження суглобів. Захворювання успадковується за аутосомно-домінантним типом, хворіють в основному чоловіки. Має сімейний характер (хондрокальциноз у віці до 50 років) |
| Вторинна | Виникає на тлі спадкових і набутих метаболічних захворювань: гіперпаратиреозу, сімейної гіпокальціуричної гіперкальціємії, гемохроматозу, гемосидерозу, гіпофосфатазії, хвороби Коновалова — Вільсона, гіпомагнезіємії. Вважають, що для утворення кристалів пірофосфату кальцію має значення підвищення рівня заліза, міді, кальцію, зниження магнію. Кристали пірофосфату кальцію виявляють у синовіальній рідині у пацієнтів із хворобою Педжета, акромегалією, охронозом, остеоартритом, подагрою, гіпотиреозом, амілоїдозом, гіпермобільністю суглобів, при травмах і ушкодженнях суглобів. |
| Ідіопатична | У більшості випадків причина розвитку пірофосфатної артропатії залишається невідомою. |
Виявляють відкладення кальцію в поверхневих відділах хрящової тканини. Ці відкладення мають різний характер — у виді зерен, смуг, гомогенних скупчень. Вапно відкладається і по краю міжхребцевих дисків. Результати рентгенологічного дослідження уражених суглобів:
- вогнищева або лінійна кальцифікація суглобового хряща, найбільш часто відмічається в колінному, плечовому, тазостегновому суглобах, лобковому симфізі;
- субхондральні кісти;
- фрагментація хряща з утворенням внутрішньосуглобових рентгенопозитивних тіл.
Виявлення хондрокальцинозу у фіброзних та гіалінових хрящах:
- хрящі менісків колінних суглобів;
- хрящ симфізу;
- трикутний фіброзний хрящ променезап’ясткового суглоба;
- фіброзний хрящ ацетабулярної западини.
Для гіалінових хрящів характерна лінійна кальцифікація: суглоби, що уражуються — колінні, плечові, ліктьові.
Виявлення кальцифікатів м’яких тканин:
- ахіллові сухожилля (рис. 1);
- фасція підошви;
- навколосуглобові м’які тканини.
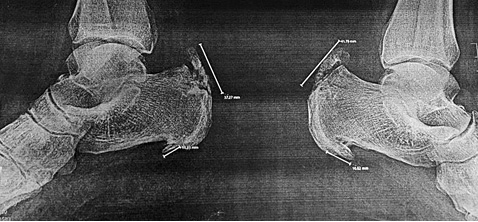
У пацієнтів із підозрою на хворобу відкладення кристалів пірофосфату кальцію, але з відсутністю в уражених суглобах хондрокальцинозу, рекомендована рентгенографія інших суглобів, що часто уражуються:
- передньо-задня проєкція обох колінних суглобів;
- передньо-задня проєкція симфізу;
- задньо-передня проєкція обох зап’ястків.
У тих випадках, коли хвороба починається в дитячому віці, розвиваються анкілоз хребта і множинні ураження суглобів. У тяжких випадках виявляють остеоліз (табл. 3).
Таблиця 3. Клінічні форми відкладення пірофосфату кальцію EULAR 2011 [3]
| Клінічні форми | Визначення |
|---|---|
| Безсимптомна хвороба відкладення кристалів пірофосфату кальцію | Хондрокальциноз
Остеоартрит з хондрокальцинозом або безсимптомний |
| Остеоартрит з хворобою відкладення кристалів пірофосфату кальцію | Хвороба відкладення кристалів пірофосфату кальцію за наявності остеоартриту клінічно |
| Гострий мікрокристалічний артрит, асоційований з пірофосфатом кальцію | Синовіїт з хворобою відкладення кристалів пірофосфату кальцію (замінив термін «псевдоподагра») |
| Хронічний мікрокристалічний артрит з пірофосфатом кальцію | Хронічний артрит, асоційований з хворобою відкладення кристалів пірофосфату кальцію |
Ультразвукова діагностика хондрокальцинозу [10]
Ультразвукові критерії верифікації наявності депозитів пірофосфату кальцію у хрящовій тканині суглоба:
- тонкі гіперехогенні смуги, паралельні поверхні гіалінового хряща, аналогічні рентгенологічному феномену хондрокальцинозу (наприклад в колінних суглобах);
- пунктирні депозити (плямисті структури), що складаються з декількох дрібних гіперехогенних плям (найбільш поширені в трикутних фіброзно-хрящових комплексах і сухожиллях);
- гомогенні гіперехогенні вузлові або округлі депозити, частіше рухливі (локалізовані в бурсах або суглобових заворотах).
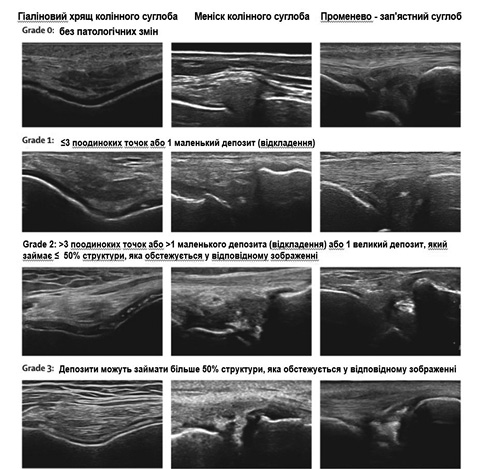
У 2023 р. опубліковані нові рекомендації OMERACT щодо ультразвукової оцінки ступеня відкладення кристалів пірофосфату кальцію (табл. 4, рис. 2) [12].
Таблиця 4. Ідентифікація хвороби відкладення пірофосфату кальцію за допомогою ультразвуку OMERACT 2018 [11]
| Структура | Форма | Ехогенність | Локалізація | Зміни при динамічному скануванні |
|---|---|---|---|---|
| Суглобовий (фіброзний) хрящ | Відкладення змінної форми | Гіперехогенні (схожі на ехогенність поверхні кістки) | Локалізується всередині волокнисто-хрящової структури | Залишаються фіксованими та рухаються разом із фіброзним хрящем під час динамічної оцінки (тобто рух суглоба та стиснення датчиком) |
| Гіаліновий хрящ | Відкладення різного розміру та форми | Гіперехогенні (подібні до ехогенності кори кістки), які не створюють задньої тіні | Локалізується в межах гіалінового хряща | Відкладення залишаються фіксованими та рухаються разом з гіаліновим хрящем (тобто рух суглоба та стиснення датчиком) |
| Сухожилля | Множинні лінійні (паралельні фібрилярній структурі сухожилля, не збігаються з профілем кістки) відкладення | Гіперехогенні (по відношенню до ехогенності сухожиль), які зазвичай не створюють задньої тіні. Відкладення зберігають високий ступінь ехогенності навіть при дуже низьких рівнях посилення і не піддаються впливу анізотропії, як навколишнє сухожилля | Локалізується в межах сухожилля | Залишаються фіксованими та рухаються разом із сухожиллям під час руху та стиснення датчиком |
| Синовіальна рідина | Відкладення різного розміру (від точкових до великих) | Гіперехогенні (подібні до ехогенності поверхні кістки), які зазвичай не створюють задньої тіні | Локалізується в синовіальній рідині | Рухливі за рухами в суглобі і тиском датчика |
Лабораторні методи [8]
Золотим стандартом діагностики хвороби відкладення кристалів пірофосфату кальцію є виявлення його кристалів в синовіальній рідині за допомогою поляризаційної світлової мікроскопії або ж фазово-контрастної мікроскопії. За умов кваліфікованого тренованого спеціаліста методи мають високу специфічність і чутливість. У синовіальній рідині виявляється велика кількість мікрокристалів пірофосфату кальцію, що знаходиться як у вільному стані, так і всередині фагоцитів. Характерним є виражений цитоз (5000–40 000 у мкл) за рахунок полінуклеарів. Діагноз відкладення пірофосфату кальцію підтверджується наявністю характерних кристалів (у формі паралелепіпеда), переважно внутрішньоклітинних, з відсутністю або слабким світловідображенням в синовіальній рідині або (рідко) в біоптаті тканини.
При виявленні кристалів пірофосфату кальцію дигідрату методом поляризаційної мікроскопії можуть виникати деякі складнощі. Так, кристали пірофосфату кальцію мають слабке променезаломлення, що ускладнює їх візуалізацію. Неодмінною умовою візуалізації кристалів пірофосфату кальцію є їх досить висока концентрація в синовіальній рідині. Низька концентрація цих кристалів може призвести до негативного результату. Поріг концентрації для надійної ідентифікації кристалів методом поляризаційної мікроскопії — 10–100 мкг/мл.
У період нападів виявляють нейтрофільний лейкоцитоз, збільшення ШОЕ, вмісту С-реактивного білка (СРБ), α2– і γ-глобулінів, серомукоїду.
Через супутні асоційовані захворювання, такі як гіперпаратиреоїдизм, гемохроматоз, або гіпомагніємія, рекомендовано визначати рівні заліза, трансферину, феритину, кальцію, магнію, лужної фосфатази та паратгормону в крові.
Гістологічні зміни, що виявляються в синовіальній оболонці, — у біоптаті відкладення кристалів пірофосфату кальцію, заліза й ознаки реактивного запалення.
Верифікація діагнозу проводиться з урахуванням виявлення кристалів пірофосфату кальцію в синовіальній рідині при поляризаційній мікроскопії та/або характерній рентгенологічній картині: хондрокальциноз менісків і суглобового хряща.
Діагностичні критерії Хвороби відкладення кристалів пірофосфату кальцію [7]
Точний діагноз хвороби відкладення кристалів пірофосфату кальцію потребує або виявлення кристалів пірофосфату кальцію в поляризаційному світлі та хондрокальцинозу чи кальцифікації м’яких тканин на рентгенограмах суглобів, або виявлення кристалів пірофосфату кальцію у тканинах або синовіальній рідині іншими надійними способами (рентгенівська дифракція, спектроскопія).
Ймовірний діагноз хвороби відкладення кристалів пірофосфату кальцію встановлюють за наявності одного з чинників:
- ідентифікація кристалів методом поляризаційної світлової мікроскопії
або
- наявність типової кальцифікації хряща або суглобової капсули при рентгенівському дослідженні будь-якого типового суглоба.
Можливий діагноз хвороби відкладення кристалів пірофосфату кальцію
- Гострий артрит крупних суглобів, особливо колінних,
або
- хронічний артрит, що нагадує остеоартрит, особливо якщо уражені суглоби нехарактерні для остеоартриту (зап’ястки, суглоби (Міжнародна класифікація функціонування), лікті та плечі) і якщо він супроводжується гострими атаками, що минають самостійно.
ДІАГНОСТИЧНІ КРИТЕРІЇ ХВОРОБИ ВІДКЛАДЕННЯ КРИСТАЛІВ ПІРОФОСФАТу КАЛЬЦІЮ (ACR, EULAR 2023 р.) [13]
Визначення критеріїв
Критерії класифікації хвороби відкладення кристалів пірофосфату кальцію слід застосовувати в такому порядку:
1. Вхідний критерій: ви коли-небудь мали принаймні один епізод болю в суглобах, набряку або чутливості.
2. Критерії абсолютного виключення: усі симптоми, швидше за все, пояснюються альтернативним захворюванням (таким як ревматоїдний артрит, подагра, псоріатичний артрит, остеоартрит тощо).
3. Достатні критерії: наявність або crowned dens syndrome, або аналіз синовіальної рідини, що демонструє кристали пірофосфату кальцію у суглобі з набряком, чутливістю або болем.
Особа класифікується як така, що має хворобу відкладення кристалів пірофосфату кальцію, якщо вхідний критерій виконано, критерій виключення не виконано і принаймні один достатній критерій виконано.
Якщо немає жодного з достатніх критеріїв, особа класифікується як така, що має хворобу відкладення кристалів пірофосфату кальцію, якщо сума критеріїв >56 балів (табл. 5).
Таблиця 5
| Критерії та показники | Бали |
|---|---|
| A. Вік появи симптомів суглобів (біль, припухлість та/або чутливість) | |
| ≤60 років | 0 |
| >60 років | 4 |
| B. Перебіг і симптоми запального артриту§ | |
| Відсутність постійного або типового запального артриту | 0 |
| Стійкий запальний артрит | 9 |
| Типовий епізод гострого артриту | 12 |
| Більш ніж один типовий епізод гострого артриту | 16 |
| C. Місце типового епізоду(ів) запального артриту в периферичних суглобах | |
| Перший плюснефаланговий суглоб | −6 |
| Немає типових епізодів | 0 |
| Суглоб (суглоби), крім променезап’ястного, колінного або першого плюснефалангового суглоба | 5 |
| Променезап’ястний суглоб | 8 |
| Колінний суглоб | 9 |
| D. Супутні метаболічні захворювання¶ | |
| Жодного | 0 |
| Наявні | 6 |
| E. Аналіз кристалів синовіальної рідини з симптоматичного суглоба# | |
| Кристали пірофосфату кальцію відсутні ≥2 проб | −7 |
| Кристали пірофосфату кальцію відсутні в 1 пробі | −1 |
| Не виконано | 0 |
| F. Остеоартрит кисті/променезап’ястного суглоба на візуалізації (визначається як наявний, якщо показник K/L ≥2) | |
| Жодна із наведених нижче знахідок або візуалізація променезап’ястного суглоба/кисті не виконана | 0 |
| Остеоартрит променезап’ястних суглобів білатерально | 2 |
| 2 з наступних знахідок: остеоартрит скафотрапецієподібного суглоба без остеоартриту зап’ястно-п’ясного суглоба; остеоартрит другого плюснефалангового суглоба; остеоартрит третього плюснефалангового суглоба | 7 |
| G. Візуалізаційні докази CPPD у симптоматичних периферичних суглобах** | |
| Немає на УЗД, КТ або двоенергетичній КТ (і відсутні на звичайній рентгенографії або звичайна рентгенографія не виконана) | −4 |
| Немає на звичайній рентгенографії (і УЗД, КТ, двоенергетична КТ не виконана) | 0 |
| Наявні на звичайній рентгенографії, УЗД, КТ або двоенергетичній КТ | 16 |
| H. Кількість периферичних суглобів із ознаками CPPD при будь-якому методі візуалізації незалежно від симптомів** | |
| Жодного | 0 |
| 1 | 16 |
| 2–3 | 23 |
| ≥4 | 25 |
*CPPD — Calcium Pyrophosphate Deposition (відкладення кристалів пірофосфату кальцію); K/L — Келлгрен/Лоуренс.
†Епізод, що виникає в периферичному суглобі або, у випадку crowned dens syndrome, в осьовому суглобі, такому як C1/C2.
‡Сrowned dens syndrome визначається як наявність а) клінічних ознак і б) ознак візуалізації. Клінічні ознаки включають гострий або підгострий початок сильного болю, локалізованого у верхній частині шиї, з підвищеними маркерами запалення, обмеженням обертання та часто лихоманкою. Слід виключити імітаційні стани, такі як ревматична поліміалгія та менінгіт. Особливості візуалізації включають звичайну КТ, яка показує кальцієві відкладення, як правило, лінійні та менш щільні, ніж кортикальна кістка, у поперечній ретроодонтоїдній зв’язці (поперечна зв’язка атланту), часто з виглядом 2 паралельних ліній на аксіальних проєкціях. Також характерні кальцифікації в атланто-аксіальному суглобі, алярній зв’язці та/або в панусі, що прилягає до кінчика зубів. Функції двоенергетичної КТ (DECT) включають індекс подвійної енергії 0,016–0,036. Повинні бути наявні як клінічні ознаки, так і особливості візуалізації. Достатні критерії також виконуються, якщо кристали пірофосфату кальцію (CPP) виявлені при гістопатологічному аналізі тканини суглоба, за умови, що пацієнт відповідає критеріям для класифікації, тобто ще не відповідає критеріям виключення. Наприклад, відкладення кристалів CPP у суглобовому хрящі у пацієнтів з кінцевою стадією остеоартриту не можна використовувати для класифікації пацієнта як хворого на хворобу відкладення пірофосфату кальцію (CPPD), коли всі симптоми краще пояснити наявністю остеоартриту (критерії виключення).
§Стійкий запальний артрит визначався як триваючий набряк суглоба з болем та/або місцевим (локальним) підвищенням температури у ≥1 суглобі. Типовий епізод визначався як епізод із гострим початком або гострим посиленням болю в суглобах із набряком та/або локальним підвищенням температури тіла, що минає незалежно від лікування.
¶Включаючи спадковий гемохроматоз, первинний гіперпаратиреоз, гіпомагніємію, синдром Гітельмана, гіпофосфатазію або сімейний анамнез хвороби відкладення пірофосфату кальцію.
#Аналіз синовіальної рідини повинна виконувати особа, яка навчена використовувати мікроскопію з компенсованим поляризованим світлом для ідентифікації кристалів.
**Візуалізація принаймні одного симптоматичного периферичного суглоба за допомогою рентгенографії, УЗД, КТ або двоенергетичної КТ вимагається для класифікації, якщо достатні критерії не відповідають. Візуалізаційні докази хвороби відкладення пірофосфату кальцію стосуються кальцифікації фіброзного або гіалінового хряща. Не слід оцінювати кальцифікацію синовіальної оболонки, суглобової капсули або сухожилля. Враховувати лише залучення периферичних суглобів.
Оцінка критеріїв
Показники можуть бути оцінені, якщо вони були наявні протягом життя пацієнта. Якщо пацієнт виконує >1 пункту в певному розділі, оцінюватиметься лише пункт з найвищою силою. Потрібна візуалізація принаймні одного симптоматичного суглоба за допомогою звичайної рентгенографії, ультразвукового дослідження (УЗД), комп’ютерної томографії (КТ) або двоенергетичної КТ.
Діагностичні ознаки хондрокальцинозу
При проведенні диференційної діагностики необхідно враховувати наступні ознаки:
- наявність хондрокальцинозу у родичів;
- гострі напади артриту з ураженням колінного або іншого великого суглоба;
- нормальна концентрація сечової кислоти в крові;
- виявлення кристалів пірофосфату кальцію в синовіальній рідині та біоптатах синовіальної оболонки;
- наявність відкладення кальцію в ділянці суглобної капсули при рентгенологічному дослідженні.
Лікування (табл. 6)
Таблиця 6. Лікування згідно з рекомендаціями EULAR 2011 р. [14]
| No | Рекомендація | Рівень | Сила |
|---|---|---|---|
| 1 | Оптимальне лікування хвороби відкладення пірофосфату кальцію потребує обох нефармакологічних та фармакологічних методів лікування та має бути чітко витримане відповідно до клінічної форми (ізольований хондрокальциноз, хронічний артрит з відкладенням ПФК, індукований артрит, остеоартрит з хворобою відкладення пірофосфату кальцію); загальних факторів ризику (вік, коморбідність); факторів ризику для метаболічних розладів | IV | 93 (85 до 100) |
| 2 | Для гострого мікрокристалічного артриту, асоційованого з пірофосфатом кальцію, оптимальне і безпечне лікування включає аплікації льоду, холод, спокій, аспірацію синовіальної рідини та в/суглобове введення глюкокортикоїдів | IIa–IV | 95 (92 до 98) |
| 3 | І пероральні НПЗП (з призначенням препаратів для гастропротекції), і низькі дози колхіцину (0,5 мг 3–4 рази на добу з/без початкової дози 1 мг) є ефективними методами лікування, хоча їх призначення може бути обмежене токсичністю та коморбідністю, особливо у пацієнтів старшого віку | Ib–IIb | 79 (66 до 91) |
| 4 | Короткий курс пероральних або внутрішньовенних глюкокортикоїдів може бути ефективним у пацієнтів з гострим мікрокристалічним артритом, асоційованим з пірофосфатом кальцію | IIb–III | 87 (76 до 97) |
| 5 | Мета та методи лікування пацієнтів з остеоартритом та хворобою відкладення пірофосфату кальцію такі самі, як і для остеоартриту без хвороби відкладення пірофосфату кальцію | IIb–IV | 81 (70 до 92) |
| 6 | Профілактика частих загострень хвороби відкладення пірофосфату кальцію — низькі дози колхіцину (0,5–1 мг на добу) або низькі дози НПЗП (з призначенням препаратів для гастропротекції) | Ia | 84 (74 до 94) |
| 7 | Для хронічного мікрокристалічного артриту, асоційованого з пірофосфатом кальцію, препаратами вибору є в порядку черговості пероральні НПЗП (з призначенням препаратів для гастропротекції), низькі дози колхіцину (0,5 мг 3–4 рази на добу з/без початкової дози 1 мг), низькі дози глюкокортикоїдів, метотрексат, гідроксихлорохін | Ib–IV | 79 (67 до 91) |
| 8 | Якщо виявлені супутні асоційовані захворювання, такі як гіперпаратиреоїдизм, гемохроматоз, або гіпомагніємія, їх слід лікувати | Ib 89 | (81 до 98) |
| 9 | Наразі немає лікування, яке здатне впливати на формування або розчинення кристалів пірофосфату кальцію, також лікування не потребує безсимптомна хвороба відкладення пірофосфату кальцію | IV | 90 (83 до 97) |
Синтетичний адренокортикотропний гормон (тетракозактид). Синтетичний адренокортикотропний гормон (АКТГ) може бути корисною альтернативою лікуванню гострих епізодів хвороби відкладення кристалів пірофосфату кальцію артриту у пацієнтів, яким протипоказані глюкокортикоїди, нестероїдні протизапальні препарати (НПЗП) і колхіцин. Невелике ретроспективне дослідження, яке оцінювало використання синтетичного АКТГ у 14 пацієнтів з гострим артритом з хворобою відкладення кристалів пірофосфату кальцію, повідомило про значне зменшення вираженості болю протягом 24 год у 13/14 пацієнтів. Інша серія випадків із 5 пацієнтів із гострою хворобою відкладення кристалів пірофосфату кальцію повідомила про зникнення гострих нападів у середньому через 4,2 дня після введення АКТГ. Побічні ефекти включали легку гіпокаліємію, яка не потребувала втручання [15].
Анакінра. Кілька серій випадків описують використання анакінри в лікуванні гострого кристалічного артриту хвороби відкладення кристалів пірофосфату кальцію. Нещодавній систематичний огляд літератури ідентифікував загалом 76 пацієнтів, які отримували лікування анакінрою, у більшості з яких описаний рецидивний гострий артрит з хворобою відкладення кристалів пірофосфату кальцію [16]. Ефективність доведена у вигляді зниження рівня СРБ у 73% випадків, покращення стану за візуальною аналоговою шкалою (ВАШ) у 70,3% випадків. Анакінра залишається хорошим вибором для пацієнтів з рефрактерною хворобою відкладення кристалів пірофосфату кальцію. Необхідні подальші рандомізовані контрольовані дослідження, щоб краще охарактеризувати оптимальну дозу та тривалість призначення анакінри при лікуванні цієї патології.
Пероральні інгібітори запалення NLRP3 (дапансутрил).
У відкритому дослідженні фази 2а дапансутрил продемонстрував прийнятний профіль безпеки та ефективність у зменшенні вираженості цільового болю в суглобах у пацієнтів із гострими нападами подагри. Теоретично такі препарати можна застосовувати для лікування та профілактики гострого артриту з хворобою відкладення кристалів пірофосфату кальцію [17]. Ці препарати мали б перевагу перед анакінрою завдяки пероральному, а не підшкірному способу введення. Потрібні майбутні дослідження з оцінки застосування пероральних інгібіторів NLRP3 у лікуванні кристалічного артриту, включаючи гострий артрит з хворобою відкладення кристалів пірофосфату кальцію.
Хронічний кристалічний запальний артрит з Хворобою відкладення кристалів пірофосфату кальцію
Лікування, що ґрунтується на доказах, досі немає, хоча була проведена невелика кількість досліджень, які оцінювали метотрексат, тоцилізумаб і гідроксихлорохін (HCQ).
Метотрексат. Базуючись на успішному зниженні балів болю, виміряних пацієнтом за ВАШ у двох невеликих серіях випадків, EULAR раніше рекомендувала метотрексат як засіб для лікування тяжкої рефрактерної хвороби відкладення кристалів пірофосфату кальцію. Однак ця рекомендація згодом була відмінена через результати невеликого подвійного сліпого рандомізованого перехресного дослідження, що включало 26 пацієнтів, які не досягли первинної кінцевої точки щодо демонстрації значного покращення балу DAS44 у пацієнтів з артропатією з хворобою відкладення кристалів пірофосфату кальцію [18]. Проте хоча недостатньо даних на підтримку застосування метотрексату в лікуванні хвороби відкладення кристалів пірофосфату кальцію, необхідні додаткові дослідження для остаточної оцінки використання цієї потенційної терапії, яка є недорогим, безпечним та добре знайомим ревматологам методом лікування.
Тоцилізумаб. Показано, що кристали пірофосфату кальцію індукують експресію прозапального цитокіну інтерлейкіну (IL)-6 [19]. Таким чином, IL-6 є вірогідною терапевтичною мішенню для лікування клінічних симптомів хвороби відкладення кристалів пірофосфату кальцію. Найбільша серія випадків включала 11 пацієнтів, 7 з яких раніше отримували лікування анакінрою [20]. Тоцилізумаб вводили щомісяця внутрішньовенно або щотижня підшкірно. Через 3 міс середня загальна оцінка за ВАШ знизилася з 60 до 15. Ця відповідь зберігалася протягом 10 міс після припинення лікування. Крім того, 3 пацієнтів, які залежали від щоденної дози 7–10 мг преднізону, змогли знизити дозу, а 2 змогли повністю припинити прийом [20]. Проте відображення в рекомендаціях також не знайдено.
Гідроксихлорохін оцінювали при хворобі відкладення кристалів пірофосфату кальцію в одному подвійному сліпому рандомізованому перехресному дослідженні за участю 36 пацієнтів (19 у групі лікування проти 17 у групі плацебо) [21]. Пацієнти в групі лікування отримували гідроксихлорохін 100 мг на добу, титруючи щомісяця до 400 мг на добу. Рівень відповіді (як визначено принаймні на 30% зменшенням кількості опухлих і чутливих суглобів) виявили у 76% пацієнтів групи лікування порівняно з 32% у групі плацебо. Крім того, під час відкритого періоду дослідження відповідь на лікування відмічена у 85% пацієнтів, які перейшли з плацебо.
Синовектомія. Радіаційну синовектомію оцінювали в невеликому подвійному сліпому самоконтрольованому дослідженні, яке включало 15 пацієнтів із двобічною хворобою відкладення кристалів пірофосфату кальцію колінного суглоба. Пацієнти отримували внутрішньосуглобово ітрій-90 (5 мКі) плюс тріамцинолону гексацетонід 20 мг в одне коліно та фізіологічний розчин плюс тріамцинолону гексацетонід в контралатеральне контрольне коліно. Через 6 міс виявлено суттєве зменшення вираженості болю, скутості, болючості суглоба та випоту у пацієнтів, які отримували лікування, порівняно з контрольною групою (p<0,05) [22]. Синовіальна деструкція лазерним опроміненням була оцінена в іншому невеликому дослідженні за участю 49 пацієнтів. Група порівняння отримувала перорально диклофенак. Відповідь визначалася як зменшення вираженості болю на 60–100% і виявлена у 69,2% пацієнтів групи лікування та 60,8% — групи диклофенаку (р<0,05) [23].
Остеоартрит з хворобою відкладення кристалів пірофосфату кальцію
EULAR 2011 рекомендує лікувати остеоартрит з хворобою відкладення кристалів пірофосфату кальцію відповідно до рекомендацій стосовно остеоартриту включно з нефармакологічними та фармакологічними методами.
Незважаючи на те що запальний компонент і швидкість прогресування остеоартриту при хворобі відкладення кристалів пірофосфату кальцію більші, рекомендації залишаються такі самі, як і при остеоартриті. Єдине застереження — з обережністю застосовувати внутрішньосуглобове введення гіалуронату — провокує загострення артриту.
Хвороба відкладення кристалів пірофосфату кальцію, пов’язана із захворюваннями поза межами суглобів
1. Ризик серцево-судинних захворювань нещодавно досліджений у пацієнтів з хворобою відкладення кристалів пірофосфату кальцію. На 25% вищий ризик нефатальних серцево-судинних подій у когорті хворих порівняно з контрольною групою [24].
2. Низька мінеральна щільність кісткової тканини зареєстрована у двох когортних дослідженнях за участю пацієнтів із хондрокальцинозом або хворобою відкладення кристалів пірофосфату кальцію. Ремоделювання субхондральної кістки може відігравати роль у патогенезі хвороби відкладення кристалів пірофосфату кальцію через втрату функції остеопротегерину, що призводить до посилення остеокластогенезу. Кумулятивна частота переломів вища у пацієнтів з гострим кристалічним артритом з хворобою відкладення кристалів пірофосфату кальцію, ніж у групі порівняння у великій електронній базі даних.
Отже, хвороба відкладення кристалів пірофосфату кальцію дигідрату — актуальна проблема сучасної ревматології, яка ще має багато питань та напрямків, що потребують подальшого дослідження.
Список використаної літератури
- 1. Kohn N. (1962) The significance of calcium pyrophosphate crystals in the synovial fluid of arthritic patients: the ‘pseudogout syndrome’. II Identification of crystals. Ann. Intern. Med., 56(56): 738–745. doi:10.7326/0003-4819-56-5-738.
- 2. Žitňan D., Sit’Aj Š. (1963) Chondrocalcinosis articularis. I. Clinical and radiological study. Ann. Rheum. Dis., 22: 142–152.
- 3. Zhang W., Doherty M., Bardin T. et al. (2011) European League Against Rheumatism recommendations for calcium pyrophosphate deposition. I. terminology and diagnosis. Ann. Rheum. Dis., 70: 563–570.
- 4. Higgins P.A. (2016) Gout and pseudogout. JAAPA, 29(3): 50–2.
- 5. Kleiber Balderrama C., Rosenthal A.K., Lans D. et al. (2017) Calcium Pyrophosphate Deposition Disease and Associated Medical Comorbidities: A National Cross-Sectional Study of US Veterans. Arthritis Care Res. (Hoboken), 69(9): 1400–1406.
- 6. Neame R.L., Carr A.J., Muir K. et al. (2003) UK community prevalence of knee chondrocalcinosis: evidence that correlation with osteoarthritis is through a shared association with osteophyte. Ann. Rheum. Dis., 62(6): 513–8.
- 7. Rosenthal A.K., Ryan L.M. (2016) Calcium Pyrophosphate Deposition Disease. N. Engl. J. Med., 30; 374(26): 2575–84. doi: 10.1056/NEJMra1511117
- 8. Коваленко В.М., Шуба Н.М., Казимирко В.К. та ін. (2013) Національний підручник з ревматології. За ред. В.М. Коваленка, Н.М. Шуби. 678 с.
- 9. Rosenthal A.K. (2018) Basic calcium phosphate crystal-associated musculoskeletal syndromes: an update. Curr. Opin. Rheumatol., 30: 168–172.
- 10. Salcion A., Kozyreff-Meurice M., Richette P. et al. (2015) Assessment of the Ultrasonography’s Efficiency as a Diagnostic Tool for Calcium Pyrophosphate Crystal Deposition Disease Annals of the Rheumatic Diseases, 74: 538.
- 11. Filippou G., Scirè C.A., Adinolfi A.A. (2018) Identification of calcium pyrophosphate deposition disease (CPPD) by ultrasound: reliability of the OMERACT definitions in an extended set of joints-an international multiobserver study by the OMERACT Calcium Pyrophosphate Deposition Disease Ultrasound Subtask Force. Ann. Rheum. Dis.,77(8): 1194–1199.
- 12. Sirotti S. et al. (2023) Development and validation of an OMERACT ultrasound scoring system for the extent of calcium pyrophosphate crystal deposition at the joint level and patient level.» The Lancet Rheumatology. doi.org/10.1016/S2665-9913(23)00136-4.
- 13. Abhishek A., Tedeschi S.K., Pascart T. et al. (2023) The 2023 ACR/EULAR Classification Criteria for Calcium Pyrophosphate Deposition Disease. Arthritis Rheumatol., 75: 1703–1713. doi.org/10.1002/art.42619.
- 14. Zhang W., Doherty M., Pascual E. (2011) EULAR recommendations for calcium pyrophosphate deposition. Part II: management. Ann. Rheum. Dis., 70(4): 571–5. doi: 10.1136/ard.2010.139360.
- 15. Stack J., McCarthy G. (2021) Calcium pyrophosphate deposition (CPPD) disease — Treatment options. Best Pract. Res. Clin. Rheumatol., 35(4): 101720. doi: 10.1016/j.berh.2021.101720.
- 16. Cipolletta E., Di Matteo A., Scanu A. et al. (2020) Biologics in the treatment of calcium pyrophosphate deposition disease: systematic literature review. Clin. Exp. Rheumatol., 38 (5): 1001–1007.
- 17. Klück V., Jansen T.L.T.A, Janssen M. et al. (2020) Dapansutrile, an oral selective NLRP3 inflammasome inhibitor, for treatment of gout flares: an open-label, dose-adaptive, proof-of-concept, phase 2a trial Lancet Rheumatol, 2 (5):e270-e280
- 18. Finckh A., Mc Carthy G.M., Madigan A. et al. (2014) Methotrexate in chronic-recurrent calcium pyrophosphate deposition disease: No significant effect in a randomized crossover trial Arthritis Res. Ther., 16 (1).
- 19. Nasi S., So A., Combes C. et al. (2016) Interleukin-6 and chondrocyte mineralisation act in tandem to promote experimental osteoarthritis. Ann. Rheum. Dis., 75 (7): 1372–1379.
- 20. Latourte A., Ea H.-K., Frazier A. et al. (2020) Tocilizumab in symptomatic calcium pyrophosphate deposition disease: a pilot study Ann. Rheum. Dis, 79 (8): 1126 LP–1128.
- 21. Rothschild B., Yakubov L. (1997) Prospective 6-month, double-blind trial of hydroxychloroquine treatment of CPDD. Compr. Ther., 23: 327–331.
- 22. Doherty M., Dieppe P. (1981) Effect of intra-articular YTTRIUM-90 on chronic pyrophosphate arthropathy of the knee. Lancet, 318 (8258): 1243–1246.
- 23. Soriano F., Campana V., Moya M. et al. (2006) Photobiomodulation of pain and inflammation in microcrystalline arthropathies: experimental and clinical results. Photomed. Laser. Surg., 24 (2): 140–150.
- 24. Bashir M., Sherman K.A., Solomon D.H. et al. (2023) Cardiovascular Disease Risk in Calcium Pyrophosphate Deposition Disease: A Nationwide Study of Veterans. Arthritis Care Res. (Hoboken), 75(2): 277–282. doi: 10.1002/acr.24783.
Адреса для листування:
А.С. Крилова
04112, Київ, вул. Дорогожицька, 9
Національний університет охорони здоров’я України імені П.Л. Шупика
Е-mail: revm@nuozu.edu.ua

Leave a comment