ЩО КАЖУТЬ ЕКСПЕРТИ З ФРАНЦІЇ ПРО ОСТЕОАРТРИТ?
Резюме. У рамках VIII Національного конгресу ревматологів України, який тривав 26–29 жовтня 2021 р., відбувся виступ вченого світового рівня — Франсуа Рану (François Rannou), доктора медичних наук, професора медицини Університету Декарта (University Paris Descartes), співавтора рекомендацій ESCEO та керівника відділу фізичної та реабілітаційної медицини лікарні Кошен (Cochin Hospital), Париж, Франція, який представив доповідь «Лікування остеоартриту: від рекомендацій до щоденної практики», фокусуючи увагу на останніх світових рекомендаціях.
 УДК 616.72-002
УДК 616.72-002
DOI: 10.32471/rheumatology.2707-6970.86.16645
Епідеміологія остеоартриту
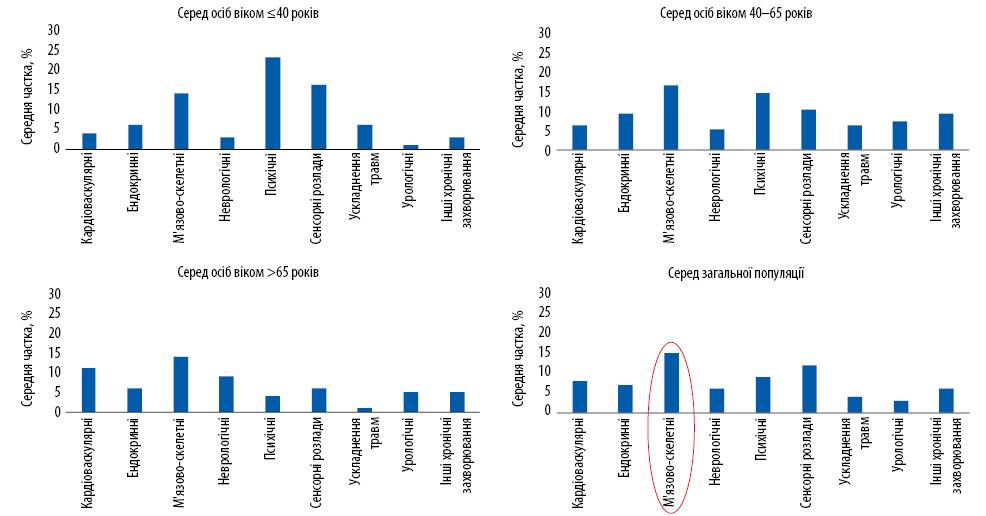
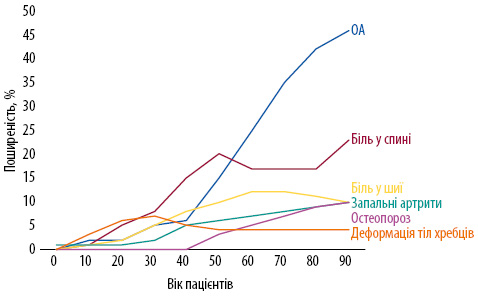
Сучасні епідеміологічні дані свідчать, що з усіх найбільш поширених хронічних захворювань людини патологія скелетно-м’язової системи — головна причина інвалідизації населення, особливо серед осіб віком 40–65 та ≥65 років (рис. 1) [1]. Результати дослідження C. Palazzo та співавторів (2014), метою якого було визначити, яка саме патологія в контексті скелетно-м’язової системи найбільш часто призводить до інвалідизації населення, продемонстрували, що серед усієї патології скелетно-м’язової системи саме остеоартрит (ОА) є найчастішою причиною інвалідизації, на який припадає 50% випадків, тоді як на біль у спині — 20%, біль у шиї — 10%, запальні артрити та остеопороз і деформації тіл хребців по 8% (рис. 2) [2]. Якщо вважати, що біль у спині — це також ОА, отже, ключовою причиною інвалідизації населення є саме ОА.
ОА — інволютивне захворювання, яке хоча і не є гострою патологією, асоційованою зі значним ризиком смерті порівняно з інсультом та інфарктом міокарда, однак значно впливає на якість життя хворих, що несе значний економічний тягар на систему охорони здоров’я. Так, у 2014 р. оприлюднені результати дослідження P. Bertin та F. Rannou, які визначили, що кожного року система охорони здоров’я Франції витрачає близько 3,6 млрд євро на лікування ОА, з яких 80% збитків пов’язано з хірургічним лікуванням — тотальним ендопротезуванням суглобів [3]. Враховуючи той факт, що сьогодні відмічають значне збільшення кількості осіб похилого і старечого віку та наявну епідемію ожиріння, відсутність відповідного лікування ОА до 2030 р. призведе до зростання частоти ендопротезування на 673% для колінного та на 174% для кульшового суглобів і ще більших економічних збитків [4].
Патофізіологічні аспекти терапії ОА та «червоні прапорці»
Сучасні стратегії лікування ОА базуються на модифікації факторів, що беруть участь у патофізіології захворювання, які представлені генетичними, метаболічними, запальними, механічними та асоційованими з віком факторами. Вік, стать та генетика — фактори, на які неможливо вплинути. Саме тому ключова стратегія лікування ОА полягає у впливі на модифікуючі фактори, які включають механічне навантаження, запалення і метаболічні фактори та ожиріння, що потребує застосування як фармакологічних, так і нефармакологічних підходів до лікування.
На сучасному етапі понад 95% пацієнтів з ОА знаходяться на рівні первинної терапії, тобто цих пацієнтів лікує сімейний лікар. Міжнародна ревматологічна рада (International Rheumatologic Board — IRB) у складі 10 експертів з трьох континентів розробила консенсус щодо діагностики ОА на первинній ланці медичної допомоги, в яких надані критерії потреби в експертній думці — направлення до фахівців вторинної ланки (лікарів ортопедів-травматологів та ревматологів) [5]. Рекомендації надані для трьох найбільш поширених локалізацій ОА: кульшового, колінного та кисті рук. Ключовою думкою гайдлайну є визначення, коли саме та за яких умов пацієнту необхідно звернутися до експерта. Так, кожен уражений ОА суглоб можна оцінити за допомогою наступних діагностичних факторів: біль у суглобі, вік >50 років, наявність звуженої суглобової щілини та/або остеофіту(-ів) на рентгенограмі.
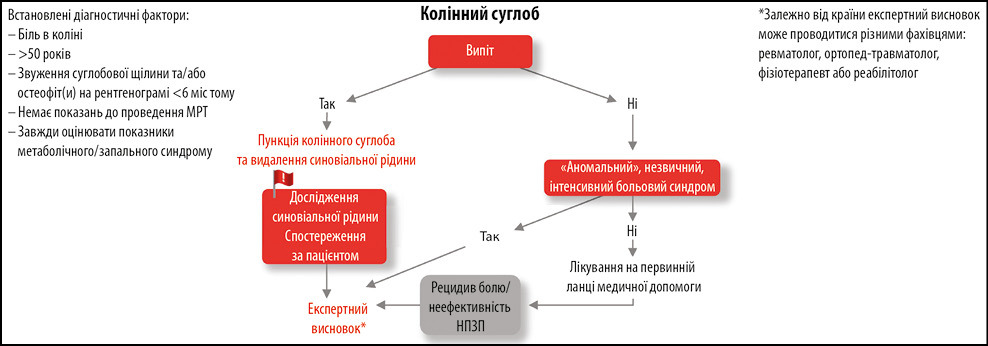
Вважатимемо, що до нас звернувся пацієнт з больовим синдромом у колінному суглобі віком старше 50 років, в якого на рентгенограмі наявне звуження суглобової щілини протягом останніх 6 міс. У такому випадку немає показань до проведення магнітно-резонансної томографії (МРТ). Алгоритм діагностики ОА колінного суглоба на первинній ланці медичної допомоги починається з визначення наявності у пацієнта можливого випоту в колінному суглобі, який і є ключовим показанням до дослідження синовіальної рідини та направлення до відповідного фахівця вторинної ланки (хірург ортопед-травматолог, лікар-ревматолог) (рис. 3). Також потреба у експертній оцінці визначається наявністю у пацієнта аномального, незвичного, інтенсивного больового синдрому в колінному суглобі. Отже, якщо випоту та аномального болю немає, менеджмент пацієнта може здійснювати сімейний лікар.
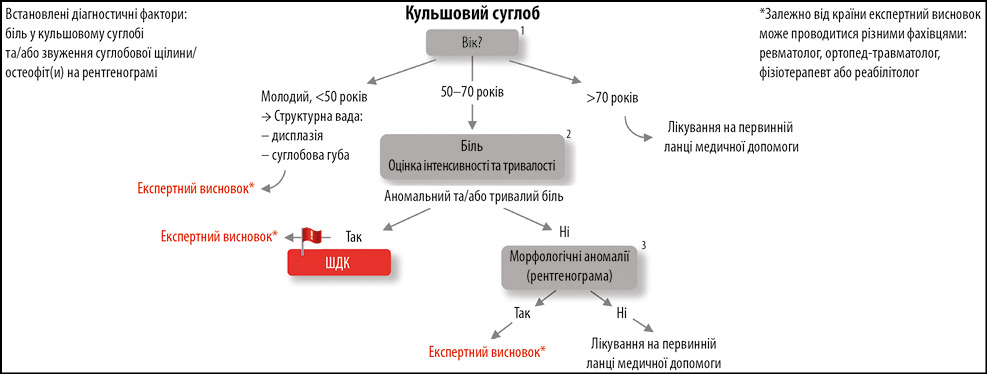
Алгоритм діагностики пацієнтів з ОА кульшового суглоба є схожим з ОА колінного суглоба, однак ключовим моментом в цьому випадку є не наявність випоту в кульшовому суглобі, а вік пацієнта (рис. 4). Так, пацієнти старшої вікової групи (>70 років) повинні отримувати терапію на первинній ланці медичної допомоги, тоді як ключовим моментом менеджменту осіб віком 50–70 років з ОА, як і при ОА колінного суглоба, є наявність болю. Якщо больовий синдром є помірним, то можна лікувати на первинній ланці медичної допомоги. Проте якщо у пацієнта наявні будь-які морфологічні аномалії на рентгенограмі або аномальний біль, необхідна експертна думка.
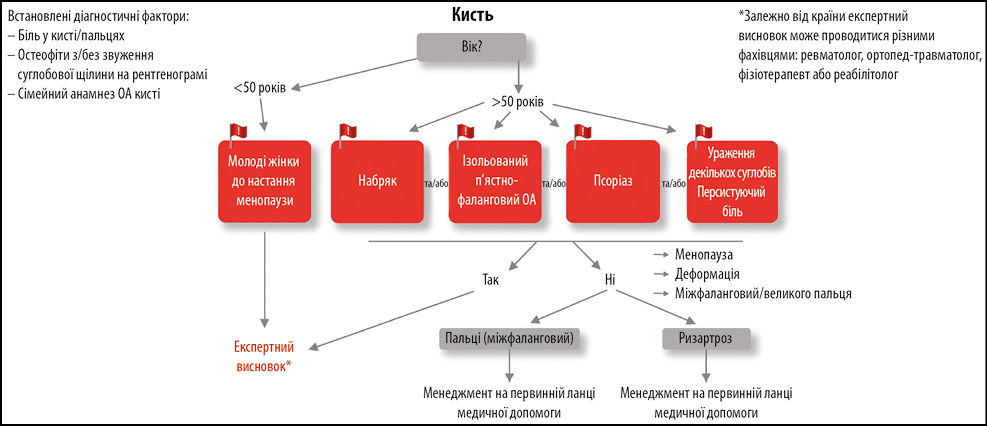
Менеджмент пацієнтів з ОА кисті є схожим з алгоритмом при ОА кульшового суглоба і також починається з оцінки віку пацієнта (рис. 5). Так, пацієнти віком <50 років з больовим синдромом у кисті, будь-якою скутістю та наявністю на рентгенограмі звуження суглобової щілини потребують експертної оцінки. Менеджмент осіб більш старшої групи (>50 років) залежить від наявності так званих червоних прапорців, які включають наявність набряку, ізольованого ураження п’ястно-фалангових суглобів, супутнього псоріазу та ураження декількох суглобів, в такому випадку пацієнт потребуватиме експертної оцінки.
Концепт ефективності та побічних ефектів терапії
Баланс між ефективністю лікування та розвитком побічних ефектів є вкрай важливим. Відповідно до сучасних рекомендацій ключовим моментом при лікуванні ОА є безпека терапії, зокрема розвиток небажаних явищ, асоційованих з артеріальною гіпертензією, цукровим діабетом, проблемами з боку серцево-судинної системи та ін. Сучасні дані свідчать, що застосування НПЗП асоційоване з низкою побічних ефектів, які включають шлунково-кишкову кровотечу, перфорацію, ниркову недостатність, кардіотоксичність (серцево-судинні ускладнення, включно з інфарктом міокарда). Враховуючи ризики, асоційовані із застосуванням НПЗП, безпека терапії — ключовий фактор при виборі терапії, яка повинна бути ефективною, безпечною та не супроводжуватися розвитком побічних ефектів. На сьогодні безпечна терапія ОА представлена нефармакологічною терапією, топічними препаратами та повільнодіючими препаратами, що структурно модифікують хрящ (symptomatic slow acting drugs for osteoarthritis — SYSADOA), зокрема пероральним хондроїтин сульфатом. Перелічені методи є більш безпечними і демонструють високий профіль ефективності. Таким чином, менеджмент пацієнтів з ОА передбачає проведення оцінки співвідношення ефективності терапії та ризиків розвитку побічних ефектів.
Підсумовуючи першу частину доповіді, Ф. Рану зазначив:
- ОА — основна причина інвалідизації не лише у Франції, а в усьому світі;
- стратегії терапії базуються на модифікації факторів, які залучені в патофізіологічний процес розвитку ОА;
- перший крок терапії цих змін полягає в оцінці балансу ефективності та небажаних ефектів, яка дозволяє визначити подальшу стратегію лікування пацієнта з ОА і з супутньою патологією, що представлена нефармакологічною терапією, топічними препаратами або SYSADOA (пероральний хондроїтин сульфат).
Сучасні рекомендації щодо менеджменту пацієнтів з ОА
У 2019 р. оприлюднені оновлені рекомендації щодо менеджменту ОА колінного суглоба Європейського товариства з клінічних та економічних аспектів остеопорозу (European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases — ESCEO), фокус яких стосувався безпеки терапії [6]. ОА — хронічне прогресуюче захворювання, що не пов’язана зі смертністю, цей факт дає можливість підбирати терапію, базуючись на ефективності та профілі безпеки препаратів.
В оновлених рекомендаціях представлений 4-етапний алгоритм лікування ОА колінного суглоба та включає базові принципи, які відносяться як до вузьких спеціалістів, так і сімейних лікарів та стосуються загальних рекомендацій (освіта пацієнта, зменшення маси тіла та фізичне навантаження) (рис. 6).

Перший крок терапії включає базове лікування, яке представлене застосуванням SYSADOA, зокрема рецептурних хондроїтин сульфату та/або глюкозамін сульфату, та в разі потреби парацетамолу. Глюкозамін сульфат не зареєстрований у Франції, тому ми його не застосовуємо. При цьому в оновленому гайдлайні вперше зменшена значущість парацетамолу при лікуванні ОА. Його рекомендують призначати лише як додатковий засіб при збереженні клінічної симптоматики на тлі прийому SYSADOA, відомих також як хондропротектори, тоді як в минулі роки лікування ОА рекомендувалося розпочинати саме з парацетамолу. Така зміна фокусу лікування пов’язана з тим, що в останнє десятиліття збільшилася кількість доказів наявності у парацетамолу небажаних побічних ефектів.
При збереженні симптомів ОА колінного суглоба, незважаючи на призначену терапію, рекомендовано застосування топічних НПЗП.
Якщо після застосування терапії 1-ї лінії симптоми ОА зберігаються, рекомендовано перейти на 2-й крок лікування, який передбачає лікування із залученням фахівців вторинної ланки — ревматологів. Терапія 2-ї лінії характеризується застосуванням пероральних НПЗП залежно від профілю гастроінтестинального/кардіоваскулярного або ниркового ризику пацієнта. Якщо симптоми ОА зберігаються, рекомендовано внутрішньосуглобове введення глюкокортикостероїдів та гіалуронової кислоти.
При збереженні симптомів рекомендовано перейти на 3-й крок терапії, який представлений застосуванням опіоїдів або дулоксетину. І хоча ESCEO рекомендують призначення коротких курсів слабких опіоїдів пацієнтам з ОА, цей варіант лікування не схвалений в деяких країнах, зокрема у Франції, оскільки асоціюється з розвитком залежності. Останній крок лікування включає залучення ортопедів-травматологів та передбачає проведення тотального/часткового ендопротезування пацієнтам з кінцевою стадією ОА.
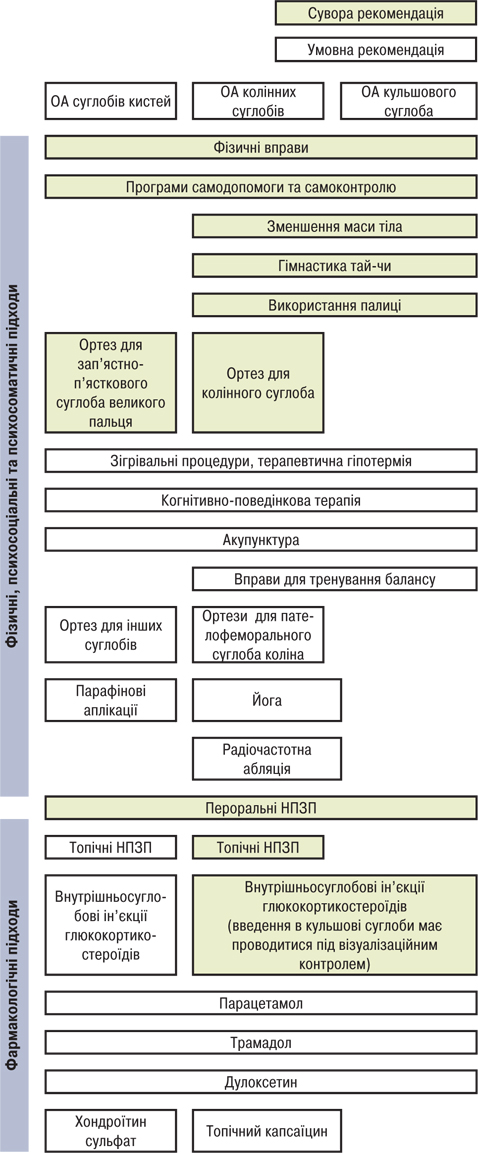
У 2019 р. було оприлюднено гайдлайн ACR щодо менеджменту пацієнтів з ОА кистей, колінного та кульшового суглобів [7]. Однак на відміну від ESCEO, ACR не поділяють лікування залежно від ланки медичної допомоги, рекомендації призначені як для лікаря загальної практики, так і ревматологів та включає застосування пероральних НПЗП, топічних засобів, глюкокортикостероїдів та хондроїтин сульфат єдиний з усіх SYSADOA (рис. 7). Ще один гайдлайн, який заслуговує уваги, це рекомендації Європейської антиревматичної ліги (European League Against Rheumatism — EULAR) стосовно терапії ОА кистей [8], відповідно до яких хондроїтин сульфат — єдиний хондропротектор, який рекомендується пацієнтам з ОА суглобів кистей та може призначатися для зменшення вираженості болю і покращення функції кистей.
 Далі Ф. Рану навів власний досвід фармакологічного лікування ОА незалежно від ураженого суглоба, який передбачає два підходи: короткострокову та тривалу терапію. Короткострокова терапія показана для лікування гострих (запальних) симптомів ОА та включає застосування пероральних або топічних анальгетиків та НПЗП. Тривала терапія рекомендована пацієнтам із хронічними симптомами захворювання та передбачає застосування пероральних SYSADOA (хондроїтин сульфат) та внутрішньосуглобові ін’єкції гіалуронової кислоти. Параметри, які впливають на вибір фармакологічного лікування при ОА, включають фенотип (гостра або хронічна фаза), локалізацію ОА, вік пацієнта, наявність супутніх захворювань та потенційні молекули, які викликають звикання (залежність від опіоїдів).
Далі Ф. Рану навів власний досвід фармакологічного лікування ОА незалежно від ураженого суглоба, який передбачає два підходи: короткострокову та тривалу терапію. Короткострокова терапія показана для лікування гострих (запальних) симптомів ОА та включає застосування пероральних або топічних анальгетиків та НПЗП. Тривала терапія рекомендована пацієнтам із хронічними симптомами захворювання та передбачає застосування пероральних SYSADOA (хондроїтин сульфат) та внутрішньосуглобові ін’єкції гіалуронової кислоти. Параметри, які впливають на вибір фармакологічного лікування при ОА, включають фенотип (гостра або хронічна фаза), локалізацію ОА, вік пацієнта, наявність супутніх захворювань та потенційні молекули, які викликають звикання (залежність від опіоїдів).
Стратегії лікування хронічного ОА, незалежно від ураженого суглоба:
- анальгезивна терапія (НПЗП);
- SYSADOA per os та внутрішньосуглобові ін’єкції гіалуронової кислоти;
- специфічне немедикаментозне лікування з метою модуляції навантаження на симптомний суглоб, включно з впливом на масу тіла, неспецифічне немедикаментозне лікування з метою покращення загального стану пацієнта, контроль маси тіла.
Таким чином, ОА — основна причина інвалідизації осіб в усьому світі. 1-м кроком при його лікуванні є оцінка супутніх захворювань та пошук найкращого балансу стосовно ефективності лікування та розвитку небажаних явищ. Фармакологічна терапія повинна призначатися після оцінки супутньої патології, наявної у пацієнта. Сучасні дані демонструють, що найкращий баланс між ефективністю терапії та ризиком розвитку побічних ефектів демонструють SYSADOA, зокрема пероральний хондроїтин сульфат, який є ефективним препаратом при лікуванні ОА, що має хороший профіль безпеки.
Після завершення своєї доповіді Ф. Рану відповів на декілька важливих питань, які наведено нижче.
― Покроковий алгоритм менеджменту пацієнтів з ОА, зазначений в рекомендаціях ESCEO, пов’язаний із клінічними симптомами чи зі стадією захворювання?
— Покроковий алгоритм створений з метою організації надання медичної допомоги пацієнтам з ОА і це не стосується проблеми тяжкості патології. Зрозуміло, що близько 80% пацієнтів з ОА на 1-му кроці не відмічатимуть тяжких симптомів захворювання та перебуватимуть на рівні первинної терапії, тоді як далі, на 2-й крок, підуть пацієнти з більш тяжкими симптомами, які потребують залучення фахівців вторинної ланки. Таким чином, незважаючи на те, що покроковий алгоритм є перш за все простою схемою для організації надання медичної допомоги, він також певною мірою є структурою відповідно до тяжкості перебігу ОА. Так, на 1-му кроці алгоритму буде наявна значно менша кількість пацієнтів з тяжкими симптомами ОА порівняно з 4-м кроком.
― Коли до терапії необхідно додавати SYSADOA?
— Безперечно, у клінічній практиці може існувати два різні варіанти перебігу ОА: гострі та хронічні симптоми. Перша ситуація, це коли пацієнт перебуває в гострій фазі патології, в нього наявний набряк, обмеження руху суглоба, можливо навіть наявний синовіїт. І в такому разі зазвичай значне локальне запалення, що потребує застосування НПЗП, спочатку топічних, і при їх недостатній ефективності — системних препаратів. Проте застосування НПЗП необхідно обмежити протягом короткого періоду, зазвичай протягом не більше 5–7 днів. Також важливо пояснити пацієнту, що якщо через 3 міс в нього знову з’являться симптоми запалення (набряк, біль), необхідно застосовувати топічні НПЗП ще протягом 2–3 днів. При недостатній ефективності топічних препаратів рекомендовано протягом 2–3 днів застосовувати системні НПЗП. Окрім того, вкрай важливо проводити оцінку пацієнта стосовно наявності в нього супутньої патології (хронічні захворювання нирок, шлунково-кишкового тракту або серцево-судинної системи), і якщо така наявна, такому пацієнту показані лише топічні НПЗП, тоді як системні протипоказані.
Друга ситуація включає пацієнта із хронічними симптомами ОА та характеризується застосуванням SYSADOA та гіалуронової кислоти. Якщо через 1–2 міс після початку терапії пацієнт не скаржиться на симптоми ОА та відзначає покращення функціональної активності, значить, лікування підібрано правильно, і терапію можна продовжити. Проте якщо пацієнт не відзначає жодних змін щодо зменшення вираженості болю та покращення функції, в такому випадку потрібно змінювати лікування. Ця стратегія стосується як фармакологічної, так і нефармакологічної терапії ОА, і її основною філософією є «спробувати і подивитися». Обмеженням такої терапії є те, що деякі лікарські засоби не можна застосовувати протягом тривалого періоду, якщо неможливо провести оцінку ефективності у конкретного пацієнта.
― У Франції наявний оригінальний препарат хондроїтину сульфату, тоді як в Україні є значна кількість дієтичних добавок та препаратів глюкозаміну і хондроїтину сульфату та інших молекул. Яким SYSADOA та яким формам введення особисто ви надаєте перевагу — внутрішньом’язовому введенню чи таблетованим формам?
— В Україні та в деяких інших країнах (Румунія, Росія) застосовують внутрішньом’язові форми хондроїтин сульфату, проте у Франції це не прийнято. У Франції дотримання офіційних рекомендацій вкрай важливе. Тому що пацієнти можуть попросити вас обґрунтувати, чому ви призначили або не призначили терапію згідно з офіційними рекомендаціями. Особисто я надаю перевагу пероральним формам хондроїтин сульфату (Структум), які є виключно лікарським препаратом.
Що стосується якості препаратів, то в останні роки з’явилися дані стосовно того, що певні дієтичні добавки мають величезні проблеми щодо якості. Саме тому дуже важливим стосовно ефективності та безпеки терапії є застосування препаратів, які є лікарським препаратом. І коли ми говоримо про купівлю препаратів в мережі Інтернет або інших джерелах, окрім аптек, важливо розуміти, що це несе певні ризики, тому особисто я проти цього і завжди пояснюю своїм пацієнтам важливість придбання саме лікарських препаратів.
Список використаної літератури
- 1. Palazzo C., Ravaud J.-F., Trinquart L. et al. (2012) Respective Contribution of Chronic Conditions to Disability in France: Results from the National DisabilityHealth Survey. PLOS ONE, 7(9): e44994.
- 2. Palazzo C., Ravaud J.F., Papelard A. et al. (2014) The burden of musculoskeletal conditions. PLoS One, 9(3): e90633. doi:10.1371/journal.pone.0090633.
- 3. Bertin P., Rannou F., Grange L. et al. (2014) Annual Cost of Patients with Osteoarthritis of the Hip and Knee in France. J. Musculoskel. Pain, 22(4): https://doi.org/10.3109/10582452.2014.937550.
- 4. Kurtz S., Ong K., Lau E. et al. (2007) Projections of primary and revision hip and knee arthroplasty in the United States from 2005 to 2030. J. Bone Joint Surg. Am., 89(4): 780–785. doi: 10.2106/JBJS.F.00222.
- 5. Martel-Pelletier J., Maheu E., Pelletier J.P. et al. (2019) A new decision tree for diagnosis of osteoarthritis in primary care: international consensus of experts. Aging Clin. Exp. Res., 31(1): 19–30. doi: 10.1007/s40520-018-1077-8.
- 6. Bruyèreab O., Honvoab G., Veronesec N. et al. (2019) An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO). Semin. Arthritis Rheum., 49(3): 337–350. doi: 10.1016/j.semarthrit.2019.04.008.
- 7. Kolasinski S.L., Neogi T., Hochberg M.C. et al. (2020) 2019 American College of Rheumatology/Arthritis Foundation Guideline for the Management of Osteoarthritis of the Hand, Hip, and Knee. Arthrit. Care Res., 72(2): 149–162.
- 8. Kloppenburg M., Féline Pb.K., Blanco F.J. et al. (2018) 2018 update of the EULAR recommendations for the management of hand osteoarthritis. Ann. Rheum. Dis., 78(1): 16–24.
Анна Хиць,
редакція журналу «Український медичний часопис»
Вперше опубліковано на сайті журналу «Український медичний часопис» (www.umj.com.ua)

Leave a comment