Ризендронат у лікуванні остеопорозу: фармакологічний профіль, клінічна ефективність, переносимістьі безпека
Резюме. У статті узагальнено результати досліджень щодо застосування ризендронату в лікуванні остеопорозу. Багаточисленні клінічні дослідження продемонстрували ефективність ризендронату у зниженні ризику хребцевих, позахребцевих переломів і переломів стегнової кістки. Ризендронат виявився ефективним при постменопау-зальному та сенільному остеопорозі, при остеопорозі у чоловіків та при глюкокортикоїд-індукованому остеопорозі. Ефект ризендронату зберігається впродовж 7 років. Доведена також хороша переносимість і безпека препарату.
Остеопороз — багатофакторне полігенне захворювання скелета, що становить найпоширенішу форму метаболічних остеопатій. Переломи кісток — наслідки нелікованого остеопорозу, серед яких найтяжчими є переломи шийки стегнової кістки, — визначають медичну і медико-соціальну значущість захворювання, в тому числі підвищення смертності та значні економічні втрати.
Кісткова тканина, попри уявну стабільність та інертність, є метаболічно активною, постійно оновлюючою системою. Упродовж життя індивідуума в ній постійно відбуваються цикли ремоделю-вання, що охоплюють два основних процеси: руйнування «старої» кістки, що визначається терміном «кісткова резорбція» та супроводжується руйнуванням і видаленням як мінеральної речовини,так і органічного матриксу з місць резорбції, та наступний процес формування нової кістки, що полягає у синтезі нового кісткового матриксу з його подальшою мінералізацією.
Порушення балансу між процесами кісткового ремоделювання, домінування кісткової резорбції над кісткоутворенням є центральною ланкою патогенезу остеопорозу. Як вважають, цей дисбаланс віддзеркалює порушення основних механізмів системної гормональної та місцевої (цитокінової) регуляції активності кісткових клітин у генетично схильних осіб. В умовах прогресуючого дефіциту естрогенів у пре- і, особливо, постменопаузальний період у жінок, сомато- і андропаузи у чоловіків, порушення кальцієвого обміну у відповідь на дефіцит вітаміну 0 і вторинного гіперпаратиреоїдизму у пацієнтів старечого і похилого віку, зменшення продукції осте-опротегерину, процес кісткової резорбції активізується, а формування нової кістки істотно гальмується і сповільнюється. Тому медикаментозна корекція порушень кісткового ремоделювання спрямована на відновлення балансу між процесами резорбції та кісткоутворення за допомогою препаратів, що, насамперед, гальмують надактивну кісткову резорбцію — антирезорбенти.
Серед чисельної групи антиостеопоротич-них препаратів найбільшу увагу привертають бісфосфонати (БФ) [2; 9]. Саме з ними пов’язаний безсумнівний прогрес у вивченні остеопорозу та підвищення ефективності його лікування. Переваги БФ полягають у вибірковій дії на кісткову тканину, найпотужнішій здатності підвищувати мінеральну щільність кісткової тканини (МЩКТ) серед усіх відомих на сьогодні антирезорбтивних засобів і в незначній частці побічних ефектів, ризик яких є суттєво нижчим порівняно з іншими препаратами [1; 2]. БФ розглядаються сьогодні як препарати першої лінії в лікуванні остеопорозу та інших остеопатій, що супроводжуються високою кістковою резорбцією.
Відкриття БФ та їх застосування для лікування остеопорозу пов’язане з ім’ям швейцарського фармаколога і патофізіолога Херберта Фляйша, який разом зі своїми співробітниками у середині 60-х років ХХ ст. виявив в організмі речовину неорганічної будови — пірофосфат, що активно зв’язувався із солями кальцію, зокрема з мінеральним компонентом кістки — гідроксиапатитом [9]. При цьому він порушував утворення їх кристалів і перешкоджав розчиненню.
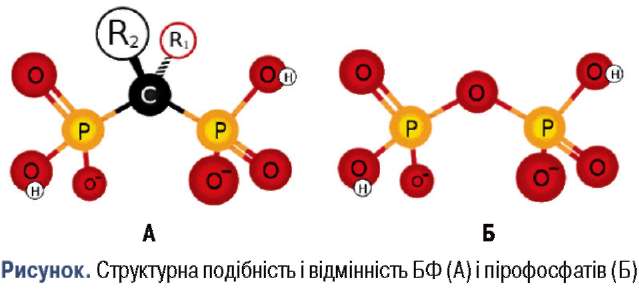
БФ є синтетичними аналогами пірофосфа-тів, стійкі до дії гідролітичних ферментів у травному тракті, у структурі яких центральний атом кисню (-О-) замінений на атом вуглецю (-С-) (рисунок). Така будова центральної частини молекули БФ зумовлює можливі-сть створення різноманітних структур на її основі за рахунок приєднання бокових ланцюгів і етерифікації кислотних фосфатних групувань. Відповідно до будови бокових ланцюгів БФ класифікуються на дві великі підгрупи [2; 18]:
1. БФ, що не містять аміногрупу і належать до І покоління (клодронат, тилудронат, етидронат).
2. БФ, що мають довгий боковий ланцюг із включенням аміно- чи ароматичних груп, належать до ІІ і ІІІ покоління (алендронат, памідронат, ризендронат, ібандронат, золендронат та ін.). їх називають амінобісфосфонатами у зв’язку із вмістом у їх
структурі атома (чи атомів) азоту, що забезпечує високу спорідненість до гідроксиапатиту і високу антирезорбтивну активність.
Наявність чи відсутність атома азоту у структурі БФ визначають абсолютно різні механізми впливу на кістку і кісткову резорбцію. Речовини, що утворюються внаслідок метаболізму в клітині безазотистих БФ, конкурують з аденозинтрифосфатом, порушуючи функцію мітохондрій, завдяки чому ініціюються процеси апоп-тозу в остеокластах. А механізми дії азотвмісних БФ пов’язані з гальмуванням процесу прениляції білків в остеокластах, що призводить до їх апоптозу.
БФ застосовують для лікування всіх типів і форм остеопорозу. Найбільш широко їх використовують в лікуванні постменопаузального остеопорозу. Серед БФ із пероральним прийомом найбільш переконливі дані, що стосуються їх антифрактурного ефекту, отримані для ризендронату, лікування яким супроводжувалося статистично вірогідним зменшенням кількості хребцевих переломів [4; 6] і переломів шийки стегнової кістки, зменшенням числа деформацій тіл хребців і сповільненням зниження зросту у жінок з постменопаузальним остеопорозом.
FDA (US Food and Drug Administration) затвердив до клінічного застосування три пероральних БФ: алендронат, ризендронат та ібандронат, які продемонстрували значне зниження ризику хребцевих переломів кісток. Також є дані про зниження ризику розвитку хребцевих переломів при внутрішньовенному застосуванні золендронату 1 раз на рік. Крім того, алендронат, ризендронат і золендронат підтвердили також значне зниження ризику переломів стегнової кістки. Задокументована також ефективність ризендронату і золендронату у запобіганні не-вертебральним переломам. Порівняльна характеристика БФ, подемонстрована в рандомізованих клінічних дослідженнях (РКД), наведена в табл.1.
ФАРМАКОЛОГІЧНИЙ ПРОФІЛЬ
Існує два головні показники, що зумовлюють різницю у клінічній ефективності БФ: подібність до гід-роксиапатиту (визначає радикал R1) зумовлює троп-ність до кістки і тривалість ефекту [23], а сила інгібування фарнезилдифосфатсинтетази (FPPS) у мевалоновому шляху утворення холестеролу (визначає радикал R2) — антирезорбтивний потенціал [28]. За силою впливу на FPPS БФ розподілилися таким чином: золендронат > ризендронат > ібандронат > алендронат [7]. Здатність зв’язуватися з гідроксиапатитом кістки також впливає на силу ан-тирезорбтивного ефекту. За цією властивістю БФ розподілилися так: золендронат > алендронат > ібандронат > ризендронат [16]. Таким чином, ризендронат є потужним антирезорбентом, при цьому не досить сильно зв’язується з гідроксиапатитом, як алендронат та ібандронат. Проте вважається, що саме такий фармакологічний профіль дозволяє ризендронату більш широко розповсюджуватися в кістці, здійснюючи потужний антирезорбтив-ний вплив [23].
Таблиця 1
Узагальнені дані щодо запобігання переломам кісток при застосуванні різних БФ (за: Р. Р.аскотт, 2008 [18])
| Зменшення переломів у проспективних рандомізованих дослідженнях, що визначені рентгенологічно | Ризендронат | Алендронат | Ібандронат | Золендронат |
| Вертебральні переломи | ||||
| 1 рік спостереження | 65% – VERT-NA – Harris, 1999 61% – VERT-MN – Reginster, 2000 |
н/д | Дані не розраховувалися – BONE — Chesnut, 2004 | 60% – HORIZON – Black, 2007 |
| 3 роки | 41% – VERT-NA- Harris, 1999 | 47% – FIT1 – Black, 1996 | 62% — BONE — Chesnut, 2004 | 70% – HORIZON – Black, 2007 |
| 4 роки | н/д | 44% – FIT 2 – Сummings, 1998 | н/д | н/д |
| Невертебральні переломи | ||||
| 3 роки | 39% – VERT NA
20% – HIP NS – 33% – VERT-MN – Reginster, 2000 |
NS – 20% – FIT1 – Black, 1996 | NS — 10% — BONE – Chesnut, 2004 | 25% – HORIZON – Black, 2007 |
| 4 роки | н/д | NS – 12% – FIT 2 – Cummings, 1998 | н/д | н/д |
| 5 років | 37% VERT MN | н/д | н/д | H/l |
| Переломи стегнової кістки | ||||
| Дослідження, в яких переломи стегнової кістки визначені як первинна кінцева точка | Є | Немає | Немає | Є |
| Переломи стегна | 60% НІР- McClung, 2001 –
Група 1 – пацієнти із встановленим остеопорозом 20% НІР, McClung, 2001 – Група 2 – пацієнти, які не були відібрані за низькою МЩК |
NS – 51% FIT 1- Black, 1996 NS – 21% FIT 2 – Cummings, 1998 | н/д | 41% – HORIZON – Black, 2007 |
н/д – немає даних; NS – not significant (дані статистично недостовірні). Дані для кожного препарату представлені частотою зниження ризику переломів, назвою дослідження, автором та роком дослідження.
Moжливo, саме ці властивості зумовлюють унікальні ефекти ризендронату на кістку, зокрема ранній ефективний вплив на хребцеві переломи кісток. Так, аналіз досліджень, в яких застосовували ризендронат, продемонстрував статистично вірогідний вплив на хребцеві переломи вже через б міс від початку терапії, що не спостерігалося при використанні інших БФ. Ці дані свідчать про більш ранній початок дії ризендронату на кістку порівняно з іншими БФ [22]. У подальшому було проведено
2 дослідження, що дали більше інформації щодо відмінностей ефектів різних БФ. Так, у дослідженні PROTECT вивчали ефективність кальцитоніну, алендронату і ризендронату у жінок. Пацієнти, у яких застосовували ризендронат, мали достовірно нижчу частоту невертебральних переломів кісток через б і 12 міс терапії порівняно з кальцитоніном і ален-дронатом [3G]. В іншому спостережному дослідженні REAL оцінювали відповідь пацієнтів на ризендронат і алендронат. Через б і 12 міс пацієнти, у яких застосовували ризендронат, мали вірогідно нижчу частоту переломів шийки стегнової кістки, ніж ті, які отримували алендронат [25].
КЛІНІЧНА ЕФЕКТИВНІСТЬ РИЗЕНДРОНАТУ
Ризендронат застосовують для лікування пацієнтів із постменопаузальним остеопорозом понад 1G років. Спочатку препарат застосовували щоденно перо-рально у формі таблеток по 5 мг; з 2GG2 р. – у формі таблеток по 35 мг 1 раз на тиждень; у 2GGB p. FDA ухвалив дозу 15G мг для щомісячного прийому.
Два дослідження VERT-North America (VERT-NA) i VERT-multinational (VERT-MN) продемонстрували, що у пацієнток із постменопаузальним остеопорозом ризендронат вірогідно підвищував MIHKr та знижував ризик хребцевих і позахребцевих переломів. Включенням до цього дослідження був один із двох критеріїв: два чи більше рентгенологічно підтверджених компресійних переломів хребців (TIV-LIV) та один хребцевий перелом зі зниженою MLUKr в поперековому відділі (T-score нижче -2,G SD). У 2 дослідженнях ризендронат підвищував MЩKT на 5,4-5,9% – в люм-бальному відділі та на 1,б-3,1% – в зоні шийки стегнової кістки [1G; 19]. В обох дослідженнях щоденний пе-роральний прийом ризендронату асоціювався зі зниженням відносного ризику вертебральних переломів (G,51 у VERT-NA та G,59 у VERT-MN) [1G; 19]. У дослідженні VERT-NA ризендронат знижував частоту вертебральних переломів на б5% впродовж 1-го року застосування та на 49% – через 3 роки, а також зменшував кількість невертебральних переломів на 39% впродовж
3 років. Впродовж 1 року застосування ризендрона-ту також достовірно зменшується кількість морфоме-трично виявлених переломів хребців.
Невертебральні переломи становлять найбільшу частку медичних витрат, пов’язаних з остео-
порозом. У 2008 р. опублікований spy phone calls app Кокранівський огляд, присвячений клінічній ефективності ризен-дронату у первинній та вторинній профілактиці ос-теопоротичних переломів кісток у жінок у постме-нопаузальний період [31]. Загалом в цей огляд було включено 7 РКД: 4 дослідження об’єднано та проаналізовано для встановлення відносного ризику невертебральних переломів кісток, що становив 0,80 (95% довірчий інтервал); 3 дослідження, що також були об’єднані, продемонстрували зниження ризику невертебральних переломів. Лише щодо ризендронату і золендронату задокументовано достовірні дані щодо зниження ризику невертебральних переломів та переломів шийки стегнової кістки у РКД тривалістю 3 роки [3; 13].
Як добре відомо, переломи шийки стегнової кістки асоціюються з високим ризиком смерті, інвалідністю, функціональною неспроможністю.
Дослідження HIP було першим рандомізованим контрольованим дослідженням з БФ, в якому перелом шийки стегнової кістки був визначений як основна кінцева точка. У ньому продемонстровано, що застосування ризендронату запобігає переломам шийки стегнової кістки у осіб похилого віку (70-79 років) із встановленим остеопорозом: 1,9% переломів кісток у групі ризендронату при 2-річному спостереженні та 3,2% — у групі плацебо [13]. Відзначимо, що у групі осіб віком старше 80 років, яка була відібрана на підставі схильності до падінь, а не низької МЩКТ, не встановлено достовірного зниження ризику переломів. Ці результати означають, що БФ, зокрема ризендронат, ефективний лише за умов низької МЩКТ та ніяк не пов’язані з ризиком падінь. Аналогічні дані відзначені також у Роттердамскому дослідженні, в якому оцінювали фактори ризику переломів шийки стегнової кістки у великій європейській когорті пацієнтів. Дослідження продемонструвало 10-разовезростання ризикупереломів у90-річ-них осіб порівняно з 50-річними, при цьому не тільки низька МЩКТ визначала ризик виникнення остеопо-ротичних переломів шийки стегнової кістки [21]. Результати досліджень наведено в табл. 2.
Таблиця 2
Ризендронат у рандомізованих контрольованих дослідженнях
Показник
| Назва РКД | VERT-NA | HIP |
| Тривалість | 3 роки | 3 роки |
| Кількість пацієнтів, п | 1641 | 9331 |
| Середній вік, років | 68 | 74 |
| Доза | 5 мг/добу | 2,5 і 5 мг/добу |
| ЭЕХД — поперековий відділ порівняно з плацебо | ↑ 4,3% | н/д |
| ЭЕХД — шийка стегнової кістки порівняно з плацебо | ↑ 2,8% | ↑ 3,4% |
| Хребцеві переломи порівняно з плацебо (% плацебо/терапія) | ↓ 41% (16/11) | н/д |
| Переломи шийки стегнової кістки порівняно з плацебо (% плацебо/терапія) | NS | ↓ 30% (3,9/2,8) |
| Невертебральні переломи порівняно з плацебо (% плацебо/терапія) | ↓ 39% (8,4/5,2) | ↓ 16% (11,2/9,4) |
н/д — немає даних; NS — not significant (дані статистично недостовірні).
Сьогодні приділяється значна увага безпеці БФ при їх тривалому використанні. Тим не менше, накопичено недостатньо даних щодо ефективності й безпеки деяких БФ, і це питання залишає багато неясностей. Ефективність БФ при тривалому (7 років) лікуванні продемонстрована для ризендронату. й.й. МеПвттот та співавтори (2004) [14] показали достовірне наростання МЩКТ у поперековому відділі хребта і в стегновій кістці через 7 років постійного прийому ризендронату у дозі 5 мг/добу порівняно з плацебо. Відзначимо, що частота вертебральних переломів через 6-7 років прийому ризендронату не відрізнялася від даних, отриманих через 4-5 років.
Відповідь на лікування добре контролюється в РКД, на відміну від ситуації з лікуванням загального населення. У США проаналізовано дані 35 537 жінок віком 45 років і старше, у яких застосовували терапію БФ — ризендронатом або алендронатом—упродовж 24 міс [26]. Лише 43% жінок дотримувалися рекомендацій лікаря і тільки 20% з них зберегли прихильність до лікування впродовж 2 років. Отже, результати досліджень щодо прихильності пацієнтів до лікування виглядають песимістично: до 50% жінок не приймають регулярно БФ [12]. Тому створення раціональних схем лікування із призначенням БФ 1 раз на тиждень або 1 раз на місяць виглядають більш привабливими щодо прихильності до лікування.
Саме тому, що ризендронат зберігає свою активність у кістці тривалий час, можливий розширений інтервал його дозування. Так, не встановлено відмінностей стосовно динаміки МЩКТ і маркерів кісткового обміну при щоденній (5 мг) і щотижневій (35 мг) дозі ризендронату [5]. Тому вважається, що інтермі-туючий прийом БФ за ефективністю не поступається щоденному прийому, але при ньому значно покращується комплаєнс між лікарем і пацієнтом.
У 2006 р. опубліковані дані однорічного дослідження застосування ризендронату (5 мг щоденно) порівняно з плацебо у чоловіків із встановленим остеопорозом. Застосування ризендронату асоціювалося з 60% зниженням ризику нових хребцевих переломів [20]. Також ризендронат продемонстрував свою дієвість стосовно запобігання переломам і лікування пацієінтів із глюкокортикоїд-індукованим остеопорозом. Так, у пацієнтів, які застосовували глюкокортикоїди у середніх або високих дозах та ризендронат у дозі 5 мг/добу впродовж 1 року, відзначено зменшення вертебральних переломів на 70% порівняно з плацебо [29].
Пацієнти з хворобою Альцгеймера також становлять велику групу підвищеного ризику переломів, що пов’язано з низькою кістковою масою і частими падіннями. Обстежено 500 жінок з середнім віком 77,7 року із встановленим діагнозом хвороби Альцгеймера. У всіх пацієнтів реєструвався виражений дефіцит вітаміну й і явища компенсованого гіперпаратиреоїдизму. Пацієнтів розподілили на 2 групи, в одній з яких отримували ризендронат, а в іншій — плацебо; в обох групах додатково отримували 1000 МО ергокальциферолу та 1200 мг елементарного кальцію впродовж 28 міс. У групі ризендронату було зареєстровано 5 переломів шийки стегнової кістки, а в контрольній групі — 24 [24].
БЕЗПЕКА РИЗЕНДРОНАТУ
Необхідно підкреслити, що терапія БФ є достатньо безпечною. При прийомі БФ всередину можуть виникати шлунково-кишкові розлади, проте більшість амі-нобісфосфонатів позбавлені цих небажаних ефектів і рідко можуть спричинити езофагіт. Внутрішньовенні інфузії амінобісфосфонатів здатні індукувати грипоподібний синдром із підвищенням температури тіла, міалгією та осалгією, але вираженість цих реакцій зменшується при подальших уведеннях препаратів. Рідшими ускладненнями є остеонекроз щелепи (ОНЩ) і увеїт. Ускладнення у вигляді фібриляцій передсердь описане у разі застосування золендронату і алендронату, але не для ризендронату.
У хворих на рак, яким внутрішньовенно вводили памідронат або золендронат у високих дозах, описано розвиток ОНЩ. Підкреслюється також, що це ускладнення більш властиве формам БФ для внутрішньовенного введення, що призначаються з метою лікування кісткових метастазів. Частота розвитку цього ускладнення є низькою (порядку 1 на 100 тис. випадків), а при застосуванні низьких доз (як при остеопорозі) ускладнення не виникають взагалі [15; 17]. При застосуванні БФ у низьких дозах, що використовуються при остеопорозі, не виявлено причинно-наслідкового зв’язку із розвитком ОНЩ.
H. Taggart та співавтори [27] проаналізували 9 РКД щодо частоти виникнення ускладнень з боку верхніх відділів травного тракту (ураження стравоходу і шлунка) у пацієнтів, які приймали ризендро-нат. Загалом за період дослідження у 60% пацієнтів в анамнезі були захворювання шлунково-кишкового тракту, у 38,7% — активна фаза хвороби, у 20,5% — застосовували антисекреторні препарати впродовж усього періоду спостереження. У 63% пацієнтів застосовували ацетилсаліцилову кислоту і нестероїд-ні протизапальні препарати. Явища ураження верхніх відділів травного тракту зафіксовано у 29,6% пацієнтів групи плацебо та у 29,8% пацієнтів групи ризендронату. В ендоскопічних дослідженнях, проведених за участю 349 пацієнтів, не виявили будь-яких відмінностей між дослідними групами.
ОНЩ визначається як наявність незагойної ділянки кістки щелепно-лицевого відділу впродовж 8 тиж за відсутності променевої терапії на цю ділянку в анамнезі.
При аналізі наукових досліджень, статей, оглядів, повідомлень за системою MEDLINE, Cochrane Database of Systematic Reviews, Cochrane Central Register of Controlled Trials та EMBASE за період з 1966 р. по вересень 2006 р. виявлено 11 публікацій і доповідей із зазначенням 26 випадків розвитку ОНЩ на тлі застосування БФ. Середній вік пацієнтів перевищував 60 років, серед них переважали жінки (лише у 3 чоловіків описані випадки ОНЩ); у12 з 15 описаних пацієнтів діагноз ОНЩ встановлений після та під час інвазивних стоматологічних втручань [17]. У 10 пацієнтів, в яких виявлено остеоне-кроз, проводився аналіз залежності між тривалістю застосування БФ та розвитком цього ускладнення, проте такої залежності не встановлено. Аналіз цих випадків дозволив виділити чинники відносного ри-
зику розвитку ОНЩ при тривалому застосуванні БФ: похилий вік пацієнтів (старше 60 років), жіноча стать, попереднє інвазивне стоматологічне лікування.
M. Etminan та співавтори (2008) [8] провели обстеження 87 837 пацієнтів похилого віку із серцево-судинним захворюваннями, які застосовували БФ. Відносний ризик розвитку ОНЩ серед усіх БФ становив 2,87. Відносний ризик для алендронату, ети-дронату і ризендронату становив, відповідно, 2,87 (95% CI 1,46-5,67), 2,43 (95% CI 1,05-5,62) та 3,34 (95% CI 1,04-10,67).
Проте, зважаючи на появу такого ускладнення, увага медичної громадськості зосередилася на реєстрації нових випадків розвитку ОНЩ та встановлення чинників ризику. Так, в багатьох країнах випущені рекомендації, що стосуються ретельного огляду пацієнтів, передусім онкологічного профілю, що тривало приймають БФ, а також виявлення факторів ризику в усіх пацієнтів, які з лікувальною метою застосовують БФ. Так, згідно із Canadian consensus practice guidelines for bisphosphonate associated osteonecrosis of the jaw (2008) [11], чинниками ризику розвитку ОНЩ є опромінення голови і шиї, травми щелеп, хвороби періодонта, місцеві онкологічні захворювання, хіміотерапія, застосування глюкокортикоїдної терапії, а також екстракція зубів у період прийому БФ. Високі дози БФ при внутрішньовенному введенні були визначені як найголовніший фактор ризику ОНЩ на відміну від низьких доз, які не виявили причинний зв’язок з цим ускладненням. Для всіх пацієнтів, які отримують терапію БФ, рекомендується припинення тютюнопаління, обмеження вживання алкоголю та підтримання належної гігієни порожнини рота.
Отже, існують численні клінічні дослідження, що продемонстрували ефективність ризендронату у зниженні ризику хребцевих, позахребцевих переломів і переломів шийки стегнової кістки у жінок постменопаузального віку, у чоловіків з остеопорозом та у жінок і чоловіків з глюкокортикоїд-індукованим остеопорозом. Антифрактурний ефект ризендронату зберігається впродовж 7 років, а саме застосування препарату добре переноситься [18]. Проведені дослідження довели ефективність і безпеку ризендронату при різних схемах дозування: щоденно, щотижнево та щомісячно, виявляючи однотипні зміни МЩКТ у різних ділянках скелета і маркерів кісткового ремоделювання. Висока ефективність, безпека, а також сприятливий фармакологічний профіль виправдовують широке використання ризендронату в клінічній практиці та дозволяють рекомендувати його до застосування в різних клінічних ситуаціях для профілактики і лікування різних типів і форм остеопорозу.
ЛІТЕРАТУРА
1. Головач І.Ю. (2009) Еволюція бісфосфонатів: сходження на вершину. Мистецтво лікування., 9-10: 68-74.
2. Поворознюк В.В. (1997) Бисфосфонатьі в профилактике и лечении остеопороза и его осложнений. Фармакол. вісн., 2: 18-22.
3. Black D.M., Delmas P.D., Eastell R. et al. (2007) Once yearly zolendronic acid for treatment of postmenopausal osteoporosis. N. Engl. J. Med., 356: 1809-1822.
4. Bock O., Felsenberg D. (2008) Bisphosphonates in the management of postmenopausal osteoporosis – optimizing efficacy in clinical practice. Clin. Interv. Aging., 3(2): 279-297.
5. Brown J.P., Kendler D.L., McClung M.R. et al. (2002) The efficacy and tolerability of risedronate once a week for the treatment of postmenopausal osteoporosis. Calcif. Tissue Int., 71: 103-111.
6. Drake M., Clarke B.L., Khosla S. (2008) Bisphosphonates: mechanism of action and role in clinical practice. Mayo Clin.Proc., 83(9):1032-1045.
7. Ebetino F.H., Francis M.D., Rogers M.J. et al. (1998) Mechanisms of action of etidronate and other bisphosphonates. Rev. Contemp. Pharm., 9: 233-243.
8. Etminan M., Aminzadeh K., Matthew I.R. et al. (2008) Use of oral bisphosphonates and the risk of aseptic necrosis: a nested case-control study. J. Rheumatol., 35: 691-695.
9. Fleisch H. (1997) Bisphosphonates in Bone Diseases. N.Y. -London: Academic Press, 1-83; 118-160.
10. Harris S.T., Watts N.B., Genant H.K. et al. (1999) Effects of risedronate treatment on vertebral and nonvertebral fractures in women with postmenopausal osteoporosis: a randomized controlled trial. Vertebral Efficacy with Risedronate Trial (VERT) Study Group. JAMA. 282: 1344-1352.
11. Khan A.A., Sandor G.K., Dore E., Morrison A.D. et al.
(2008) Canadian consensus practice guidelines for bisphosphonate associated osteonecrosis of the jaw. J. Rheumatol., 35(7): 1391-1397.
12. Lombas C., Hakim C., Zanchetta J.R. (2001) Compliance with alendronate treatment in an osteoporosis clinic. J. Bone Miner. Res., 15: 529.
13. McClung M.R., Geusens P., Miller P.D. et al. (2001) Effect of risedronate on the risk of hip fracture in elderly women. HIP Intervention Program Study Group. N. Engl. J. Med., 344: 333-340.
14. Mellstrom D.D., Sorensen O.H., Goema S. et al. (2004) Seven years of treatment with risedronate in women with postmenopausal osteoporosis. Calcif. Tissue Int., 75: 462-468.
15. Murad O.M., Arora S., Farag A.F., Guber H.A. (2007) Bisphosphonates and osteonecrosis of the jaw: a retrospective study. Endocr. Pract., 13(3): 232-238.
16. Nancollas G.H., Tang R., Phipps R.J. et al. (2006) Novel insights into actions of bisphosphonates on bone: differences in interactions with hydroxyapatite. Bone, 38: 617-627.
17. Pazianas M., Miller P., Blumentals W.A., Bernal M., Ko-thawala P. (2007) A review of the literature on osteonecrosis of the jaw in patients with osteoporosis treated with oral bisphosphonates: prevalence, risk factors, and clinical characteristics. Clin. Ther. 29(8): 1548-1558.
18. Rackoff P. (2009) Efficacy and safety of risedronate 150 mg once a month in the treatment of postmenopausal osteoporosis. Clin. Interv. Aging., 4: 207-214.
19. Reginster J., Minne H.W., Sorensen O.H. et al. (2000) Randomized trial of the effects of risedronate on vertebral fractures in women with established postmenopausal osteoporosis. Vertebral Efficacy with Risedronate Therapy (VERT) Study Group. Osteoporos Int., 11: 83-91.
20. Ringe J.D., Faber H., Farahmand P. et al. (2006) Efficacy of risedronate in men with primary and secondary osteoporosis: Results of a 1 year study. Rheumatol Int., 26: 427-431.
21. Rivadeneira F., Zillikens M.C., De Laet C.E. et al. (2007) Femoral neck BMD is a phone spy app strong predictor of hip fracture susceptibility in elderly men and women because it free essay sociology detects cortical bone instability: the Rotterdam Study. J. Bone Miner. Res., 22: 1781-1790.
22. Roux C., Seeman E., Eastel R. et al. (2004) Efficacy of risedronate on clinical vertebral fractures within six months. Curr. Med. Res. Opin., 20: 433-439.
23. Russell R.G.G. (2007) Determinants of structure-function relationships among bisphosphonates. Bone., 40 (2): 521-525.
24. Sato Y., Kanoko T., Satoh K. et al. (2005) The prevention of hip fracture with risedronate and ergocalciferol plus calcium supplementation in elderly women with Alzheimer disease: a randomized controlled trial. Arch. Intern. Med., 165: 1737-1742.
25. Silverman S.L., Watts N.B., Delmas P.D. et al. (2007) Effectiveness of bisphosphonates on nonvertebral fracture and hip fractures
in the first year of therapy: the risedronate and etidronate (REAL) cohort. Osteoporos Int., 18: 25–34.
26. Siris E.S., Harris S.T., Rosen C.J. et al. (2006) Adherence to bisphosphonate therapy and fracture rates in osteoporotic women: relationship to vertebral and nonvertebral fractures from 2 US claims databases. Mayo Clin. Proc., 81: 1013–1022.
27. Taggart H., Bolognese M.A., Lindsay R. et al. (2002) Upper gastrointestinal tract safety of risedronate: a pooled analysis of 9 clinicaltrials. Mayo Clin. Proc., 77: 262–270.
28. van Beck E., Lowik C., Que I. et al. (1996) Dissociation of binding and antiresorptive properties of hydroxybisphosphonates by substitution of the hydroxyl group with an amino group. J. Bone Miner. Res., 11: 1492–1497.
29. Wallach S., Cohen S., Reid D.M. et al. (2000) Effects if risedronate on bone density and vertebral fracture in patients on corticosteroid therapy. Calcif. Tissue Int., 67: 277–285.
30. Watts N.B., Worley K., Solis A. et al. (2004) Comparison of risedronate and alendronate relative to calcitonin for early reduction of nonvertebral fracture risk: results from a managed care administrative claims database. J. Manag. Care Pharm., 10: 142–151.
31. Wells G., Cranney A., Petersen J. et al. (2008) Risedronate for the primary and secondary prevention of osteoporotic fractures in postmenopausal women. Cochrane Database Syst. Rev., 23: CD 004523.
И.Ю. Головач
Резюме. В статье обобщены результаты исследований по применению ризендроната в лечении остеопороза. Мночисленные клинические исследования продемонстрировали эффективность ризендроната в снижении риска верте-бральных, невертебральныхпереломов и переломов бедренной кости. Ризендронат выявился эффективным при постменопаузальном и се-нильном остеопорозе, при остеопорозе у мужчин и при глюкокортикоид-индуцированном остеопорозе. Эффект ризендроната сохраняется в течение 7лет. Доведена также хорошая переносимость и безопасность препарата.
Ключевые buy thesis online слова: остеопороз, ризендронат. эффективность, безопасность, переломы.

Leave a comment