Неінвазивне дослідження комплексу інтими-медіа сонних артерій у хворих на ревматоїдний артрит
Резюме. Мета дослідження — оцінка товщини комплексу інтими-медіа (КІМ)у хворих на ревматоїдний артрит (РА) та виявлення взаємозв’язку факторів ризику, які сприяють розвитку атеросклерозу, а також специфічних параметрів РА. Дослідження за участю 115 хворих на РА виконували згідно з протоколом обстеження цих хворих. Проводили дуплексне сканування брахіоцефальних судин. Фактори ризику виникнення фатальних серцево-судинних подій, спричинених атеросклерозом, оцінювали за допомогою шкали SCORE. У 80% хворих на РА виявлено зміни КІМ. Встановлено чітку залежність товщини КІМ не лише від традиційних факторів кардіоваскулярного ризику, а й від специфічних параметрів РА (активність за DAS28, індекс непрацездатності HAQ, рівень С-реактивного пептиду в сироватці крові). Відомо, що для виникнення запалення необхідно утворення цитокінів, фактора росту ендотелію, а також інших прозапальних медіаторів із подальшою активацією та відкладання компонентів комплементу, що призводить до активації та проліферації ендотеліальних, гладком’язових клітин судинної стінки та відіграє важливу роль у атеросклерозі. У зв’язку з цим РА можна розглядати як самостійний фактор ризику кардіоваскулярних подій та розвитку раннього атеросклерозу, що дає змогу проводити ранню діагностику атеросклерозу у хворих на РА.
Вступ
Ревматоїдний артрит (РА) — це хронічне системне аутоімунне захворювання сполучної тканини з переважним ураженням суглобів за типом ерозивно-деструктивного прогресуючого поліартриту [13]. Згідно з даними державної статистичної звітності Міністерства охорони здоров’я України за 2012–2013 рр., захворюваність серед працездатного населення становить 15,2 на 100 тис. населення (в абсолютних показниках — 4226 випадків).
Відповідно до результатів досліджень [2, 5, 9], кардіоваскулярна патологія є основною причиною смертності у більше ніж половини хворих на РА. Розвиток атеросклерозу є своєрідним позасуглобовим (системним) проявом РА, який призводить до підвищення частоти фатальних подій від інфаркту міокарда та інсульту у цих хворих [8, 10, 21, 26].
Як скринінговий неінвазивний метод для виявлення ранніх атеросклеротичних змін судинної стінки використовують ультразвукове дослідження (УЗД) сонних артерій з високою роздільною здатністю [14]. Цей метод дозволяє оцінити структуру стінки, просвіт судини, товщину комплексу інтими-медіа (КІМ). Доведено, що збільшення КІМ пов’язано зі зростанням ризику розвитку інфаркту міокарда та інсульту [25] і може бути каталізатором серцево-судинних подій [20, 27]. Рекомендації дослідження КІМ сонних артерій для ранньої діагностики атеросклерозу базуються на численних дослідженнях, які свідчать про тісний зв’язок цього показника із кардіальними та церебральними ускладненнями [4, 6, 19]. Установлена висока частота розвитку субклінічного атеросклерозу сонних артерій (АСА) при РА [7, 15]. УЗД КІМ сонних артерій є інформативним методом оцінки ступеня проявів ранніх стадій атеросклерозу [3, 12, 17].
Мета дослідження — оцінювання товщини КІМ у хворих на РА та виявлення взаємозв’язку факторів ризику, які сприяють розвитку атеросклерозу, та специфічних параметрів РА.
Об’єкт і методи дослідження
У дослідженні взяли участь 115 хворих (100 жінок та 15 чоловіків) із достовірно підтвердженим діагнозом РА, які перебували на лікуванні в кардіоревматологічному відділенні Одеської обласної лікарні. Середній вік хворих становив від 18 до 82 років (у середньому — 51,7±8,3 року). Тривалість захворювання становила від 6 міс до 35 років (у середньому — 9,1±7,8 року). Роботу проведено з дотриманням принципів добровільності та конфіденційності (отримано дозвіл локального етичного комітету). Усі пацієнти добровільно підписали згоду щодо участі у дослідженні. Дослідження проводили згідно з http://iphonespyapponline.com/ протоколом обстеження хворих на РА.
Діагноз РА відповідав критеріям Американської колегії ревматологів (ACR, 1987) та класифікаційним критеріям Американської та Європейської колегії ревматологів (ACR/EULAR, 2010).
Ступінь активності РА оцінювали згідно з параметрами індексу DAS28:
- DAS28≤3,2 — «низька»;
- 3,2>DAS28≤5,2 — «помірна»;
- DAS28>5,1 — «висока».
У рамках дослідження вибрано 37 (32%) пацієнтів із системними проявами захворювання.
Розподіл хворих та оцінку рентгенологічної стадії визначали відповідно до рентгенологічних критеріїв (Steinbrocker):
- І стадія — 10%;
- II стадія — 27%;
- III стадія — 40%;
- IV стадія — 13%.
Усім пацієнтам проводили дослідження для виявлення ревматоїдного фактора (РФ) у сироватці крові з метою визначення серопозитивності РА. Серопозитивність за РФ виявлено у 75 (65%) хворих, антитіла до циклічного цитрулінового пептиду — у 82 (71%) пацієнтів. Оцінку функціонального класу збереження рухової активності суглобів проведено згідно з критеріями Американської колегії ревматологів (ACR, 1992). Також усі індивідууми були опитані за Стенфордською анкетою «Оцінки здоров’я хворих на ревматоїдний артрит» (HAQ).
До моменту включення в дослідження всі хворі застосовували глюкокортикоїди. У 85% випадків — отримували базисну терапію (метотрексат, лефлуномід, сульфасалазин або їх комбінацію). Тривалість базисної терапії становила від кількох місяців до 10–15 років.
Усім пацієнтам проводили допплерографічне дослідження сонних артерій. КІМ сонних артерій визначали у трьох точках: перша — на відстані 10 мм до цибулини, друга — приблизно на рівні біфуркації, третя — 10 мм після розгалуження, у ділянці внутрішньої сонної артерії. Враховували середнє арифметичне трьох показників та максимальне значення КІМ. За норму було прийнято КІМ <0,9 мм [18], потовщення — 0,9–1,2 мм [16], критерії бляшки — >1,2 мм або наявність атеросклеротичної бляшки (АБ) за наявності нормальної товщини КІМ.
Визначали такі фактори ризику атеросклерозу: проведено лабораторне дослідження рівня загального холестерину (ЗХС), тригліцеридів (ТГ), ліпопротеїдів високої щільності (ЛПВЩ), ліпопротеїдів низької щільності (ЛПНЩ), spy on cell phone маркерів запального процесу рівня лейкоцитів, швидкості осідання еритроцитів (ШОЕ), С-реактивного пептиду (СРП), вимірювання артеріального тиску (АТ).
Статистичний аналіз матеріалу виконано при використанні програми Statistica 6.0 з використанням коефіцієнтів кореляції Пірсона, Т-тесту для незалежних вибірок. З урахуванням кожної ознаки у порівняльних групах виявлено середню арифметичну величину (М) та стандартну похибку середньої (m). Для підтвердження статистичної достовірності різниці середніх вважали сприйнятливим значення отриманого рівня достовірності р<0,05.
Результати та обговорення
Із 115 хворих на РА у 80% випадків виявлено зміни у сонних артеріях: у 33 пацієнтів, які становили 1-шу групу, ознаки АСА були відсутні. До 2-ї групи увійшли 32 хворих із потовщенням КІМ — 0,9–1,2 мм. Учасники 3-ї групи (n=50) мали виражений атеросклеротичній процес (потовщення КІМ >1,2 мм, численні АБ).
Надалі проведено порівняння потовщення КІМ та частоти наявності й кількість АБ (табл. 1).
(χ² Пірсона =39,3, c=2, p<0,001)
| Наявність АБ | Група | |||||
|---|---|---|---|---|---|---|
| 1-ша (n=33) | 2-га (n=32) | 3-тя (n=50) | ||||
| n | % | n | % | n | % | |
| Є | – | – | 4 | 12,5 | 14 | 28 |
| Немає | 33 | 100 | 28 | 87,5 | 36 | 72 |
Аналіз даних (див. табл. 1) свідчить про більшу кількість АБ у представників 3-ї групи порівняно із двома іншими.
Наступним кроком було визначення частоти розповсюдженості атеросклеротичних змін сонних артерій та локалізації ураження останніх у різних груп хворих на РА (табл. 2).
| Група | Сонна артерія | ||
|---|---|---|---|
| ліва | права | обидві | |
| 1-ша (КІМ <0,9 мм) | 15 (13) | 12 (10,4) | 6 (5,2) |
| 2-га (КІМ 0,9–1,2 мм) | 7 (3,5) | 10 (11,5) | 15 (13) |
| 3-тя (КІМ >1,2 мм) | 13 (11,3) | 16 (14) | 21 (18) |
Розподіл хворих на групи дав можливість дослідити значення різних факторів ризику розвитку атеросклерозу. Найважливіші з них традиційні фактори кардіоваскулярного ризику: вік, стать, наявність артеріальної гіпертензії (АГ), спадковий анамнез серцево-судинних захворювань (ССЗ), підвищений індекс маси тіла (ІМТ) та наявність дисліпідемії.
Встановлено, що пацієнти з атеросклеротичним ураженням мають більшу кількість факторів ризику порівняно з менш вираженим атеросклеротичним процесом або без нього (р<0,001). Більш виражений вплив на атеросклеротичний процес демонструє наявність АГ та дисліпідемії (підвищення концентрації ЛПНЩ та зниження ЛПВЩ) (табл. 3).
| Показник | Група | р | |
|---|---|---|---|
| 1-ша (n=33) | 2-га (n=50) | ||
| Лейкоцити, ⋅10/л | 7,7±2,3 | 11,5±1,7 | <0,001 |
| ШОЕ, мм/год | 20,2±5,3 | 36,5±9,9 | <0,001 |
| ЗХС, ммоль/л | 4,2±0,7 | 5,1±0,2 | 0,6 |
| ЛПВЩ, ммоль/л | 1,2±0,4 | 0,6±0,018 | 0,0018 |
| ЛПНЩ, ммоль/л | 2,3±1,2 | 4,8±2,7 | 0,01 |
| ТГ, ммоль/л | 1,7±0,4 | 1,9±,6 | 0,8 |
| SCORE, % | <5 | >5 | <0,001 |
| Систолічний АТ, мм рт. ст. | 125,75±5,7 | 140,2±10,3 | 0,02 |
| Діастолічний АТ, мм рт. ст. | 70,3±12,7 | 80,5±10,6 | 0,025 |
Це відображається у дослідженнях інших авторів [1, 11], які стверджують, що АГ та дисліпідемія — найбільш розповсюджені кардіоваскулярні фактори ризику у хворих на РА [12, 22, 23].
Щодо значення SCORE необхідно зауважити, що показник товщини судинної стінки збільшувався зі зростанням індексу SCORE. Отже, при SCORE ≤5% КІМ становила 0,75±0,4 ліворуч та 0,68±0,15 — праворуч, а при SCORE >5% — відповідно 0,89±0,28 (р<0,05) ліворуч та 0,89±0,22 order essay online (р<0,05) — праворуч, що відображає тісний зв’язок традиційних факторів атеросклерозу з КІМ.
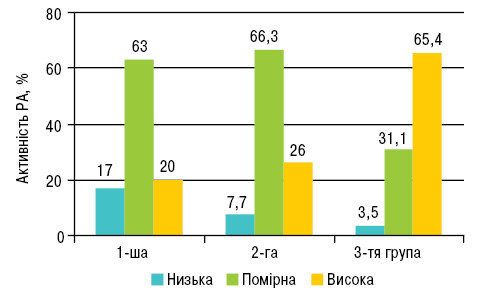
При подальшому дослідженні виявлено зв’язок атеросклеротичного процесу з активністю захворювання за DAS28. Високу активність за DAS28 виявлено серед пацієнтів зі значним атеросклеротичним ураженням, на відміну від представників 1-ї та 2-ї груп (р<0,02). У хворих 3-ї групи високу активність виявляли у 3 рази частіше, ніж у пацієнтів без атеросклерозу (65,5 та 20% випадків відповідно). Низька активність у 5 разів рідше спостерігалась у хворих із вираженим атеросклеротичним процесом, ніж у пацієнтів без ознак АСА (3,5 та 17% відповідно) (рисунок).
Існує значна кількість наукових робіт, які свідчать про асоціацію наявності АБ у сонних артеріях та активність захворювання за DAS28 у хворих на РА [11, 18, 24]. У джерелах [11, 18, 25, 27] наведено дані стосовно зв’язку прискореного розвитку атеросклерозу з наявністю РФ у сироватці крові та рівнем СРП. При дослідженні не виявлено чіткого зв’язку атеросклеротичного ураження КІМ із тривалістю РА та наявністю РФ, однак спостерігалася тенденція до підвищення рівня СРП у пацієнтів із вираженим атеросклеротичним процесом порівняно із групами з меншими атеросклеротичними змінами чи за їх відсутності (р=0,048).
Оскільки РА — хронічне захворювання, було досліджено взаємозв’язок між перебігом захворювання та атеросклеротичним ураженням сонних артерій. Задля цього проведено кореляційний аналіз зв’язку КІМ та показників, які характеризують особливості перебігу РА. Під час проведення дослідження виявлено тісний взаємозв’язок між КІМ і тривалістю РА (r=0,25; р=0,003) та індексом непрацездатності HAQ (r=0,27; р=0,004).
Висновки
Отже, в результаті проведеного дослідження у 80% хворих на РА виявлено зміни КІМ. Встановлено чітку залежність товщини КІМ не лише від традиційних факторів кардіоваскулярного ризику, а й від специфічних параметрів РА (активність за DAS28, індекс непрацездатності HAQ, рівень СРП у сироватці крові). Відомо, що для виникнення запалення необхідне утворення цитокінів, фактора росту ендотелію, а також інших протизапальних медіаторів із подальшою активацією та відкладання компонентів комплементу, що призводить до активації та проліферації ендотеліальних, гладком’язових клітин судинної стінки та відіграє важливу роль в атеросклерозі. У зв’язку з цим РА можна розглядати як самостійний фактор ризику кардіоваскулярних подій та розвитку раннього атеросклерозу, що дозволяє використовувати вимірювання КІМ у ролі ранньої діагностики атеросклерозу у хворих на РА.
Список використаної літератури
1. Аршин Е.В., Туев А.В., Щекотов В.В. (2005) Ремоделирование и диастолическая функция левого желудочка у больных артериальной гипертонией с ревматоидным артритом. Рос. кардиол. журн., 3: 32—37.
2. Агеев Ф.Т. (2005) Роль эндотелиальной дисфункции в развитии и прогрессировании сердечно-сосудистых заболеваний. Сердеч. недостаточность, 4(1): 20–22.
3. Гиляревский С.Р. (2005) Современные подходы к диагностике и профилактике прогрессирования начальных стадий атеросклероза сонных артерий. Трудный пациент, 3: 5–9.
4. Дряженкова И.В. (2012) Поражение сердечно-сосудистой системы при ревматических заболеваниях. Терапевт. арх., 4: 40–47.
5. Каратеев Д.Е. (2004) Основные тенденции и вариабельность эволюции ревматоидного артрита: результаты многолетнего наблюдения. Науч.-практ. ревматол., 1: 8–24.
6. Курак Т.А. (2010) Ультразвуковое исследование сонных артерий в диагностике ранних проявлений атеросклероза у больных с ревматоидным артритом. Мед. журн., 2: 76—78.
7. Мясоедова Е.Е., Мясоедова С.Е., Обжерина С.В. (2009) Бессимптомный атеросклероз сонных артерий и предикторы его развития при ревматоидном артрите. Клин. медицина, 87(7): 37–41.
8. Насонов Е.Л. (2003) Проблема атеротромбоза в ревматологии. Вестн. РАМН, 7: 6−10.
9. Насонов Е.Л. (2004) Ревматоидный артрит как общемедицинская проблема. Терапевт. арх., 5: 5–7.
10. Насонов Е.Л. (2005) Изучение хронического воспаления в патогенезе ревматических болезней. Фарматека, 7: 10−14.
11. Насонова Е.Л., Насонова В.А. (2010) Ревматология: национальное руководство. ГЭОТАР-медиа, Москва, 549 с.
12. Никитина Н.М., Ребров А.П. (2009) Применение аторвастатина у больных ревматоидным артритом с гиперлипидемией. Кардиология, 49(9): 21—26.
13. Полякова С.А., Раскина Т.Ф. (2007) Кардиоваскулярные факторы риска и толщина комплекса интима-медиа у женщин репродуктивного возраста, больных ревматоидным артритом. Науч.-практ. ревматол., 2: 24−28.
14. Сагитова Э.Р., Багирова Г.Г. (2012) Ранняя диагностика атеросклероза сонных артерий у больных с ревматоидным артритом. Клиницист, 1: 36–41.
15. Чазов Е.И. (2004) Взгляд из прошлого в будущее. Терапевт. арх., 6: 8–15.
16. Del Porto F., Laganà B., Lai S. et al. (2007) Response to anti- tumour necrosis factor alpha blockade is associated with reduction of carotid intima-media thickness in patients with active rheumatoid arthritis. Rheumatology (Oxford), 46: 1111–1115.
17. Hjeltnes G., Hollan I., Førre Ø. et al. (2011) The presence of anti-CCP antibodies and RF IgM was related to impaired endothelial function independent of other cardiovascular risk factors in RA patients. Scand. J. Rheumatol., 40: 422–427.
18. Kumeda Y., Inaba M., Goto H. (2008) Increased thickness of the arterial intima-media detected by ultrasonography in patient with rheumatoid arthritis. Arthritis Rheum., 46: 1489–1497.
19. Mayet W.-J., Schwarting A., Orth Th. et al. (2004) Cytotoxic effects of antibodies to proteinase 3 (c-ANCA) on human endothelial cells. Clin. Exp. Immunol., 97: 458–465.
20. Ortega-Hernandez O.D., Pineda-Tamayo R., Pardo A.L. et al. (2009) Cardiovascular disease is associated with extra-articular manifestations in patients with rheumatoid arthritis. Clin. Rheumatol., 28: 767–775.
21. Pasceri V., Yeh E.T.(2004) A tale of two diseases: atherosclerosis and rheumatoid arthritis. Circulation, 100: 2124−2126.
22. Roman M.J., Moeller E., Davis A. et al. (2006) Preclinical carotid atherosclerosis in patients with rheumatoid arthritis. Ann. Intern. Med., 144(4): 249–256.
23. Solomon D.H., Curhan G.C., Rimm E.B. et al. (2004) Cardiovascular risk factors in women with and without rheumatoid arthritis. Arthritis Rheum., 50: 3444–3449.
24. Touboul P.J., Hennerici M.G., Meairs S. et al. (2007) Mannheim carotid intima-media thickness consensus (2004–2006). An update on behalf of the advisory board of the 3 and 4 watching the risk symposium, 13 and 15 European spy app stroke conferences, Mannheim, Germany, 2004, and Brussels, Belgium, 2006. Cerebrovasc. Dis., 23: 75–80.
25. Turesson C., McClelland R.L., Christianson T.J. et al. (2007) Severe extra-articular disease manifestations are associated with an increased risk of first ever cardiovascular events in patients with rheumatoid arthritis. Ann. Rheum. Dis., 66: 70–75.
26. van Doornum S., McColl G., Wick I.P. (2005)Accelerated atherosclerosis. An Extraarticular feature of rheumatoid arthritis. Arthritis Rheum., 46: 862–873.
27. Yamasaki Y., Kawamori R., Matsushima H. et al. (2004) Atherosclerosis in carotid artery of young IDDM patients monitored by ultrasound high-resolution B-mode imaging. Diabetes, 43: 634–639.
Неинвазивное исследование толщины комплекса интимы-медиа у больных ревматоидным артритом
Резюме. Цель исследования — оценка толщины комплекса интимы-медиа (КИМ) у больных ревматоидным артритом (РА) и выявление взаимосвязи факторов риска, способствующих развитию атеросклероза, а также специфических параметров РА. Исследование при участии 115 больных РА выполняли в соответствии с протоколом обследования этих больных. Проводили дуплексное сканирование брахиоцефальные сосудов. Факторов риска фатальных сердечно-сосудистых событий, вызванных атеросклерозом, оценивали с помощью шкалы SCORE. У 80% больных РА выявлены изменения КИМ. Установлена четкая зависимость толщины КИМ не только от традиционных факторов кардиоваскулярного риска, но и от специфических параметров РА (активность по DAS28, индекс нетрудоспособности HAQ, уровень С-реактивного пептида в сыворотке крови). Известно, что для возникновения воспаления необходимо образование цитокинов, фактора роста эндотелия, а также других провоспалительных медиаторов с последующей активацией и отложение компонентов комплемента, что приводит к активации и пролиферации эндотелиальных, гладкомышечных клеток сосудистой стенки и играет важную роль в атеросклерозе. В связи с этим РА можно рассматривать как самостоятельный фактор риска кардиоваскулярных событий и развития раннего атеросклероза, что дает возможность ранней диагностики атеросклероза у больных РА.
ревматоидный артрит, атеросклероз сонных артерий, толщина комплекса интимы-медиа сонных артерий, кардиоваскулярные факторы риска.
Адреса для листування:
Закритов Денис Олексійович
650025, Одеса, вул. Академіка Заболотного, 26
Одеська клінічна обласна лікарня

Leave a comment