ОЦІНКА ЯКОСТІ ЖИТТЯ, ТРИВОЖНОСТІ й ДЕПРЕСІЇ У ПАЦІЄНТІВ ІЗ РЕВМАТОЇДНИМ АРТРИТОМ
Головач И.Ю., Авраменко О.Н., Куринная Л.И.
Резюме. Резюме. У статті наведено результати дослідження, мета якого — оцінка якості життя, вираженості тривожності й наявності депресивних розладів у пацієнтів із ревматоїдним артритом, а також встановлення кореляційних взаємозв’язків із клінічними характеристиками перебігу ревматоїдного артриту. Під наглядом перебували 76 пацієнтів із достовірним діагнозом ревматоїдного артриту. Якість життя вивчали за допомогою опитувальників SF-36 і NAIF. Встановлено, що якість життя хворих на ревматоїдний артрит достовірно нижча порівняно із практично здоровими особами, що зумовлено наявністю хронічного захворювання. Найбільш значне зниження відзначено за шкалами фізичної мобільності, соціальної функції та економічного становища пацієнта. З високою частотою при ревматоїдному артриті виявляються депресія і тривожність, що корелюють з основними клінічними проявами ревматоїдного артриту.
Введение
В течение последних десятилетий нарастает внимание общества к субъективному благополучию и качеству жизни человека. В соответствии с этим и понимание природы соматических заболеваний, и подходы к их лечению и реабилитации все больше смещаются от биомедицинской к биопсихосоциальной модели медицины [4, 7]. Ревматология, в особенности ревматоидный артрит (РА) как центральная проблема современной ревматологии, представляют особый интерес относительно биопсихосоциальных концепций [14, 18]. Это заболевание часто рассматривается как классическая модель психосоматического расстройства и прикладное поле основных теоретических проблем медицины, в частности интегративного подхода, поэтому успехи в изучении, и особенно в терапии, РА существенно влияют на развитие медицины в целом.
РА — аутоиммунное ревматическое заболевание, поражающее до 2% взрослого населения развитых стран в наиболее трудоспособном возрасте, характеризуется хроническим эрозивным артритом и системным поражением внутренних органов [11]. Основные проблемы, дезадаптирующие пациентов с РА, обусловлены хроническим болевым синдромом, ограничением повседневной активности с утратой трудоспособности и социальных связей, нередко приводят к необходимости смены работы, ухудшению материального положения, изменению семейных, социальных взаимоотношений и качества жизни [1, 12, 19]. Высокая степень дезадаптации, зачастую неконтролируемые рецидивы болезни, а также высокая частота коморбидных РА тревожно-депрессивных расстройств (ТДР) объясняют необходимость проведения исследований, посвященных изучению клинико-патогенетических взаимосвязей РА и депрессии, во многом определяющих динамику и прогноз системного заболевания, влияющих на тактику комплексного лечения и его эффективность [20].
Несмотря на то что психосоматические, психологические и психопатологические аспекты РА изучаются многие годы, однако до настоящего времени остается много спорных вопросов, касающихся психологических предшественников заболевания, и недостаточно изученных аспектов психосоциальных последствий РА [6, 13].
Изначально ТДР при РА рассматривались как последствия тяжелого хронического соматического расстройства. Однако в последние годы все больше исследователей предлагают рассматривать ТДР в качестве самостоятельных заболеваний, зачастую предшествующих развитию РА и имеющих с ним единые провоцирующие и предрасполагающие факторы, а также схожие звенья патогенеза [1, 17, 23]. В частности, известно, что примерно ⅔ больных РА имеют ТДР еще до возникновения симптомов ревматического заболевания [16].
Кроме того, артрит и депрессия — заболевания, имеющие самые низкие оценки качества жизни. Высокий уровень депрессии и тревоги определен у пациентов с такими хроническими заболеваниями, как артрит и сахарный диабет ІІ типа, хроническая обструктивная болезнь легких и хроническая сердечная недостаточность [17]. Влияние депрессии и тревоги на течение этих заболеваний оказалось не менее значимым, чем влияние их соматических характеристик [18].
Одной из важных характеристик является оценка качества жизни. ВОЗ рекомендует определять качество жизни как взаимосвязь показателей здоровья человека и социально-экономических факторов, которые оценивают как комплекс физических, эмоциональных, психических и интеллектуальных характеристик человека, определяющих его индивидуальную способность к функционированию в обществе [22]. Однако медицинское понятие качества жизни включает, прежде всего, те показатели, которые связаны с состоянием здоровья человека [8]. Под медицинскими аспектами качества жизни понимают влияние самого заболевания (его симптомов и признаков), вызванных им ограничений функциональной способности, а также лечения на повседневную жизнедеятельность больного [5]. Качество жизни сегодня — это надежный, информативный и экономичный метод оценки здоровья больного как на индивидуальном, так и на групповом уровне.
Цель исследования — оценка качества жизни, выраженность тревожности и наличие депрессивных расстройств у пациентов с РА, а также установление корреляционных взаимосвязей с клиническими характеристиками течения РА.
Объект и методы исследования
В основу исследования положены данные о 76 пациентах с РА, находившихся на стационарном лечении в отделении ревматологии и внутренней патологии Клинической больницы «Феофания» (Киев) за период 2012–2013 гг. Критериями исключения из исследования были: наличие злокачественных новообразований, наличие иных клинически значимых хронических соматических заболеваний с неблагоприятным краткосрочным прогнозом, отказ от участия в исследовании. Критерии включения в исследование: наличие РА, согласие больных на участие в исследовании, постоянное применение метотрексата в стабильной дозе, прием кальция и витамина D в рекомендованных дозах. Больных включали в исследование по мере поступления. Каждый пациент подписывал бланк информированного согласия. Диагноз РА являлся достоверным согласно критериям Американской коллегии ревматологов (ACR, 1987) и критериям ACR/EULAR (2010) [11].
Возраст обследованных пациентов колебался от 32 до 74 лет, в среднем составлял 45,7±7,3 года. Среди включенных в исследование было 27 мужчин и 49 женщин. Все пациенты были обследованы согласно стандартам, что включало определение рентгенологической стадии процесса, активности заболевания, серопринадлежности, наличия и степени поражения внутренних органов. Так, у 25 пациентов определен ранний РА с длительностью суставного синдрома до 12 мес (средняя продолжительность суставного синдрома составила 6,7±2,8 мес). У этих пациентов I рентгенологическая стадия определена у 12 человек, II стадия — у 13. У остальных (51 пациента) верифицирован поздний РА; начальные рентгенологические стадии не определялись вообще, II стадия — у 10 пациентов, III стадия — у 34, IV — у 7. Средняя длительность суставного синдрома у пациентов с поздним РА составила 96,3±32,7 мес. Превалирующее большинство больных были серопозитивными по ревматоидному фактору (РФ): 56 против 20. Серопозитивными по антителам к цитруллированным белкам (антиЦЦП) были 62 пациента, серонегативными соответственно — 14 больных. Активность процесса определяли согласно индексу DAS28, для его расчета использовали визуальный on-line-калькулятор оценки активности заболевания. Низкая активность установлена у 15 пациентов, средняя — у 27, высокая — у 34. Средний балл по DAS28 составил 4,93±1,06.
Контрольная группа включала 30 практически здоровых лиц, репрезентативных по возрасту и полу основной группе.
Для количественного определения нарушений жизнедеятельности при РА обычно используют различные опросники (общие — SF-36, EQ-5D и специфические — HAQ, RAPID-3), заполняемые больными самостоятельно и отражающие в определенной степени качество их жизни. Именно определение нарушений жизнедеятельности (disability) пригодно для потенциального измерения исходов длительно текучих хронических заболеваний, таких как РА, и хорошо согласуется с программой TreattoTarget (T2T), в которой сохранение высокого качества жизни больных является еще одной, не менее важной, целью терапии РА [2].
Для оценки качества жизни у пациентов с РА использовали две наиболее распространенные шкалы — NAIF и SF-36 [8].
Оценку качества жизни проводили по методике NAIF (New Assessment and Information Form to Measure Quality of life), предложенной P.Y. Hugenholtz и R.A.M. Erdman в 1995 г. [22]. Перевод на русский язык и адаптирование выполнено А.Л. Пушкаревым и Н.Г. Аринчиной в лаборатории психологических проблем реабилитации НИИ медико-социальной экспертизы и реабилитации (Минск, Республика Беларусь) [9]. Опросник состоит из 24 вопросов-суждений, имеет 6 составляющих: физическая мобильность, эмоциональное состояние, сексуальная функция, социальная функция, познавательная функция, экономическое положение. Оценка по составляющим проводится по сумме баллов, итоговая сумма баллов представляет собой интегральный показатель качества жизни. Полученные показатели переводятся в проценты. У человека с сохраненными функциями, довольного всеми сторонами своей жизни, интегральный показатель качества жизни равен 100% или приближается к этому уровню; незначительное снижение качества жизни — до 75%, умеренное — до 50%, значительное — до 25%, резко выраженное — менее 25%.
Одновременно качество жизни пациентов с РА определяли по опроснику SF-36 (Short Form-36-Item HealthSurvey) [10] с вычислением 8 основных показателей: ФФ — физическое функционирование, РФФ — ролевое физическое функционирование, Б — боль, ОЗ — общее здоровье, Ж — жизнеспособность, СФ — социальное функционирование, РЭФ — ролевое эмоциональное функционирование, ПЗ — психическое здоровье и оценка двух суммарных измерений: физического (PCS) и психологического здоровья (MCS), которые сравнивали с популяционным контролем соответствующего пола и возраста. Обработку шкал SF-36 производили с использованием специального лицензионного пакета статистических программ [8].
Болевой синдром оценивали по 10-балльной визуальной аналоговой шкале (ВАШ) самими пациентами.
Для изучения психоэмоционального состояния использовали шкалу самооценки тревоги Спилбергера, адаптированную Ю.Л. Ханиным [3, 21], и шкалу оценки депрессии Гамильтона (ШДГ) [3, 15]. Уровень тревожности оценивали по сумме баллов: <30 баллов — низкий, 30–45 баллов — умеренный, >45 баллов — высокий. Результаты тестирования по ШДГ определяли по итоговой сумме баллов: 6–8 баллов считалось нормой, 16–18 баллов у пациентов молодого возраста и 18–20 баллов у лиц пожилого возраста свидетельствовали о наличии непсихотического депрессивного состояния, >18–20 баллов свидетельствовали о возможной психотической депрессии.
Статистическую обработку материала проводили с использованием программы Statistica 8.0. По каждому признаку в сравниваемых группах определяли среднюю арифметическую величину (М) и ошибку средней (m). Для всех видов анализа различия считали достоверными при р<0,05.
Результаты исследований и их обсуждение
Результаты сравнительного анализа параметров качества жизни больных РА и группы популяционного контроля соответствующего пола и возраста, оцененных с помощью опросников NAIF и SF-36, свидетельствуют о том, что все показатели качества жизни больных были статистически значимо ниже по сравнению с популяционными.
При тестировании по методике NAIF значительное снижение интегрального показателя (ИП) качества жизни (от 49 до 25%) выявлено у 40 пациентов с РА (52,6%), умеренное снижение ИП (от 74 до 50%) — у 29 больных РА (38,2%), незначительное снижение ИП (от 100 до 75%) — у 7 (9,2%) больных РА. Таким образом, у всех пациентов с РА ИП качества жизни был достоверно снижен. Наибольшее снижение отмечено по физической мобильности (на 47,24%), сексуальной функции (на 37,68%), экономическому положению (на 46,77%) и ИП (на 29,78%). Полученные данные свидетельствуют, что наличие такого хронического соматического заболевания, как РА, снижает качество жизни во всех сферах. С увеличением возраста и длительности заболевания выявлено снижение качества жизни в основном за счет снижения физической мобильности, сексуальной функции и экономического статуса. Так, достоверные разницы по этим шкалам установлены у пациентов с ранним и поздним РА (p<0,05). При анализе данных отмечена зависимость качества жизни от интенсивности болевого синдрома. При оценке боли по 10-балльной ВАШ боли достоверно (р<0,05) снижен ИП NAIF, составивший у пациентов с уровнем боли от 1 до 3 баллов 58,27±12,03%, от 4 до 6 баллов — 57,88±11,24%, от 7 до 10 баллов — 46,76±13,61%. Более низкий уровень ИП при нарастании боли от 3 до 6 баллов обусловлен снижением физической мобильности с 56,12±12,36 до 42,33±12,76% (р<0,01), сексуальной функции — с 92,78±5,24 до 44,86±14,73% (р<0,01), экономического положения — с 92,66±7,14 до 32,08±14,33% (р<0,01) соответственно. Серопозитивный вариант заболевания и наличие системных проявлений оказывали отрицательное влияние на качество жизни пациентов. Снижение ИП NAIF при серопозитивном варианте РА происходило в основном за счет изменения эмоционального состояния; кроме этого, данный показатель коррелировал с выраженностью изменений РФ и антиЦЦП. При развитии системных проявлений заболевания в большей степени страдали сексуальная и социальная функции, а также экономическое положение. Характер костно-суставных изменений существенно влияет на качество жизни. При повышении рентгенологической стадии РА достоверно снижались сексуальная и социальная функции. Значимо ухудшалось экономическое положение: у больных РА I стадии рентгенологических изменений этот показатель составил 84,67±13,56%, IV стадии — 35,33±11,67% (р<0,01). Из приведенных данных следует, что с увеличением тяжести заболевания и ограничением функциональной способности качество жизни пациентов с РА снижается, они теряют возможность вести активный образ жизни, чувствовать себя полноценными членами общества.
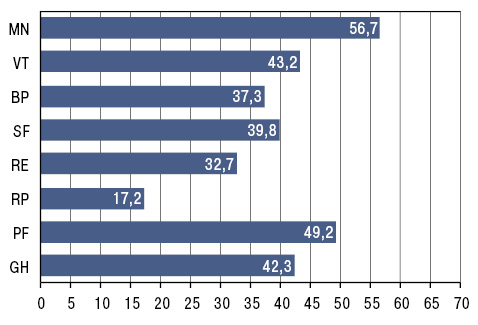
Тестирование пациентов с помощью опросника SF-36 также продемонстрировало снижение показателей качества жизни при РА. В наибольшей степени это касалось PCS, который на >19 баллов ниже средних значений популяционного контроля, что свидетельствовало о значительных ограничениях больных РА при самообслуживании и выполнении физических нагрузок. В наибольшей степени изменялись показатели физического здоровья (ФФ, РФФ, Б, ОЗ). ФФ было снижено на 44,8%, показатель РФФ — на 38,1%, показатель Б — на 37,3% по сравнению со средними значениями популяционного контроля. Среди показателей качества жизни, характеризующих психологическое здоровье (Ж, СФ, РЭФ, ПЗ), в большей степени были снижены Ж на 36,8% и СФ — на 31,9%.
Нами проведен анализ корреляционных зависимостей некоторых клинических показателей со значениями шкал PCS и MCS SF-36. Результаты представлены в таблице.
| Показатель | PCS | MCS |
|---|---|---|
| Возраст, лет | –0,36* | –0,32* |
| Активность по DAS28, баллов | –0,54* | –0,43 |
| Боль по ВАШ, мм | –0,58* | –0,66* |
| Число болезненных суставов, n | –0,34* | –0,38* |
| Число припухших суставов, n | –0,38* | –0,46* |
| Рентгенологическая стадия РА по Штейнброкеру | –0,17 | –0,10 |
| РФ, МЕ/мл | –0,09 | –0,18* |
| ИП NAIF, % | 0,74* | 0,77* |
Числовые значения коэффициента корреляции по Пирсону, знак «–» означает отрицательную корреляционную связь; *статистически значимая корреляционная связь при р<0,05.
Как видно из таблицы, большинство шкал имело умеренные, статистически значимые корреляционные связи с возрастом, активностью заболевания по DAS28, числом болезненных и припухших суставов, болью по ВАШ. Выявлена высокая корреляционная связь между шкалами SF-36 и ИП NAIF. Не выявлено взаимосвязи КЖ с рентгенологической стадией заболевания (r=–0,17; r=–0,10), также PCS с наличием или отсутствием РФ в крови (r=–0,09).
Показатели качества жизни пациентов по отдельным шкалам представлены на рис. 1.
При тестировании тревожности по методике Спилбергера — Ханина реактивная и личностная тревожность у больных РА была достоверно выше, чем у лиц контрольной группы. Среди пациентов с РА чаще отмечали лиц с высокой ситуационной (22,86%) и личностной (76,77%) тревожностью по сравнению с практически здоровыми обследованными: 10,0 и 40,0% соответственно.
У пациентов с высокой реактивной и личностной тревожностью уровень качества жизни был достоверно ниже, чем у больных с умеренным и низким уровнем тревожности. Так, у лиц с высокой реактивной тревожностью интегральный показатель (ИП) качества жизни составил в среднем 45,67±7,54%, с умеренной — 55,03±9,76% (р<0,05) и с низкой — 57,14±10,63% (р<0,01). При нарастании уровня реактивной тревожности выявлено достоверное (р<0,05) снижение эмоционального состояния и сексуальной функции, наблюдалось также недостоверное, однако значимое снижение физической мобильности, социальной функции и экономического положения. Одновременно у пациентов с высокой личностной тревожностью качество жизни было ниже по всем составляющим. ИП качества жизни у больных РА с высокой личностной тревожностью составил 52,12±10,16%, а у пациентов с умеренной личностной тревожностью — 65,58±9,75% (р<0,001).
Сниженный фон настроения, бессонница, отсутствие интереса к жизни, возникающие при депрессии, негативно отражаются на качестве жизни больных РА. При тестировании по ШДГ средние значения у больных РА были достоверно выше по сравнению с лицами контрольной группы — 12,17±5,33 и 7,98±2,54 балла (р<0,01). Депрессивные расстройства выявлены у 28 (36,84%) пациентов с РА, из них у 19 (25,0%) человек депрессия была непсихотической, а у 9 (11,84%) — психотической.
Общеизвестно, что распространенность депрессивных расстройств при РА, как показывает анализ многочисленных исследований, имеет большой диапазон значений — от 12,5 до 80% [6]. Однако в целом депрессия у пациентов с РА отмечается чаще, чем у соматически здоровых и у пациентов с другими соматическим заболеваниями. Природа депрессивных расстройств при РА определяется взаимным влиянием соматогенных, психогенных и конституционально-личностных факторов. А тяжесть соматической патологии выступает также и фактором психической травматизации [13].
Интересные закономерности установлены при анализе депрессивных расстройств и клинических показателей течения РА. Так, наиболее высокие показатели по ШДГ установлены при высокой активности заболевания, выраженном болевом синдроме, большом количестве припухших суставов, а также при раннем РА в сравнении с поздним РА.
Корреляционные взаимосвязи между показателями депрессии и клиническими особенностями течения РА представлены на рис. 2.
Полученные данные при оценке тревожности и депрессивных расстройств свидетельствуют о значимости влияния психоэмоционального состояния на формирование качества жизни, являющегося интегральным показателем здоровья.
Комплексное изучение качества жизни больных РА выявило существенные взаимосвязи этих показателей с основными клиническими характеристиками пациентов, выраженностью боли и степенью активности заболевания. У более чем половины пациентов с РА выявляют ТДР, выраженность которых коррелирует с основными показателями активности воспалительного процесса.

Выводы
1. Качество жизни больных РА достоверно ниже по сравнению с практически здоровыми лицами, что обусловлено наличием хронического заболевания. Наиболее значительно снижены физическая мобильность, социальная функция и экономическое положение пациента.
2. Качество жизни пациентов с РА в большей степени зависит от психоэмоционального состояния, чем от длительности и тяжести заболевания.
3. Показатели качества жизни, тревожность и выраженность депрессивных расстройств значимо коррелируют с основными клиническими показателями течения РА.
Список использованной литературы
1. Авраменко О.Н., Головач И.Ю., Прима И.В. и др. (2011) Распространенность и важность диагностики тревожно-депрессивных расстройств у больных ревматоидным артритом. Medix. Anti-Aging., 3(21): 48–52.
2. Амирджанова В.Н., Погожева Е.Ю. (2012) Качество жизни больных ревматоидным артритом, получающих цертулизумаба пэгол. Науч.-практ. ревматол., 54(5): 80–84.
3. Батаршев А.В. (2005) Базовые психологические свойства и самоопределение личности: Практ. руководство по психологической диагностике. Речь, Санкт-Петербург, с. 44–49.
4. Дробижев М.Ю. (2006) Депрессия как общемедицинская проблема. Психиатрия и психофармакотерапия, 8(2): 57–61.
5. Коц Я.И., Либис Р.А. (1993) Качество жизни у больных с сердечно-сосудистыми заболеваниями. Кардиология, 5: 66–72.
6. Кремлева О.В. (2004) Психотерапия в системе лечения больных ревматоидным артритом (с позиций биопсихосоциального подхода): Автореф. дисс. … докт. мед. наук, Санкт-Петербург, 48 с.
7. Курпатов В.И. (2000) Психосоматический подход к лечению заболеваний сердечно-сосудистой системы. Психическое здоровье Санкт-Петербурга 2000: Матер. конф., Санкт-Петербург, с. 137–138.
8. Новик А.А., Ионова Т.И. (2002) Руководство по исследованию качества жизни в медицине. Нева, Санкт-Петербург, ОЛМА-ПРЕСС Звездный мир, Москва, 320 с.
9. Пушкарев А.Л., Аринчина Н.Г. (2000) Методика оценки качества жизни больных и инвалидов: Метод. рекомендации. Минск, 22 с.
10. Разрешение на использование и воспроизведение опросника SF-36. MedicalOutcomesTrust. — URL (http://www.sf-36.com./tools/sf36.shtml).
11. Ревматология: Национальное руководство (2010). Под ред. Е.Л. Насонова, В.А. Насоновой., М.: ГЭОТАР-Медиа. — 720 с.
12. Симонова Я.О., Никитина Н.М., Ребров А.П. (2009) Качество жизни больных ревматоидным артритом как критерий эффективности лечения. Сибир. мед. журн., 91(8): 79–81.
13. Ташлыков В.А. (2010) Особенности клиники и терапии депрессии при ревматоидном артрите. Вест. Северо-Запад. гос. мед. ун-та им. И.И. Мечникова, 2(1): 83–85.
14. Dougados M., Soubrier M., Antunez A. et al. (2014) Prevalence of comorbidities in rheumatoid arthritis and evaluation of their monitoring: results of an international, cross-sectional study (COMORA). Ann.Rheum. Dis., 73(1): 62–68.
15. Hamilton M. (1969) Standardised assessment and recording of depressive symptoms. Psychiatr. Neurol. Neurochir., 72: 201–205.
16. Hanly J.G., Fisk J.D., McCurdy G. et al. (2005) Neuropsychiatric syndromes in patients with systemic lupus erythematosus and rheumatoid arthritis. J. Rheumatol., 32: 1459–1466.
17. Katon W.J. (2011) Epidemiology and treatment of depression in patients with chronic medical illness. Dial. Сlin. Neurosci., 13: 7–23.
18. Kojima M., Kojima T., Suzuki S. et al. (2009) Depression, inflammation, and pain in patients with rheumatoid arthritis. Arthritis Rheum., 61(8): 1018–1024.
19. Lutze U., Archenholtz B. (2007) The impact of arthritis on daily life with the patient perspective in focus. Scand. J. Caring. Sci., 21: 64–70.
20. Rose G. (2006) Why do patients with rheumatoid arthritis use complementary therapies? Musculoskeletal. Care., 4: 101–115.
21. Spielberger C.D., Gorsuch R.L., Lushene R.E. (1970) Manual for the State-Trait Anxiety Inventory. Consulting Psychologist Press. Palo. Alto., CA: 38.
22. The WHOQOL Group. What quality of life? (1996) World Health Forum, 17: 354–356.
23. Yirmiya R., Pollak Y., Morag M. et al. (2000) Illness, Cytokines, and Depresion. Ann. NY Acad. Sci., 917: 478–487.
Адрес для переписки:
Головач Ирина Юрьевна
03680, Киев, ул. Заболотного, 21, 3-й корпус
Клиническая больница «Феофания» ГУД
E-mail: golovachirina@yandex.ru

Leave a comment