АНАЛІЗ ВІДТЕРМІНУВАННЯ ВСТАНОВЛЕННЯ ДІАГНОЗУ ПРИ СИСТЕМНОМУ ЧЕРВОНОМУ ВОВЧАКУ
Резюме. Актуальність. Встановлення діагнозу системний червоний вовчак (СЧВ) часто викликає значні труднощі та потребує участі лікарів різних спеціальностей, проведення великої кількості лабораторних та інструментальних досліджень. Основними причинами є гетерогенність клінічної картини, можливість залучення практично всіх органів та систем, недостатня обізнаність лікарів щодо варіантів дебюту та перебігу СЧВ. Мета. Визначити час відтермінування встановлення діагнозу СЧВ в різних вікових категоріях та при різних клінічних проявах у дебюті, узагальнити маршрути пацієнтів до підтвердження діагнозу. Методи. Проведено ретроспективний аналіз медичної документації 167 пацієнтів, що перебували на лікуванні в ДУ «ННЦ «Інститут кардіології імені академіка М.Д. Стражеска НАМН України» в період з 2011 по 2020 р. Дані 130 з них виявилися достатньо інформативними та були включені в аналіз. Результати, встановлені у групах дослідження, порівнювали за допомогою критерію Манна — Уїтні. Розбіжності вважали статистично значущими при р<0,05. Результати. Встановлено, що час відтермінування діагнозу є достовірно вищим у віковій категорії старше 40 років. Виявлено, що наявність артриту в дебюті захворювання подовжує діагностичний пошук, тоді як наявність ураження нирок та серозиту — скорочує. Описано перелік хибних діагнозів, що встановлювалися пацієнтам, виділено деякі типові маршрути до встановлення діагнозу. Висновки. Отримані дані свідчать про необхідність вищої настороженості щодо СЧВ у пацієнтів середнього та похилого віку, за наявності суглобового синдрому, ізольованого ураження окремих органів з нетиповими проявами.
DOI: 10.32471/rheumatology.2707-6970.87.16747
УДК: 616.5–002.52–074
Системний червоний вовчак (СЧВ) характеризується різноманітними мультисистемними проявами, що часто зумовлює тривалу затримку у встановленні діагнозу. Згідно з різними дослідженнями, проведеними у великих центрах третинної допомоги, середній час відтермінування діагностики становив близько 2 років (ймовірно, вони охоплювали переважно пацієнтів з тяжкими формами хвороби) [1, 2]. У 2018 р. у Великій Британії проведено дослідження шляхом онлайн-анкетування учасників форуму пацієнтів з СЧВ. Згідно з його результатами середній час від появи перших симптомів до встановлення діагнозу становив 6 років 11 міс, що, ймовірно, пов’язано з охопленням усіх категорій пацієнтів, у тому числі з легкою формою захворювання та повільно прогресуючим перебігом [3]. Високий індекс підозри на СЧВ є дуже важливим, тому у разі наявності клінічних проявів з боку двох і більше систем організму, що не мають однозначного пояснення, слід провести дообстеження з приводу СЧВ [4]. Також автори деяких досліджень дають уточнення до даної рекомендації:
- оскільки артрит і артралгії є найпоширенішими початковими симптомами захворювання, кожна молода жінка з цими симптомами повинна бути обстежена на предмет СЧВ [5];
- у молодих людей часто діагностують психіатричну патологію до того, як їм верифікували діагноз СЧВ, що потребує особливої настороженості в даній ситуації [4];
- можливий дебют СЧВ з ізольованого ураження нирок, діагноз може бути підтверджений біопсією нирок чи імунологічними дослідженнями [6].
Основним скринінговим лабораторним маркером СЧВ є визначення титру антинуклеарних антитіл (АНА). Проте практично не існує чіткої регламентації показань до його призначення. Один з нечисленних прикладів — рекомендації з дослідження антинуклеарних антитіл (Antinuclear Antibody (ANA) Testing Protocol) Британської Колумбії (провінція Канади), створені у 2013 р. [7]. Згідно з ними призначення аналізу крові на рівень АНА є доцільним і може зробити внесок у встановлення діагнозу, лише якщо скарги пацієнта, анамнез, дані фізикального обстеження чи рутинних лабораторних методів вказують на СЧВ, склеродермію, синдром Шегрена, змішане захворювання сполучної тканини або дермато- чи поліміозит. У таких пацієнтів зазвичай відмічають принаймні одну з наступних клінічних ознак, що не пояснюється іншими причинами:
- артрит;
- плеврит або перикардит;
- фоточутливий висип;
- лабораторні дані про порушення функції нирок;
- гемолітична анемія, імунна тромбоцитопенія або нейтропенія;
- зміни шкіри, характерні для СЧВ, склеродермії, дерматоміозиту або васкуліту;
- клінічні чи лабораторні ознаки міозиту;
- феномен Рейно;
- неврологічні симптоми.
За відсутності вищеперелічених проявів позитивний тест на АНА лише утруднює діагностичний процес, оскільки позитивний результат часто виявляють при багатьох неревматичних станах (вірусні інфекції, онкологічні захворювання, тиреотоксикоз, захворювання печінки, синдром хронічної втоми). До того ж досить високою є поширеність АНА у здорових людей — 3–15%. Продукція цих аутоантитіл дуже залежить від віку та збільшується до 10–37% в осіб старше 65 років. Деякі ліки (статини, блокатори β-адренорецепторів, інгібітори ангіотензинперетворювального ферменту (АПФ) та нестероїдні протизапальні препарати (НПЗП) тощо) також можуть викликати підвищення рівня АНА. Проте для системних захворювань сполучної тканини характерні високі титри АНА, тоді як у здорових осіб та при інших захворюваннях підвищення є незначним чи помірним.
Визначення АНА вважається малоінформативним для оцінки таких скарг, як хронічна втома, біль у спині чи інший скелетно-м’язовий біль за відсутності вищезазначених клінічних даних.
Зазвичай рівень АНА визначається одноразово. При позитивному результаті повторне визначення не потрібне, оскільки титр АНА не має чіткої кореляції з активністю захворювання (при СЧВ для контролю активності захворювання використовують рівень антитіл до двоспіральної ДНК, компонентів комплементу С3 і С4). При негативному результаті повторне визначення доцільне лише при появі нових клінічних ознак, що дозволяють запідозрити системне захворювання сполучної тканини.
Раннє встановлення діагнозу має важливе значення як для здоров’я пацієнта, так і для системи охорони здоров’я в цілому. Так, у пацієнтів із затримкою діагностики менше ніж на 6 міс відмічаються нижча частота рецидивів та менші витрати на лікування порівняно з пацієнтами із затримкою більше 6 міс [8]. Для пацієнтів із залученням життєво важливих органів (нефрит, ураження нервової системи) затримка діагностики та початку імуносупресивної терапії пов’язана зі значимими негативними наслідками [9, 10].
Іншим важливим аспектом, що впливає на відтермінування діагнозу, є вік дебюту СЧВ. Вважається, що дане захворювання найчастіше виникає у молодих людей віком 20–30 років. Проте останнім часом все більше досліджень вказують на більш пізній середній вік дебюту захворювання. Для прикладу, у Великій Британії цей показник становить 47,9 року, а у штаті Каліфорнія (США) — 43,9 року [11, 12].
МАТЕРІАЛИ І МЕТОДИ дослідження
Вивчено медичну документацію 167 пацієнтів та проведено анкетування 40 пацієнтів, що проходили стаціонарне та амбулаторне лікування в Інституті кардіології імені академіка М.Д. Стражеска за період з 2011 по 2020 р. Достатньо інформативними виявилися дані 130 пацієнтів. У кожного визначено час від появи перших симптомів до встановлення діагнозу СЧВ, клінічні прояви в дебюті, прослідковано динаміку клінічних проявів та процес діагностичного пошуку.
Пацієнтів розподілено на 3 вікові категорії: до 20 років — 41 пацієнт (31,5%); 20–40 років — 72 пацієнти (55,5%); старше 40 років — 17 пацієнтів (13%). З метою урівняння кількості хворих в групах обрано саме такі часові межі, а не класичні: до 18 років — ювенільний СЧВ, після 50 років — СЧВ з пізнім початком («late-onset SLE»). Визначено середній час відтермінування діагнозу СЧВ в кожній групі та зіставлено між собою. Також виявлено залежність даного показника від наявності чи відсутності найпоширеніших проявів СЧВ в дебюті (артрит, шкірний висип, серозит, нефрит). При дослідженні динаміки захворювання та тактики діагностики визначено частоту встановлення хибних діагнозів, виділено кілька «типових маршрутів» пацієнтів.
Нормальність розподілу даних перевіряли за критерієм Колмогорова — Смірнова. Оскільки розподіл виявився ненормальним, то результати, встановлені у досліджуваних групах, порівнювали за допомогою критерію Манна — Уїтні. Розбіжності вважали статистично значущими при р<0,05.
РЕЗУЛЬТАТИ дослідження
Серед обстежених пацієнтів було 109 жінок (84%) та 21 чоловік (16%). Співвідношення статей — 5,2:1. Середній вік встановлення діагнозу — 26,8±0,91 року. Достовірної різниці між чоловіками та жінками не виявлено (24,5±2,7 та 27,2±0,96 року відповідно). Даний показник є значно нижчим, ніж у вищенаведених зарубіжних дослідженнях, що свідчить про потребу посилення настороженості лікарів щодо СЧВ у пацієнтів середнього та пенсійного віку.
Середній час затримки встановлення діагнозу становив 1 рік 11 міс та 1 тиж (1,94±0,27 року). Достовірної різниці між чоловіками та жінками не виявлено (1,88±0,52 та 1,95±0,31 року відповідно). Встановлено, що в осіб віком старше 40 років діагноз СЧВ встановлювався пізніше, ніж в групах до 20 та 20–40 років (рис. 1).
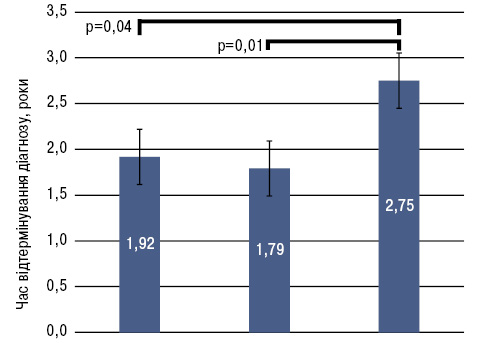
Цей факт підтверджує недостатню ефективність діагностики СЧВ в даній віковій категорії.
Серед проявів захворювання в дебюті найпоширенішими були:
- суглобовий синдром — 77%;
- шкірний висип — 55%;
- сечовий синдром — 20%;
- серозит — 15%.
Відповідно до кожного клінічного прояву пацієнтів було розподілено на дві групи: 1-ша група — наявний конкретний клінічний прояв; 2-га група — відсутній. Надалі порівнювали їх між собою за часом відтермінування діагнозу. Виявлено, що наявність суглобового синдрому подовжувала час діагностичного пошуку більше ніж у 2 рази (зазвичай спрямовуючи його в бік запальних артритів). Натомість при наявності сечового синдрому та серозиту діагноз встановлювався раніше. Щодо шкірного висипу — різниця виявилася недостовірною (рис. 2).
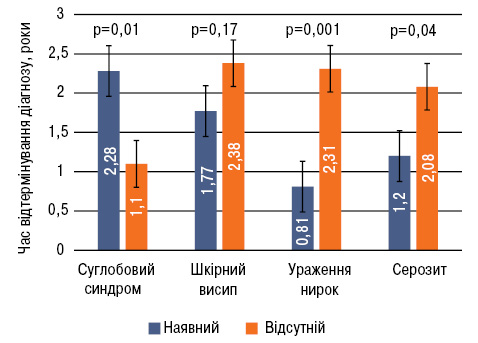
Хоча б один хибний діагноз встановлювався у 59% пацієнтів. Для порівняння у вищезгаданому Британському дослідженні цей показник становив 67% [3]. На рис. 3 наведені найпоширеніші хибні діагнози.
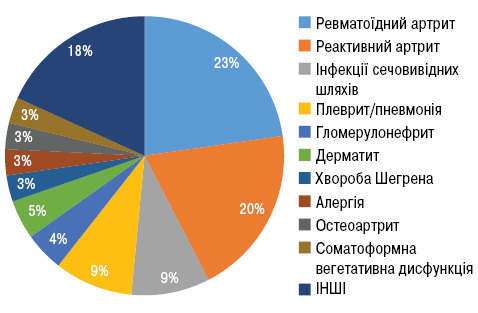
Найпоширенішим хибним діагнозом був ревматоїдний артрит (23%). Примітно, що у 4 із 18 таких пацієнтів відмічено низькопозитивний рівень ревматоїдного фактора в сироватці крові (підвищення не більше ніж у 3 рази). У 14 пацієнтів причиною перегляду діагнозу була поява таких симптомів, як фебрильна лихоманка, шкірний висип, серозит та зміни в загальному аналізі сечі. У 3 пацієнтів був визначений рівень АНА при першому зверненні в наш центр, ще в одного пацієнта — після неотримання відповіді на стандартну терапію. Вищеописане схематично представлено на рис. 4.
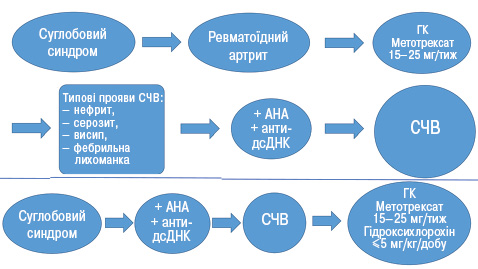
У верхній частині показаний реальний шлях пацієнтів до встановлення діагнозу. У нижній змодельована ідеальна ситуація, коли вже в дебюті визначено рівень АНА, а при їх позитивності — й інших імунологічних маркерів та встановлено діагноз СЧВ.
Бачимо, що в обох випадках базисним препаратом є метотрексат (МТ), і загалом схема лікування є схожою, проте встановлення правильного діагнозу вже в дебюті дає ряд переваг, а саме:
- додавання гідроксихлорохіну, що покращує довготривалий прогноз;
- правильний вибір препаратів другої лінії при неефективності МТ;
- більш ретельний моніторинг виникнення можливих проявів СЧВ.
Серед інших хибних діагнозів, що відмічали в одного-двох пацієнтів, були наступні:
- змішане захворювання сполучної тканини;
- системна склеродермія;
- ревматична поліміалгія;
- ювенільний ревматоїдний артрит;
- анкілозивний спондиліт;
- серонегативний спондилоартрит;
- хвороба Стілла у дорослих;
- геморагічний васкуліт;
- вірусна інфекція Епштейна — Барр;
- лихоманка нез’ясованого генезу;
- міастенія;
- гостре порушення мозкового кровообігу;
- транзиторна ішемічна атака.
Шлях пацієнтів з більш рідкісними первинними проявами можна підсумувати у вигляді схеми, наведеної на рис. 5.
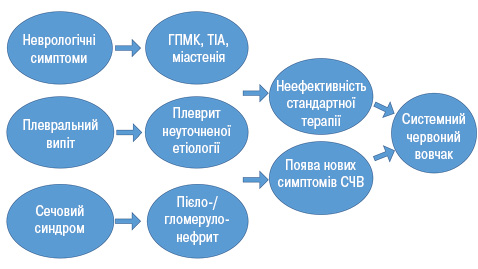
У більшості випадків ключовими моментами, що врешті-решт наштовхували на правильний діагноз, були неефективність терапії чи поява нових симптомів, характерних для СЧВ.
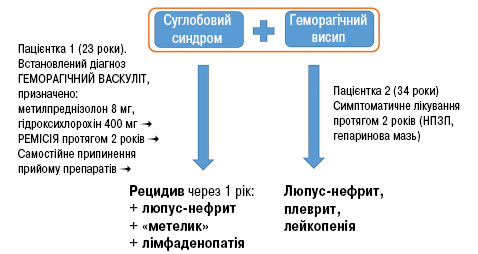
Серед обстежених пацієнтів у 2 виявлено поєднання суглобового синдрому та геморагічного висипу, що є досить рідкісним для СЧВ. На рис. 6 представлені короткі дані про їх шлях до встановлення діагнозу.
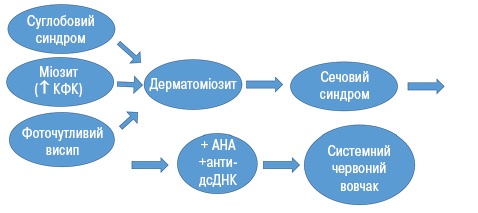
Особливо нетипові прояви СЧВ відмічені у 1 пацієнтки, в якої захворювання дебютувало в 15-річному віці з артриту, міозиту та фоточутливого висипу, на основі чого встановлено діагноз «ювенільний дерматоміозит». Проте через 3 роки приєднався сечовий синдром (який є вкрай рідкісним проявом при дерматоміозиті), а при дообстеженні виявлено підвищення рівня АНА та антитіл до двоспіральної ДНК і встановлено діагноз СЧВ (рис. 7).
На основі даної ситуації варто звернути увагу на два важливі моменти:
- фоточутливий висип є спільним проявом СЧВ і дерматоміозиту;
- при СЧВ можливий істинний міозит з підвищенням рівня креатинфосфокінази (КФК) у сироватці крові (у 3–5% пацієнтів).
Для узагальнення наводимо дані про розподіл пацієнтів залежно від часу відтермінування діагнозу (рис. 8).
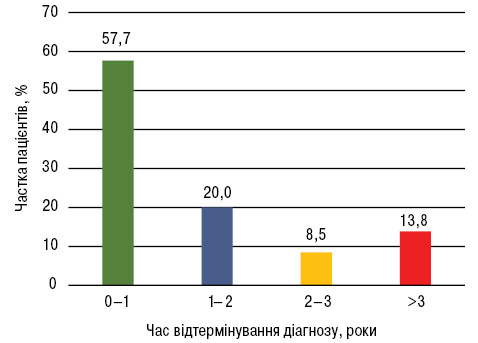
У більшості випадків (57,7%) діагноз встановлювався протягом 1 року від появи симптомів, проте частка пацієнтів з більш тривалою затримкою є досить значною.
Проаналізувавши дані пацієнтів з часом відтермінування більше 3 років, отримали такі результати:
- у 16 пацієнтів захворювання характеризувалося артралгіями чи артритом; у 7 з них встановлено діагноз «ревматоїдний артрит» та призначено базисну терапію;
- 1 пацієнтку протягом 5 років турбували лише шкірний висип за типом «метелика», фотосенсибілізація та виразки в ротовій порожнині, після приєднання артриту та виявлення панцитопенії встановлено діагноз СЧВ;
- у 1 пацієнтки відмічені рецидивуючі тромбози вен нижніх кінцівок, гостре порушення мозкового кровообігу, а діагноз СЧВ із вторинним антифосфоліпідним синдромом встановлено через 6 років (після приєднання ураження нирок).
Позитивним є те, що у пацієнтів з пізнім (>3 років) встановленням діагнозу переважає повільно прогресуючий перебіг, тому в більшості випадків таке відтермінування не веде до критичних негативних наслідків.
ВИСНОВКИ
1. Середній вік встановлення діагнозу серед обстежених пацієнтів становив 26,8 року, що є нижчим порівняно з даними інших країн.
2. Середній час затримки встановлення діагнозу становив 1,94 року (1 рік 11 міс та 1 тиж), що зіставно з міжнародними даними, проте є достовірно більшим у пацієнтів віком старше 40 років. Це потребує більшої настороженості щодо СЧВ у даній віковій категорії.
3. За наявності нефриту та серозиту діагноз СЧВ встановлювався раніше, ніж при їх відсутності. Наявність суглобового синдрому значно збільшувала час встановлення діагнозу, часто спрямовуючи діагностичний пошук в бік запальних артритів.
4. У кожного пацієнта з артритом, ізольованим ураженням серозних оболонок, нирок, нервової системи, а також за наявності шкірного висипу необхідно проводити диференційну діагностику з СЧВ.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- 1. Gergianaki I., Bertsias G. (2018) Systemic Lupus Erythematosus in Primary Care: An Update and Practical Messages for the General Practitioner. Front. Med. (Lausanne), 5: 161.
- 2. Feng X., Zou Y., Pan W. et al. (2014) Associations of clinical features and prognosis with age at disease onset in patients with systemic lupus erythematosus. Lupus, 23: 327–334.
- 3. Sloan M., Harwood R., Sutton S. et al. (2020) Medically explained symptoms: a mixed methods study of diagnostic, symptom and support experiences of patients with lupus and related systemic autoimmune diseases. Rheumatol. Adv. Pract., 26;4(1): rkaa006.
- 4. Pramanik B. (2014) Diagnosis of systemic lupus erythematosus in an unusual presentation: what a primary care physician should know. Curr. Rheumatol. Rev., 10: 81–86.
- 5. Ozbek S., Sert M., Paydas S. et al. (2003) Delay in the diagnosis of SLE: the importance of arthritis/arthralgia as the initial symptom. Acta. Med. Okayama., 57(4): 187–190.
- 6. Petri M., Orbai A.M., Alarcon G.S. et al. (2012) Derivation and validation of the Systemic Lupus International Collaborating Clinics classification criteria for systemic lupus erythematosus. Arthritis. Rheum., 64: 2677–2686.
- 7. British Columbia Medical Association (2013) Antinuclear Antibody (ANA) Testing Protocol: BC Guidelines. British Columbia Medical Association, Canada, 3 p.
- 8. Oglesby A., Korves C., Laliberté F. et al. (2014) Impact of early versus late systemic lupus erythematosus diagnosis on clinical and economic outcomes. Appl. Health Econ. Health Policy, 12(2): 179–190.
- 9. Faurschou M., Dreyer L., Kamper A.L. et al. (2010) Long-term mortality and renal outcome in a cohort of 100 patients with lupus nephritis. Arthritis. Care Res., 62: 873–880.
- 10. Lu X., Gu Y., Wang Y. et al. (2008) Prognostic factors of lupus myelopathy. Lupus, 17: 323–328.
- 11. Nightingale A.L., Davidson J.E., Molta C.T. et al. (2017) Presentation of SLE in UK primary care using the Clinical Practice Research Datalink. Lupus Sci. Med., 4: e000172.
- 12. Dall’Era M., Cisternas M.G., Snipes K. et al. (2017) The Incidence and Prevalence of Systemic Lupus Erythematosus in San Francisco County, California: The California Lupus Surveillance Project. Arthritis. Rheumatol., 69(10): 1996–2005.
АНАЛИЗ ОТСРОЧКИ УСТАНОВЛЕНИЯ ДИАГНОЗА ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧанКЕ
ГУ «ННЦ «Институт кардиологии имени академика Н.Д. Стражеско НАМН Украины», г. Киев
Резюме. Актуальность. Установление диагноза системной красной волчанки (СКВ) часто вызывает значительные трудности и требует участия врачей разных специальностей, проведения большого количества лабораторных и инструментальных исследований. Основными причинами являются гетерогенность клинической картины, возможность вовлечения практически всех органов и систем, недостаточная осведомленность врачей о вариантах дебюта и течения СКВ. Цель. Определить время отсрочки установления диагноза СКВ в разных возрастных категориях и при разных клинических проявлениях в дебюте, обобщить маршруты пациентов до подтверждения диагноза. Методы. Проведен ретроспективный анализ медицинской документации 167 пациентов, находившихся на лечении в ГУ «ННЦ «Институт кардиологии имени академика М.Д. Стражеско НАМН Украины» в период с 2011 по 2020 г. 130 из них оказались достаточно информативными и были включены в анализ. Результаты, установленные в группах исследования, сравнивали с помощью критерия Манна — Уитни. Различия считали статистически значимыми при р<0,05. Результаты. Установлено, что время отсрочки диагноза достоверно выше в возрастной категории старше 40 лет. Выявлено, что наличие артрита в дебюте заболевания удлиняет диагностический поиск, тогда как наличие поражения почек и серозита сокращает. Описан список ложных диагнозов, устанавливаемых пациентам, выделены некоторые типичные маршруты для установления диагноза. Выводы. Полученные данные свидетельствуют о необходимости более высокой настороженности по поводу СКВ у пациентов среднего и пожилого возраста, при наличии суставного синдрома, изолированного поражения отдельных органов с нетипичными проявлениями.
Ключевые слова: системная красная волчанка, отсрочка диагноза, дебют заболевания, антинуклеарные антитела, возрастные категории, ложный диагноз, маршрут пациента.
Адреса для листування:
Проценко Галина Олександрівна
03151, м. Київ, вул. Народного ополчення, 5
ДУ «ННЦ «Інститут кардіології імені академіка
М.Д. Стражеска НАМН України»
E-mail: g_protsenko@yahoo.com

Leave a comment