ВПЛИВ ЮВЕНІЛЬНОЇ ГОСТРОЇ РЕВМАТИЧНОЇ ЛИХОМАНКИ НА ПЕРЕБІГ ХРОНІЧНОЇ РЕВМАТИЧНОЇ ХВОРОБИ СЕРЦЯ У ДОРОСЛИХ пацієнтів
Челпан Л.Л., Прохоров Е.В. , Синяченко О.В.
Резюме. Мета роботи: вивчити клініко-патогенетичний зв’язок хронічної ревматичної хвороби серця (ХРХС) у дорослих із перенесеною гострою ревматичною лихоманкою (ГРЛ) у дитячому віці. Об’єкт і методи: обстежено 97 хворих, 19% з яких перенесли ГРЛ. Вивчали плазмову ланку реологічних властивостей крові та стан ендотеліальної функції судин. Результати. ХРХС, яка дебютувала в дитячому віці з ГРЛ, характеризується пізнішим маніфестним початком пороків серця та меншими темпами їх прогресування, більш рідким розвитком мітрального стенозу, меншою масою міокарда лівого шлуночка і функціональним класом серцевої недостатності, а для ювенільного ревматизму характерний у майбутньому відносно рідкісний розвиток порушень збудливості міокарда й діастолічної дисфункції лівого шлуночка, але типове формування більшої кількості пороків, при цьому віковий диморфізм ХРХС характеризується частотою шлуночкової екстрасистолічної аритмії, параметром товщини лівого шлуночка і лівого передсердя. Висновки: існує диморфізм перебігу ХРХС, дебютом якої була в дитинстві ГРЛ.
Введение
Ревматизм в виде острой ревматической лихорадки (ОРЛ) и хронической ревматической болезни сердца (ХРБС) продолжает занимать ведущие позиции среди наиболее актуальных проблем современной медицины в целом и ревматологии, в частности (Seckeler M.D., Hoke T.R., 2011; Webb R., Wilson N., 2011; Лисенко Г.І., Хіміон Л.В., 2013), поскольку существует четкая связь распространенности заболевания с социально-экономическими факторами (Joseph N. et al., 2013; Longenecker C.T. et al., 2014; Viali S., 2014). ОРЛ и ХРБС значительно ухудшают качество жизни больных (Essawy M.A. et al., 2010; Do Nascimento Moraes A. et al., 2013), причем развитие заболеваний в детском возрасте, якобы, повышает риск смертности у взрослых (Vahanian A. et al., 2011). В некоторых странах ОРЛ является основной причиной смерти детей (Tantchou Tchoumi J.C. et al., 2011; Okello E. et al., 2014), а от ХРБС, согласно разным статистическим данным, в мире регистрируют от 350 до 500 тыс. смертей в год (Azevedo P.M. et al., 2011; Parks T. et al., 2012). В Украине за 7 лет от всех форм ревматизма смертность снизилась на 40,5% (на 80,2% от ОРЛ и на 38,1% — от ХРБС) (Дорогой А.П., 2013), но ХРБС продолжает занимать одно из ведущих мест в стойкой потере трудоспособности больных (Іпатов А.В. та співавт., 2013).
Более 15 млн детей в мире хотя бы раз перенесли ОРЛ (Pelajo C.F. et al., 2010), а у 60–76% из них в последующем сформировалась ХРБС (Ransome O.J., Roode H., 2008; Волосовець О.П., 2010). 84,6% взрослых больных ХРБС перенесли в прошлом один эпизод ОРЛ, а остальные — два и более (Kelmendi M.I., 2009). Замечены особенности течения ХРБС у взрослых, которая началась в детском возрасте (McEnry M., Palloni A., 2010; Barlow J.B., 2012; Toor D., Vohra H., 2012), но клинико-патогенетическая связь с перенесенной ОРЛ остается неизученной. Это стало целью данного исследования.
Объект и методы исследования
Проанализированы результаты наблюдения 97 взрослых пациентов с ХРБС. В разработку не были включены пациенты, которым ранее выполнена хирургическая коррекция порока сердца (протезирование клапанов, аннулопластика, комиссуротомия). 18,6% больных в детском возрасте перенесли ОРЛ (1-я, основная группа), а остальные (81,4%), составившие 2-ю (контрольную) группу, были без ювенильной ОРЛ в анамнезе. Порок сердца еще в детском возрасте сформировался у 60,8% больных, а уже во взрослом — в 39,2%, средний возраст на том этапе в этих подгруппах составил соответственно 12,3±0,42 и 23,8±1,01 года. Необходимо отметить, что порок сердца в детстве был образован у 40,7% мальчиков и 59,3% девочек, а во взрослом возрасте — у 15,8% мужчин и 84,2% женщин (χ=6,70; р=0,010).
Всем пациентам выполняли электрокардиографию (аппараты «МІДАК-ЕК1Т», Украина и «Fukuda Denshi Cardimax-FX326», Япония), эхокардиографию (аппарат «Acuson-Aspen-Siemens», Германия), холтеровское мониторирование (аппарат «Кардиотехника-04-08», Россия) и ультразвуковое исследование периферических сосудов (аппарат «Aplia-XG-Toshiba», Япония). При анализе результатов исследования высчитывали индекс прогрессирования ревматизма (Y) по формуле:
А+В
Y= ________ ,
½С
где А — функциональный класс сердечной недостаточности, В — сумма клинических проявлений кардиальной патологии (частоты различных нарушений возбудимости миокарда, электрической проводимости сердца, изменений толщины миокарда и объема сердечных камер), С — длительность порока сердца.
Митральная недостаточность (МН) установлена в 100,0% наблюдений, аортальная недостаточность (АН) — в 74,2%, митральный стеноз (МС) — в 51,6%, аортальный стеноз — в 22,7%, органическая трикуспидальная недостаточность (ТН) — в 13,4%. Изолированная МН и МН + МС выявлены соответственно у 11,3% больных, МН + АН — у 15,5%, МН + МС + АН — у 27,8%, МН + АН + АС — у 18,6%, МН + МС + АН + ТН — у 8,3%, МН + МС + ТН, МН + АН + АС + ТН и МН + МС + АН + АС — соответственно у 2,1%, МН + ТН — у 1,0%.
Ранее нами (Синяченко и соавт., 2007; Синяченко О.В., 2011) установлена прогностическая значимость при ХРБС нарушений плазменного звена реологических свойств крови (РСК) и эндотелиальной функции сосудов (ЭФС), их взаимосвязи. С учетом сказанного у больных основной и контрольной групп изучены уровни объемной вязкости (ОВ) сыворотки крови (ротационный вискозиметр «Low-Shear-30», Швейцария), модуля вязкоэластичности (ВЭ), поверхностного натяжения (ПН) и времени релаксации (ВР) с помощью компьютерных тензиореометров «ADSA-Toronto» (Германия-Канада) и «PAT2-Sinterface» (Германия), концентрации вискозоопределяющих липидов в крови (холестерина — ХС, триглицеридов — ТГ, липопротеидов низкой плотности — ЛПНП и аполипопротеидов-В — апо-В) с помощью биоанализаторов «BS-200» (Китай) и «Olympus-AU640» (Япония), содержание нитритов (NO2) спектрофотометрически с реактивом Грейса («СФ-46», Россия), показатели эндотелина-1 (ЕТ1), тромбоксана-А2 (ТхА2), простациклина (PgI2) и циклического гуанозинмонофосфата (cGMP) иммуноферментным методом (ридер «PR2100-Sanofi diagnostic pasteur», Франция).
Статистическая обработка полученных результатов исследований проведена с помощью компьютерного вариационного, непараметрического, корреляционного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы «Microsoft Excel» и «Statistica-Stat-Soft», США). Оценивали средние значения (M), их стандартные ошибки (m), критерии дисперсии (D), Стьюдента (t), Уилкоксона — Рао (WR), Макнемара — Фишера (χ) и достоверность статистических показателей (р).
Результаты и их обсуждение
По нашим данным, ОРЛ в детском возрасте способствует в
дальнейшем более позднему формированию пороков сердца, хотя, как известно, циркуляция антистрептококковых антител ускоряет развитие ХРБС (Delunardo F. et al., 2013). К тому же негативными кардиогенными свойствами в отношении развития пороков сердца при ОРЛ обладают антигенные детерминанты сердечного миозина S2 (Ellis N.M. et al., 2010), аутоантиген RHDAG1 (Meng J.X. et al., 2011) и гликопротеин острой фазы фетуин-А (Cagli K., 2010). У больных основной группы Y составляет 2,48±0,229 о.е., а контрольной — 2,04±0,338 о.е. Среди пациентов с ХРБС с пороком в детском возрасте Y был равен 1,76±0,192 о.е., а в остальных случаях — 3,40±0,351 о.е. (t=4,46; p<0,001). Следовательно, развитие порока сердца во взрослом организме является прогнознегативным фактором дальнейшего течения ХРБС.
По данным многофакторного дисперсионного анализа Уилкоксона — Рао, перенесенная ОРЛ мало влияет на последующие интегральные признаки течения болезни. Однофакторный дисперсионный анализ свидетельствует о слабом воздействии ОРЛ на дальнейшие варианты пороков сердца, хотя, по результатам непараметрического анализа Макнемара — Фишера, имеются статистические различия по разнообразию пороков у больных 1-й и 2-й групп (χ=32,77; p=0,012).
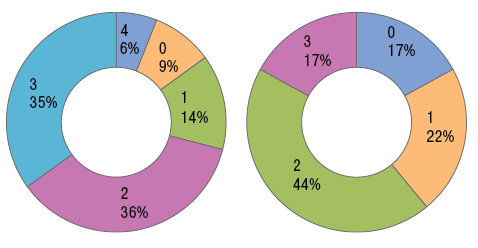
В основной группе развитие МС формируется в 1,7 раза чаще (χ=4,94; р=0,026). В этой связи можно говорить в том, что ОРЛ является определенным предиктором стенозирования левого атриовентрикулярного отверстия. Основная и контрольная группы больных мало отличаются между собой по среднему числу пороков сердца (соответственно 2,58±0,096 и 2,44±0,185), но в 1-й группе функциональный класс сердечной недостаточности в 1,4 раза превышает таковой у больных, не перенесших ОРЛ (t=2,05; p=0,043; χ=29,51; р<0,001; рис. 1). Если комбинированные и сочетанные пороки сердца в основной группе имеют место соответственно у 17,7 и 69,6% обследованных, то в контрольной — у 16,7 и 72,2% (различия с 1-й группой недостоверны).
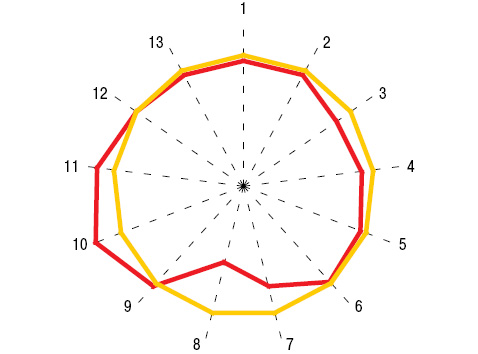
Как показывает ANOVA/MANOVA, перенесенная ОРЛ не оказывает влияния на интегральные электро- и эхокардиографические признаки ХРБС, в том числе на нарушения возбудимости миокарда, электрической проводимости и размеры камер сердца. Развитие трепетания предсердий, наджелудочковой экстрасистолической аритмии и синдрома укорочения PQ наблюдалось в единичных случаях только у пациентов 1-й группы (результаты недостоверны). Следует подчеркнуть, что масса миокарда левого желудочка у представителей основной группы, то есть после перенесенной ОРЛ, оказалась достоверно (на 22%) меньшей (t=2,17; p=0,034).
Возраст пациентов с ХРБС оказывает значительное влияние на интегральные признаки течения заболевания (WR=1,25; p=0,006) и характер пороков сердца (WR=1,39; p=0,006), что демонстрирует многофакторный дисперсионный анализ. По данным ANOVA, возраст пациентов определяет варианты (комбинации) пороков (D=3,05; p=0,002), по которым 1-я и 2-я подгруппы высокодостоверно отличаются (χ=71,39; p<0,001). Если заболевание развилось в детском возрасте, то среднее количество пороков сердца на одного больного составляет 2,39±0,113, тогда как во взрослом возрасте — 1,73±0,136 (t=3,73; p<0,001). По усредненному функциональному классу сердечной недостаточности эти подгруппы между собой не отличаются, но, по данным непараметрической статистики Макнемара — Фишера, интегральный класс в случаях развития ХРБС во взрослом возрасте выше (χ=10,25; р=0,017).
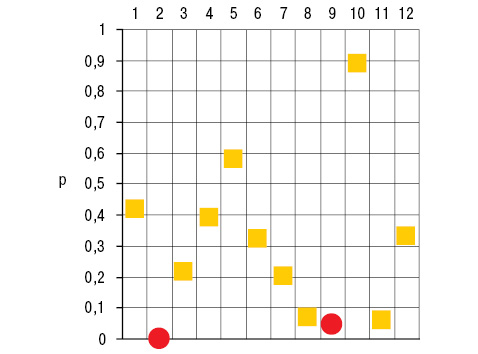
Как видно из рис. 3, у лиц с дебютом болезни в детском возрасте частота развития МС в 1,8 раза реже (χ=13,23; p<0,001), нарушений возбудимости миокарда — в 1,6 раза (χ=4,01; p=0,045), диастолическая дисфункция левого желудочка — в 1,6 раза (χ=4,32; p=0,038). Полученные результаты исследований свидетельствуют о том, что в случаях дебютирования ХРБС у взрослых дальнейшее течение патологического процесса менее благоприятно. Возраст формирования порока сердца оказывает влияние на последующее развитие желудочковой экстрасистолической аритмии (D=3,88; p=0,048), степень гипертрофии миокарда левого желудочка (D=4,42; p=0,038) и левого предсердия сердца (D=11,60; p=0,001), что демонстрирует выполненный дисперсионный анализ. Следует подчеркнуть, что 1-я и 2-я группы больных не отличаются между собой по частоте желудочковой экстрасистолической аритмии и гипертрофии миокарда левого желудочка, но гипертрофия левого предсердия у пациентов с эволюцией болезни из ювенильной оказалась в 2,3 раза более редкой (χ=20,62; p<0,001). Последний факт объясняется меньшей частотой формирования у таких пациентов МС.
За последние годы улучшилось понимание патогенеза ревматизма, но многие вопросы остаются невыясненными (Carapetis J.R., Zühlke L.J., 2011; Toor D., Vohra H., 2012; Tandon R. et al., 2013). ХРБС свойственен повышенный уровень ЕТ1 в крови, а эндотелиальная дисфункция сосудов (ЭДС) участвует в патогенетических построениях заболевания, в частности в формировании митрально-аортальных сочетанных пороков сердца (Moura E.B. et al., 2010). Установлено, что такой реологический показатель, как ОВ, самым тесным образом связан с ЭФС, процессами вазоконстрикции/вазодилатации (Baskurt O.K., 2008).
Разнообразный спектр стрептококковых антигенов при ОРЛ вызывает синтез противоэндотелиальных aнтител, усугубляя у таких больных ЭДС (Mirabel M. et al., 2012; Delunardo F. et al., 2013). У 40,0% пациентов с ХРБС в сыворотке крови выявляют антиэндотелиальные антитела (Scalzi V. et al., 2010). Как демонстрирует выполненный нами ANOVA/MANOVA, перенесенная ОРЛ в детском возрасте оказывает существенное влияние на интегральное состояние РСК и ЭФС у взрослых пациентов с ХРБС. Однофакторный ANOVA продемонстрировал зависимость от характера пороков сердца параметров ОВ (D=7,78; p=0,019), ВЭ (D=3,07; p=0,018), ПН (D=6,46; p=0,001), ВР (D=25,92; p<0,001) и PgI2 (D=6,16; p=0,017), а показателей простациклинемии и вторичного мессенджера системы оксида азота cGMP — от перенесенной ОРЛ (соответственно D=17,05; p<0,001 и D=3,73; p=0,045). Необходимо отметить, что в основной группе больных оказались на 18% большими значения ОВ (t=2,97; p=0,004), что нашло отражение в таблице.
основной и контрольной групп (M±m)
| Показатель | Группа | Отличия | ||
|---|---|---|---|---|
| основная(n=38) | контрольная(n=59) | t | p | |
| ОВ, мПа · с
ВЭ, мН/м ПН, мН/м ВР, с ХС, ммоль/л ТГ, ммоль/л ЛПНП, ммоль/лАпо-В, г/л ЕТ1, пг/мл ТхА2, нг/мл PgI2, нг/мл NO2, мкмоль/л cGMP, пмоль/мл |
2,6±0,13
25,9±0,60 47,2±0,73 107,2±3,67 5,3±0,21 2,2±0,22 2,0±0,29 1,0±0,07 6,2±0,27 12,8±0,79 25,3±1,63 5,6±0,16 13,8±0,36 |
2,2±0,07
24,9±0,55 46,9±0,74 105,5±3,28 5,5±0,17 2,2±0,15 2,4±0,23 1,1±0,06 6,0±0,25 13,6±0,80 29,0±1,49 5,9±0,13 12,9±0,33 |
2,97
1,23 0,23 0,34 0,52 0,19 0,99 1,07 0,36 0,68 1,58 1,57 1,76 |
0,004
0,220 0,816 0,732 0,602 0,850 0,327 0,286 0,721 0,501 0,117 0,119 0,082 |
Отметим, что высказанная ранее гипотеза о негативной роли перенесенной ОРЛ в детском возрасте в отношении дальнейшей ХРБС оказалась преувеличенной. Более того, существует некое своеобразное тормозящее влияние ОРЛ на темпы дальнейшего формирования и прогрессирования пороков сердца. Предположительно, в детском возрасте ОРЛ способна уменьшать выраженность процессов антителообразования к антигенам клапанов сердца, угнетать продукцию провоспалительных цитокинов, факторов роста, ядерного фактора NFκB в клапанном аппарате (Mohamed A.A. et al., 2010; Delunardo F. et al., 2013).
В заключение отметим, что распределение нами пациентов с ХРБС на представленные две группы весьма условно, поскольку на современном этапе отмечается тенденция к более скрытому, малосимптомному течению ОРЛ с латентно протекающим кардитом без артрита, хореи, эритемы и ревматических узлов — диагностических проявлений ОРЛ. Об этом косвенно свидетельствует тот факт, что у 2–8% детей c ХРБС ревматические пороки сердца определяют случайно при эхокардиографическом исследовании (Bhaya M. et al., 2010; Ozdemir O. et al., 2011; Webb R.H. et al., 2011). Конечно, перечисленные признаки остаются очень специфичными для ОРЛ, но сейчас становятся малоинформативными в отношении диагностической значимости вследствие крайне низкой их чувствительности (частоты выявления). Разработку новых диагностических критериев ОРЛ, возможно, предстоит решить в ближайшем будущем.
Выводы
Таким образом, ХРБС, которая дебютировала в детском возрасте с ОРЛ, характеризуется более поздним манифестным началом пороков сердца и меньшими темпами их прогрессирования, более редким развитием МС, меньшими массой миокарда левого желудочка и функциональным классом сердечной недостаточности, а для ювенильного ревматизма характерно в будущем относительно редкое развитие нарушений возбудимости миокарда и диастолической дисфункции левого желудочка, но типично формирование большего числа пороков, при этом возрастной диморфизм ХРБС характеризуется частотой желудочковой экстрасистолической аритмии, параметрами толщины левого желудочка и левого предсердия.
Список использованной литературы
- Волосовець О.П. (2010) Гостра ревматична лихоманка як проблема сучасної дитячої ревматології. Здоровье ребенка, 24 (3): 3–11.
- Дорогой А.П. (2013) Динаміка та структура смертності населенні України при гострій ревматичній гарячці та хронічних ревматичних хворобах серця. Укр. ревматол. журн., 53 (3): 120–121.
- Іпатов А.В., Лисунець О.М., Ханюкова І.Я. та ін. (2013) Первинная інвалідність в Україні внаслідок гострої ревматичної гарячки та хронічних ревматичних хвороб серця. Укр. ревматол. журн., 53 (3): 127–128.
- Лисенко Г.І., Хіміон Л.В. (2013) Сучасні проблемні питання гострої ревматичної лихоманки. Укр. ревматол. журн., 54 (4): 4–12.
- Синяченко О.В., Ермолаева М.В., Мартыненко Т.В. и др. (2007) Клинико-патогенетическое значение эндотелиальной дисфункции и ее коррекция при хронической ревматической болезни сердца. Укр. тер. журн., 3: 4–7.
- Синяченко О.В. (2011) Адсорбционно-реологические свойства биологических жидкостей в ревматологии. Донеччина, Донецк, 286 с.
- Azevedo P.M., Pereira R.R., Guilherme L. (2011) Understanding rheumatic fever. Rheumatol. Int., 28 (9): 67–73.
- Barlow J.B. (2012) Aspects of active rheumatic carditis. Aust. NZ J. Med., 22 (5): 592–600.
- Baskurt O.K. (2008) In vivo correlates of altered blood rheology. Biorheology, 45 (6): 629–638.
- Bhaya M., Panwar S., Beniwal R. et al. (2010) High prevalence of rheumatic heart disease detected by echocardiography in school children. Echocardiography, 27 (4): 448–453.
- Cagli K. (2010) Association of serum fetuin-A with valvular calcium concentration in rheumatic mitral valve disease. J. Heart Valve Dis., 19 (5): 636–643.
- Carapetis J.R., Zühlke L.J. (2011) Global research priorities in rheumatic fever and rheumatic heart disease. Ann. Pediatr. Cardiol., 4(1): 4–12.
- Delunardo F., Scalzi V., Capozzi A. et al. (2013) Streptococcal-vimentin cross-reactive antibodies induce microvascular cardiac endothelial proinflammatory phenotype in rheumatic heart disease. Clin. Exp. Immunol., 173(3): 419–429.
- Do Nascimento Moraes A., Ramos Ascensão Terreri M.T., Esteves Hilário M.O. et al. (2013) Health related quality of life of children with rheumatic heart diseases: reliability of the Brazilian version of the pediatric quality of life inventory™ cardiac module scale. Health Qual. Life Outcomes, 15(11): 198–202.
- Ellis N.M., Kurahara D.K., Vohra H. et al. (2010) Priming the immune system for heart disease: a perspective on group A streptococci. J. Infect. Dis., 202(7): 1059–1067.
- Essawy M.A., Bahgat Z.S., Kassem H.A. (2010) Health-related quality of life of school- age children with rheumatic fever. J. Egypt Public. Health Assoc., 85(3–4): 205–222.
- Joseph N., Madi D., Kumar G.S. et al. (2013) Clinical spectrum of rheumatic Fever and rheumatic heart disease: a 10 year experience in an urban area of South India. N. Am. J. Med. Sci., 5(11): 647–652.
- Kelmendi M.I. (2009) Rheumatic fever in Kosoava — long-term study. Med. Arh., 63(4): 231–233.
- Longenecker C.T., Okello E., Lwabi P. et al. (2014) Management of rheumatic heart disease in uganda: the emerging epidemic of non-AIDS comorbidity in resource-limited settings. J. Acquir. Immune Defic. Syndr., 65(2): 79–80.
- McEnry M., Palloni A. (2010) Early life exposures and the occurrence and timing of heart disease among the older adult Puerto Rican population. Demography, 47(1): 23–43.
- Meng J.X., Li Y.X., Zhu P. et al. (2011) Screening and identification of auto-antigen RHDAG1 of rheumatic heart disease. Nan Fang Yi Ke Da Xue Xue Bao, 31 (7): 1154–1158.
- Mirabel M., Ferreira B., Sidi D. et al. (2012) Rheumatic heart disease: future prospects. Med. Sci., 28(6–7): 633–638.
- Mohamed A.A., Rashed L.A., Shaker S.M. et al. (2010) Association of tumor necrosis factor-alpha polymorphisms with susceptibility and clinical outcomes of rheumatic heart disease. Saudi Med. J., 31(6): 644–649.
- Moura E.B., Gomes M.R., Corso R.B. et al. (2010) Amplification of the genes that codify endothelin-1 and its receptors in rheumatic mitral valves. Arq. Bras. Cardiol., 95(1): 122–130.
- Okello E., Beaton A., Mondo C.K. et al. (2014) Rheumatic heart disease in Uganda: the association between MHC class II HLA DR alleles and disease: a case control study. BMC Cardiovasc. Disord., 14(1): 28–33.
- Ozdemir O., Oguz D., Atmaca E. et al. (2011) Cardiac troponin T in children with acute rheumatic carditis. Pediatr. Cardiol., 32(1): 55–58.
- Parks T., Smeesters P.R., Steer A.C. (2012) Streptococcal skin infection and rheumatic heart disease. Curr. Opin. Infect. Dis., 25(2): 145–153.
- Pelajo C.F., Lopez-Benitez J.M., Torres J.M. et al. (2010) Adherence to secondary prophylaxis and disease recurrence in 536 Brazilian children with rheumatic fever. Pediatr. Rheumatol. Online J., 26(8): 22–30.
- Ransome O.J., Roode H. (2008) Rheumatic fever in an urban community. S. Afr. Med. J., 73(3): 154–156.
- Scalzi V., Hadi H.A., Alessandri C. et al. (2010) Anti-endothelial cell antibodies in rheumatic heart disease. Clin. Exp. Immunol., 161(3): 570–575.
- Seckeler M.D., Hoke T.R. (2011) The worldwide epidemiology of acute rheumatic fever and rheumatic heart disease. Clin. Epidemiol., 22(3): 67–84.
- Tandon R., Sharma M., Chandrashekhar Y. et al. (2013) Revisiting the pathogenesis of rheumatic fever and carditis. Nat. Rev. Cardiol., 10(3): 171–177.
- Tantchou Tchoumi J.C., Ambassa J.C., Kingue S. et al. (2011) Occurrence, aetiology and challenges in the management of congestive heart failure in sub-Saharan Africa: experience of the cardiac centre in shisong, Cameroon. Pan. Afr. Med. J., 8(11): 175–179.
- Toor D., Vohra H. (2012) Immune responsiveness during disease progression from acute rheumatic fever to chronic rheumatic heart disease. Microbes Infect., 14(12): 1111–1117.
- Vahanian A., Garbarz E., Iung B. (2011) Acquired childhood heart diseases in developing countries. Bull. Acad. Natl. Med., 195(2): 315–325.
- Viali S. (2014) Rheumatic heart disease in Samoa and the pacific nations. J. Prim. Health Care., 6(1): 84–85.
- Webb R.Н., Wilson N.J. (2011) Rheumatic fever in New Zealand. J. Paediatr. Child. Health, 10(11): 1440–1454.
- Webb R.H., Wilson N.J., Lennon D.R. et al. (2011) Optimising echocardiographic screening for rheumatic heart disease in New Zealand: not all valve disease is rheumatic. Cardiol. Young., 21(4): 436–443.
Адрес для переписки:
Синяченко Олег Владимирович
Е-mail: synyachenko@ukr.net

Leave a comment