ГРАНУЛЕМАТОЗНЕ ЗАПАЛЕННЯ ЯК ОСНОВА ДЕЯКИХ РЕВМАТОЛОГІЧНИХ ЗАХВОРЮВАНЬ
Казимирко В.К., Иваницкая Л.Н. , Дубкова А.Г. , Силантьева Т.С., Кутовой В.В.
Резюме. Резюме. У роботі наведено характеристику гранулематозного запалення при деяких ревматологічних захворюваннях. Гранульоми розвиваються за участю імунопатологічних механізмів, і блокувати ланки розвитку гранулематозного процесу на молекулярному рівні можна за допомогою антицитокінових засобів. Антицитокінові засоби на сьогодні ефективно застосовуються при ревматоїдному артриті, але вони, очевидно, перспективні й щодо інших гранулематозних захворювань у ревматологічній практиці.
ВВЕДЕНИЕ
Образование гранулем — это способ изоляции патогенных веществ, которые фагоциты не в состоянии расщепить, удалить из ткани. В этом процессе важную роль играют такие цитокины макрофагов, как фактор некроза опухоли-α, интерлейкин-1. В настоящее время насчитывают более 70 нозологических форм гранулематозных болезней (ГБ). Их объединяют по нозологическому и этиологическому принципу в четыре группы [9]: ГБ инфекционной, неинфекционной, неустановленной этиологии, медикаментозные. К группе ГБ неинфекционной этиологии относят [6, 9] подагру. Из ГБ инфекционной этиологии к компетенции ревматологов относится острая ревматическая лихорадка. Из ГБ неустановленной этиологии ревматологи чаще всего имеют дело с ревматоидным артритом (РА), гигантоклеточным артериитом, гранулематозом Вегенера, синдромом Черджа — Стросс, артериитом Такаясу, идиопатическим церебральным ангиитом, панникулитом типа Вебера — Крисчена [1, 3]. Врачи-ревматологи участвуют в лечении таких ревматических проявлений ГБ, как саркоидоз и болезнь Крона.
Исходом гранулем может быть: 1) рассасывание инфильтрата; 2) казеозный некроз; 3) нагноение, формирование абсцесса в гранулеме; 4) образование на месте гранулемы рубца или фиброзного узелка; 5) формирование на месте гранулемы псевдоопухоли. Ярким примером трансформации гранулем (то есть атером, бляшек) служит атеросклероз.
Подагра
Подагра характеризуется отложением в коже, хрящах, эпифизах костей, околосуставных тканях, почках, интиме венечных артерий, клапанах, в миокарде, перикарде микрокристаллов уратов. Отложения повреждают ткани, активируют продукцию фагоцитами медиаторов воспаления, инициируют хроническое пролиферативное воспаление с формированием гранулем [9]. Развивается макрофагально-гистиоцитарная инфильтрация с большим количеством гигантских клеток инородных тел, фагоцитирующих кристаллы уратов. Вокруг кристаллов возникает пролиферативное гранулематозное воспаление. Таким образом подагрические гранулемы (тофусы) — это скопления кристаллов мочевой кислоты и ее солей (чаще натриевой), окруженные фиброзной капсулой с включениями макрофагов, гигантских клеток (рис. 1).
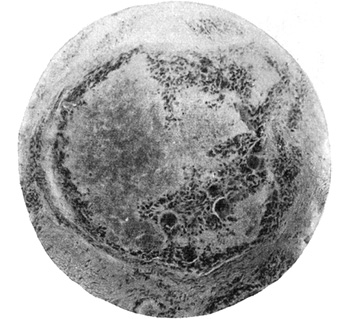
В субхондральных отделах костей гранулемы вызывают деструкцию костной ткани, в интерстициальной ткани почек — нефропатию. Грануляционная ткань в виде паннуса «наползает» на суставной хрящ, субхондральные отделы кости. Отложение уратов в интерстиции почек, эпителии канальцев приводит к развитию абактериального пиелонефрита, а затем нефросклероза, подагрически сморщенной почки и хронической почечной недостаточности. Кристаллизация урата натрия в канальцах, лоханках, мочеточниках приводит к нарушению оттока мочи. Кроме уратных камней, образуются кальциевые конкременты. Микротофусы возникают в хрящах и других соединительнотканных образованиях. Под влиянием провоцирующих факторов увеличивается гиперурикемия, освобождение уратов, депонированных в хряще. Они появляются в синовиальной жидкости, фагоцитируются лейкоцитами, в результате возникает острый синовит.
Кристаллы урата мононатрия преимущественно откладываются в бессосудистых тканях (хрящах), слабо васкуляризованных (связки, сухожилия), сильно охлаждающихся местах — в дистальных суставах, ушных раковинах. При отсутствии лечения гранулемы-тофусы в среднем образуются через 10 лет после приступа подагры. Они чаще располагаются в синовиальной ткани; субхондральных отделах костей; в области суставов кистей и стоп, сумки локтевого отростка; на разгибательной поверхности предплечья; в области ахиллова сухожилия; реже — в области ушных раковин. Целостность тофуса может нарушиться, и его содержимое выходит наружу. Раннее появление тофусов характерно для ювенильной подагры, заболеваний почек, сопровождающихся выраженной гиперурикемией, женщин пожилого возраста, принимающих диуретики, миелопролиферативных заболеваний. Тофусы могут образовываться до развития артрита, что наблюдается у женщин пожилого возраста с почечной недостаточностью, принимающих диуретики. В число подагрических висцеропатий входит гепатопатия вследствие образования в ней подагрических гранулем. Возникают митральная недостаточность, АВ-блокады различной степени, экстрасистолия, тахикардия. Часто имеется сочетание с коронарным атеросклерозом и ишемической болезнью сердца, которые у пациентов с подагрой начинаются в более молодом возрасте и протекают более тяжело. К рентгенологическим признакам, характерным для подагры, относятся отек мягких тканей, тофусы, эрозии и сужение суставной щели. Тофусы на рентгенограмме видны как очаги неравномерного уплотнения мягких тканей, в которых иногда откладывается кальций. Костные эрозии имеют «штампованную» форму (симптом «пробойника») со склеротической каемкой и нависающими краями, образующимися при разрушении коркового вещества кости (симптом «вздутия костного края») иногда эти эрозии называют «крысиными укусами». Подагрические тофусы могут образовываться в узелках Гебердена. Размеры тофусов варьируют от 1 мм до 5 см, они могут сливаться и образовывать конгломераты. Известно, что значительное уменьшение концентрации мочевой кислоты в сыворотке крови способствует резорбции уратов из тофусов. Поэтому концентрацию мочевой кислоты в сыворотке крови рекомендуется поддерживать как минимум на 1,0 мг/дл ниже верхней границы нормы (6,8 мг/дл). Положительный результат наступает при длительном лечении аллопуринолом.
Острая ревматическая лихорадка
Иммунный воспалительный процесс при острой ревматической лихорадке приводит к дезорганизации соединительной ткани, которая происходит в несколько этапов [5–7, 9]. На одной из стадий воспалительного процесса формируются специфические ревматические гранулемы (табл. 1).
| Стадии воспалительного процесса | Характеристика патологического процесса |
|---|---|
| Мукоидное набухание | Деполимеризуется основное вещество соединительной ткани, в нем накапливаются мукополисахариды (в основном кислые). Соединительная ткань разволокняется. Патологический процесс обратим |
| Фибриноидный некроз |
Наступает глыбчатый распад коллагена, дезорганизация коллагеновых волокон, их набухание, отложение фибриноида. Процесс необратим |
| Формирование специфических ревматических гранулем |
Гранулемы формируются вокруг очагов фибриноидного некроза и представлены крупными базофильными гистиоцитами, базофилами, моноцитами, лимфоцитами, плазматическими клетками |
| Стадия склероза | Исход гранулемы |
Одновременно с гранулемами в ткани отмечают проявления неспецифического воспаления. Ревматические гранулемы возникают в сердце, располагаются в периваскулярной соединительной ткани или в интерстиции миокарда с преимущественной локализацией в левом желудочке, перегородке, сосочковых мышцах, эндокарде, наружной оболочке сосудов. Они состоят из базофильных клеток (крупных, неправильной формы) гистиоцитарного происхождения; гигантских многоядерных клеток; лимфоидных, плазматических и тучных клеток. Цикл формирования и рубцевания гранулемы занимает в среднем 3–4 мес. Исходом имевшегося вальвулита является кардиосклероз. Дезорганизация соединительной ткани, экссудативное воспаление, васкулит наблюдаются в суставных тканях, сосудах мозга. Изменения клеток полосатого тела, субталамических ядер большого мозга и мозжечка являются причиной возникновения малой хореи. Васкулит, очаговая воспалительная реакция являются причиной поражения кожи и подкожной клетчатки.
Ра
Характерным проявлением РА как ГБ являются ревматоидные узелки и ревматоидные гранулемы, разрушающие кости суставов [5–7, 9]. Узелки — это соединительнотканные плотные образования округлой формы диаметром от нескольких миллиметров до нескольких сантиметров. Они безболезненны, подвижные, но иногда могут быть спаяны с костью или апоневрозом. Бывают единичными, множественными, симметричными, асимметричными. Как правило, узелки развиваются у больных с высоким титром ревматоидного фактора и в 20–35% случаев локализуются на разгибательной поверхности предплечья (рис. 2). Могут располагаться в области затылка, голосовых связок, крестца, в миокарде, клапанных структурах, в легких, центральной нервной системе (ЦНС). Появляются в период обострения и исчезают в период ремиссии (раннее появление считается прогностически неблагоприятным фактором). Выделяют так называемый ревматоидный нодуллез, когда множественные ревматоидные узелки сочетаются с: 1) выраженным синовитом; 2) субхондральными кистозными изменениями мелких суставов кистей и стоп; 3) высоким титром ревматоидного фактора.
Ревматоидные узелки являют собой зону фибриноидного некроза, которая окружена гистиоцитами (вытянутой формы) и клетками соединительной ткани по периферии. Множественные ревматоидные узелки могут развиваться в легких. Они располагаются в периферических отделах легких, могут распадаться с образованием бронхоплевральных свищей. При силикозе могут определяться округлые, многочисленные очаги диаметром 0,5–5 см на периферии легких (синдром Каплана). Миокардит бывает как интерстициальный, так и гранулематозный. Тяжелое поражение с развитием сердечной недостаточности развивается редко. Гранулематоз эндокарда ведет к формированию пороков сердца. Гранулематоз поражает стенки аорты (выслушивается систолический шум над аортой), а также склеры.

Гранулематозный васкулит
Гранулематозное воспаление имеет место при неспецифическом аортоартериите, гигантоклеточном (височном) артериите, изолированном ангиите ЦНС, гранулематозе Вегенера, синдроме Черджа — Стросс [4, 8, 9, 16], вторичном аортите — ревматоидном, туберкулезном, сифилитическом. При гранулематозном воспалении, синдроме Черджа — Стросс имеет место продукция антител к лизосомным ферментам нейтрофилов (ANCA). В биоптатах тканей при гранулематозном васкулите выявляют характерные изменения (табл. 2).
| Васкулит | Место взятия биоптата, другие методы диагностики | Характер клеточной инфильтрации в биоптатах |
|---|---|---|
| Синдром Черджа — Стросс | Биопсия пораженных органов (обычно легких) | Гранулематозные эозинофильные инфильтраты |
| Гранулематоз Вегенера | Биопсия легких, ANCA | Некротизирующиеся гранулемы в верхних и нижних дыхательных путях. Некротизирующий очаговый артериит в легких, некротизирующий гломерулонефрит |
| Гигантоклеточный артериит | Биопсия височных артерий | Гигантоклеточные инфильтраты в стенках сосудов |
| Болезнь Такаясу | Ангиография, МРТ грудной клетки | Гигантоклеточные инфильтраты в стенках сосудов |
| Изолированный васкулит ЦНС | Биопсия мозговых оболочек или пораженных участков мозга | Гранулематозное воспаление мелких и средних артерий мозга |
Гигантоклеточный артериит
Гигантоклеточный артериит характеризуется гранулематозным воспалением аорты и ее основных ветвей — преимущественно внечерепных ветвей сонной артерии, височной, позвоночной или других [9, 11, 15]. Чаще всего поражается височная артерия. Возможно развитие продуктивного флебита, тромбофлебита. При гистологическом исследовании пораженных артерий выявляют очаги некроза во внутреннем и мышечном слое стенки артерий среднего калибра; деструкцию эластической мембраны; инфильтрацию лимфоцитами всех слоев стенки артерий; гранулемы вокруг очагов деструкции, содержащие макрофаги, гигантские многоядерные клетки, лимфоциты; утолщение интимы; пристеночный тромбоз; сужение/обтурацию просвета артерий.
Артериит Такаясу
Гранулематозное воспаление поражает аорту и ее основные ветви, приводит к окклюзии и отсутствию пульса на руках [9, 12, 15]. Оно локализуется в наружных слоях медии и адвентиции. В гранулемах определяют скопления макрофагов, лимфоцитов и гигантских многоядерных клеток. Воспаление сопровождается фиброзом гранулем, склерозированием и повреждением медии, разрушением эластических мембран, пролиферацией эндотелия, сужением просвета сосудов. У пациентов с артериитом Такаясу выявляют очаги некроза в средней оболочке сосудов; вокруг них располагаются клеточные инфильтраты, состоящие из макрофагов, гигантских многоядерных лимфоидных клеток, плазмоцитов; клеточная инфильтрация распространяется на все оболочки сосудистой стенки; отмечаются разрастания интимы, тромбозы; прогрессирующий склеротический процесс приводит к окклюзии просвета артерий. Описанные изменения выражены в местах отхождения артерий от аорты, в том числе от ее брюшного отдела. Внутриорганные артерии подобным изменениям не подвергаются. Следствием сужения просвета сосудов является тромбообразование. Поражаются vasa vasorum, нарушается кровоток в различных органах.
Морфологические изменения при артериите Такаясу и гигантоклеточном артериите идентичны, различия состоят только в локализации гранулематозного воспаления. При гигантоклеточном артериите преимущественно поражается сонная артерия, ее ветви.
Гранулематоз Вегенера
Для заболевания характерно наличие некротизирующего артериита, поражающего систему дыхания и почки; изъязвление слизистой оболочки носовых пазух, носоглотки, гортани, трахеи; развитие некротических гранулем с участками некроза, напоминающими географическую карту; поражение почек — гломерулонефрит (с образованием полулуний); выявление у 70% пациентов сANCA; быстрое прогрессирование болезни при отсутствии лечения, развитие почечной недостаточности; высокая эффективность циклофосфамида [5, 9, 14, 17]. В генезе и обострении болезни предполагается этиологическая роль инфекции. Некротизирующий васкулит с эрозивно-язвенным поражением верхних дыхательных путей может возникнуть после применения сульфаниламидов, антибиотиков, противотуберкулезных средств, дифенилгидантоина, введения противостолбнячной сыворотки, длительного приема наркотиков. Значение имеет и идиосинкразия к сывороткам, вакцинам. В стенках мелких артерий и вен, а также в окружающих тканях выявляют воспалительные гранулемы. Некротический васкулит, гранулемы, полости выявляются в ткани легких. Вследствие воспаления, фиброза и рубцевания развивается обструкция бронхов. Гранулематозное воспаление и некроз (с васкулитом или без) имеется в слизистой оболочке верхних дыхательных путей, придаточных пазух носа, в носоглотке. В почках гранулемы определяются редко, сначала появляются морфологические признаки очагового гломерулонефрита, а затем экстракапиллярного. Гранулемы в пищеварительном тракте и дыхательных путях некротизируются (в них мало клеток фибробластического ряда), в печени и почках — рубцуются. Следствием хронического гранулематозного воспаления может явиться стеноз гортани и трахеи со стридорозным дыханием и дыхательной недостаточностью. В ткани легкого возникает воспалительный процесс, который протекает остро или хронически. В периваскулярном пространстве интерстициальной ткани и перегородок альвеол образуются воспалительные гранулемы (узелки). Они могут располагаться в стенках сосудов и бронхах. Очаги острого и хронического воспаления рассасываются без образования рубца или с отложением в этих участках коллагена.
При гистологическом исследовании легких выявляют характерную триаду признаков: некротические полиморфно-клеточные гранулемы, васкулит, очаги некроза. Гранулемы имеют неправильную форму, содержат нейтрофилы, лимфоциты, плазматические клетки, макрофаги, гигантские многоядерные клетки, эозинофилы. Гистиоциты вокруг очагов некроза образуют характерные «палисадные» структуры. Очаги некрозов определяются в гранулемах и легочной ткани. За счет большого количества разрушенных ядер клеток очаги некроза обладают базофилией. Они напоминают микроабсцессы. К предполагаемым причинам некроза относят активацию нейтрофилов и ишемию.
Cиндрома Черджа — Стросс представляет собой гранулематозный некротизирующий васкулит, для которого характерно поражение мелких и средних сосудов, развитие воспаления верхних дыхательных путей, аллергического ринита, эозинофилии, бронхиальной астмы [6, 9, 13, 17]. Раньше синдром расценивался как астматический вариант узелкового полиартериита. В стенках сосудов и периваскулярно развиваются эозинофильные инфильтраты. Важную патогенетическую роль в его развитии играют антинейтрофильные цитоплазматические антитела. Отличительные признаки, характерные для синдрома Черджа — Стросс: поражаются артерии (среднего и мелкого калибра, как при узелковом полиартериите), артериолы, капилляры (в том числе почечных клубочков), венулы и вены; у 70% пациентов определяют рANCA; воспаление имеет гранулематозный характер. К данным, позволяющим установить диагноз синдрома Черджа — Стросс, относят: симптомы аллергии или бронхиальной астмы в анамнезе; эозинофилию; инфильтраты в легких; полиорганное поражение; гранулематозное воспаление сосудов и эозинофильную инфильтрацию тканей (биопсия). Морфологические проявления, присущие синдрому Черджа — Стросс, включают: некротический васкулит мелких артерий и вен; мелкие некротические гранулемы, экстраваскулярно расположенные по отношению к артериям и венам малого калибра; характерное строение гранулемы: центральное эозинофильное ядро и окружающие его радиально расположенные макрофаги и гигантские многоядерные клетки; преобладание среди воспалительных элементов эозинофилов.
Церебральный ангиит
В основе церебрального ангиита лежит гранулематозное воспаление мелких и средних артерий мозга [9, 10]. Синонимами термина «церебральный ангиит» являются «изолированный ангиит ЦНС», «первичный васкулит (ангиит) ЦНС», «идиопатический васкулит (ангиит) ЦНС». Эта форма васкулита относится к редким заболеваниям. При люмбальной пункции у больных выявляют признаки хронического менингита. При гистологическом исследовании биоптатов определяют воспаление сосудов, лейкоцитарную инфильтрацию с преобладанием лимфоцитов, нередко — гранулемы, что свидетельствует о пролиферативном характере воспаления. Заболевание проявляется одним из нижепредставленных синдромов: 1) многоочаговой симптоматикой, напоминающей рассеянный склероз; 2) энцефалопатией (острой и подострой), проявляющейся психопатологическими нарушениями; 3) общемозговой или очаговой симптоматикой, имитирующей опухоль головного мозга и быстро прогрессирующей. Диагноз устанавливают на основании результатов церебральной ангиографии и биопсии ткани мозга и мозговых оболочек. Также исключаются другие причины стенозирования мозговых артерий.
Панникулит
Для панникулита характерно системное поражение жировой ткани (являющейся разновидностью соединительной) средостения, эпикарда, большого сальника и др. [2, 6, 9]. Повышенный липолиз и ангиоспастический синдром сопровождаются ишемией жировой ткани, нарушением структуры коллагена, дифференциации жировых клеток соединительной ткани, развитием воспалительного процесса, появлением участков некроза. В дальнейшем на месте некротических очагов возникает фиброзная ткань. Возможно развитие жировой дистрофии печени, почек, сердечно-сосудистой системы. В основе заболевания лежит васкулит мелких сосудов жировой ткани с развитием некроза жировых клеток и фиброзной ткани. Выделяют подкожную и системную формы болезни. Характерно острое начало, напоминающее инфекционное заболевание. Появляются узлы различного размера — от 1 до 1,5 см, локализующиеся на конечностях, бедрах и туловище, реже — на лице, голове, кистях, щеках, грудных железах. Они единичные или множественные, имеют различную форму (чаще круглую), при пальпации болезненные, кожа над ними горячая на ощупь, синюшно-красная. Узлы могут образовывать конгломераты — крупные бляшки неправильной формы, расположенные глубоко в подкожной клетчатке. Узлы вначале плотные, затем они становятся мягкими, появляется флюктуация, их содержимое прорывается кнаружи в виде желтоватой пенистой массы. В дальнейшем эти участки кожи атрофируются, она втягивается, появляется пигментация, может откладываться кальций. Следует учитывать возможные варианты поражения жировой клетчатки: средостения, эпикарда, брыжейки кишечника, кишечника, сальника, забрюшинной, околопочечной, орбиты глаза и др. Воспалительная инфильтрация, очаги некроза с дальнейшим атрофическим процессом возникают в печени, селезенке, почках, надпочечниках, нервной системе. При поражении внутренних органов заболевание протекает тяжело, с выраженной интоксикацией, фебрильной температурой тела. В таких случаях развивается перитонит, перикардит, плеврит, сердечная и почечная недостаточность с возможным летальным исходом. Выделяют узловую, бляшечную и инфильтративную формы, острое, подострое и хроническое течение болезни, а также четыре степени активности (0, І, ІІ, ІІІ). Наиболее благоприятно хроническое течение болезни, характеризующееся длительными ремиссиями (>1 года). Рецидивы могут возникать через период от нескольких недель до нескольких лет. При тяжелом течении с системным поражением жировой клетчатки (перитонит, перикардит, плеврит, сердечная и почечная недостаточность) летальность достигает 10%.
Учитывая большую роль в гранулематозном воспалении цитокинов, осуществляющих взаимную активацию макрофагов и лимфоцитов, а также ингибирование образования гранулем антителами к фактору некроза опухоли-α в эксперименте [9], перспективным является распространение антицитокиновой терапии на большинство из вышепредставленных гранулематозных болезней, относящихся к компетенции ревматологов.
Список использованной литературы
- 1. Бунчук Н.В. (1997) Ревматическая полимиалгия. В кн.: Клиническая ревматология. Под ред. А.А. Насонова, Н.В. Бунчук. Москва, Медицина, с. 212–216.
- 2. Вест С. (1999) Дж. Секреты ревматологии. Пер с англ. Издательство БИНОМ — Невский диалект, Москва — Санкт-Петербург, 768 с.
- 3. Коваленко В.Н., Шуба Н.М. (ред.) (2004) Номенклатура, класифікація, критерії діагностики та програми лікування ревматичних хвороб. Київ, 256 с.
- 4. Насонова В.А., Насонов Е.Л. (ред.) (2003) Системные васкулиты. В кн.: Рациональная фармакотерапия ревматических заболеваний: Руковод. для практикующих врачей. Литтерра, Москва, 507 с.
- 5. Насонова В.А. (ред.) (2006) Лечение ревматических заболеваний ударными дозами метилпреднизолона. Пульс-терапия: Пособие для врачей. Киев, 27 с.
- 6. Насонова В.А., Бунчук Н.В. (ред.) (1997) Ревматические болезни: Руковод. для врачей. Медицина, Москва, 520 с.
- 7. Насонов Е.Л. (ред.) (2006) Клинические рекомендации. Ревматология. ГЭОТАР-Медиа, Москва, 288 с.
- 8. Насонов Е.Л. (2005) Системные васкулиты. В кн.: Рациональная фармакотерапия сердечно-сосудистых заболеваний: Руковод. для практикующих врачей. Е.И. Чазов, Ю.Н. Беленков, Е.О. Борисова, Е.Е. Гогин и др. Под общ. ред. Е.И. Чазова, Ю.Н. Беленкова. Литтерра, Москва, 972с.
- 9. Струков А.И., Кауфман О.Я. (1989) Гранулематозное воспаление и гранулематозные болезни. Медицина, Москва, 183 с.
- 10. Фаучи Э. (2005) Васкулиты. В кн.: Внутренние болезни по Тинсли Р. Харрисону. Под ред. Э. Фаучи, Ю. Браунвальда, К. Иссельбаха и др. В 7 т. Т. 5. Пер. с англ. Практика — Мак-Гроу, Москва (совместное издание), 491 с.
- 11. Шилкина Н.П., Насонов Е.Л., Баранов А.А. (1997) Гигантоклеточный артериит. В кн.: Ревматические болезни: Руковод. для врачей. Под ред. В.А. Насоновой, Н.В. Бунчука. Медицина, Москва, с. 248.
- 12. Шилкина Н.П., Насонов Е.Л., Баранов А.А. (1997) Неспецифический аортоартериит (болезнь Такаясу). В кн.: Ревматические болезни: Руковод. для врачей. Под ред. В.А. Насоновой, Н.В. Бунчука. Медицина, Москва, с. 253.
- 13. Шилкина Н.П., Насонов Е.Л., Баранов А.А. (1997) Синдром Чарга — Стросса (аллергический ангиит и гранулематоз). В кн.: Ревматические болезни: Руковод. для врачей. Под ред. В.А. Насоновой, Н.В. Бунчука. Медицина, Москва, с. 241.
- 14. Шилкина Н.П., Насонов Е.Л., Баранов А.А. (1997) Гранулематоз Вегенера. В кн.: Ревматические болезни: Руковод. для врачей. Под ред. В.А. Насоновой, Н.В. Бунчука. Медицина, Москва, с. 253.
- 15. Dennis G.J. (1999) Васкулиты крупных сосудов: гигантоклеточный артериит и болезнь Такаясу. В кн.: Cекреты ревматологии. Пер. с англ. С.Дж. Вест. Издательство БИНОМ — Невский Диалект, Москва —Санкт-Петербург, с. 251.
- 16. Jennette J.C., Falk R.J., Andrassy K. et al. (1994) Nomenclature of systemic vasculitides: proposal of an international consensus conference. Arthr. Rheum., 37: 187–192.
- 17. Malyak M. (1999) Гранулематоз Вегенера и прочие заболевания, при которых выявляются антинейтрофильные цитоплазматические антитела. В кн.: Cекреты ревматологии. Пер. с англ. С.Дж. Вест. Издательство БИНОМ — Невский Диалект, Москва — Санкт-Петербург, с. 238.
Адрес для переписки:
Казимирко Виталий Казимирович
04112, Киев, ул. Дорогожицкая, 9
Национальная медицинская академия
последипломного образования им. П.Л. Шупика

Leave a comment