АРТЕРІАЛЬНА ГІПЕРТЕНЗІЯ ПРИ СИСТЕМНОМУ ВАСКУЛІТІ
Бевзенко Т.Б.1, Головач И.Ю.2, Ермолаева М.В.3, Седая Л.В.3, Синяченко О.В.3
- 1Научно-практический центр профилактической и клинической медицины ГУД, Киев
- 2Клінічна лікарня «Феофанія» ДУС, Київ
- 3Донецкий национальный медицинский университет им. Максима Горького, Красный Лиман
Резюме. Мета дослідження — оцінка частоти розвитку артеріальної гіпертензії (АГ) при васкуліті Шенляйна — Геноха (ВШГ), ідіопатичному кріоглобулінемічному васкуліті (КГВ), гранулематозі з поліангіїтом Вегенера (ГПА), мікроскопічному поліангіїті (МПА), вузликовому поліартеріїті (ВПА), еозинофільному гранулематозному поліангіїті Черджа — Стросс (ЕПА) та аортоартеріїті Такаясу (ААТ), вивчення чинників ризику підвищення артеріального тиску (АТ) при системному васкуліті (СВ), зв’язок з іншими проявами захворювань. Під спостереженням перебували 503 хворих на СВ, а співвідношення кількості пацієнтів з ВШГ, МПА, КГВ, ВПА, ЕПА, ААТ і ГПА становило 7:3:3:1:1:1:1. Виявлено підвищення АТ у 72% хворих на ВПА, у 69% — на ААТ, у 65% — на КГВ, у 61% — на МПА, у 54% — на ГПА, у 25% — на ВШГ, у 20% — на ЕПА, що високовірогідно прямо корелює з параметрами периферичного судинного опору, пов’язане з віком пацієнтів, тривалістю захворювання, ступенем активності патологічного процесу, причому розвиток АГ впливає на інтегральну тяжкість клінічних ознак СВ, що демонструють багатофакторний дисперсійний аналіз й аналіз множинної регресії. Виявлено, що АГ частково носить симптоматичний ренальний характер, впливає на ураження серця (при ВШГ, КГВ, МПА), суглобів (ВШГ, ЕПА) і нирок (ВШГ), визначаючи швидкість клубочкової фільтрації та темпи прогресування нефропатії, а зростання АТ взаємопов’язано із загальною вираженістю судинної патології та характером вазодилатації.
Введение
Системный васкулит (СВ) относится к гетерогенной группе заболеваний, основным морфологическим признаком которых считается иммунное воспаление сосудистой стенки, что определяется типом, калибром и локализацией пораженных сосудов (Ruperto N., 2012). Распространенность СВ в мире неуклонно ежегодно повышается, составляя 2–3 случая на 10 тыс. населения (Mohammad A.J. et al., 2009). В настоящее время изучение СВ относится к наиболее динамично развивающимся областям ревматологии, при этом подчеркивается как клинико-патогенетическая общность этих заболеваний, так и определенные отличия отдельных нозологических форм (Gibelin A. et al., 2011).
Одним из характерных проявлений СВ является повышение артериального давления (АД), в частности у больных аортоартериитом Такаясу (ААТ) (De Jesus G.R. et al., 2012; De Souza A.W., de Carvalho J.F., 2014; Sandeep S. et al., 2014), узелковым полиартериитом (УПА) (Kawajiri H. et al., 2013), гранулематозом с полиангиитом Вегенера (ГПА) (Florian A. et al., 2011; Miszalski-Jamka T. et al., 2011; Soriano A. et al., 2012), микроскопическим полиангиитом (МПА) (Villiger P.M., Guillevin L., 2010), эозинофильным полиангиитом Черджа — Стросс (ЭПА) (Taormina G. et al., 2014), васкулитом Шенляйна — Геноха (ВШГ) (Naija O. et al., 2013). При этом течение и патогенез артериальной гипертензии (АГ) у больных СВ изучены недостаточно (Gross W.L. et al., 2008; Csernok E. et al., 2009). Обсуждаются активация ренин-ангиотензин-альдостероновой системы вследствие появления почечной микроангиопатии и нарушения системы простагландины — кинины (Cacoub P., Guillevin L., 2006; Amoroso A. et al., 2008; Gao P. et al., 2014), а АГ при ААТ рассматривают в контексте реноваскулярных (вазоренальных) механизмов (Borchers A.T., Gershwin M.E., 2012).
Цель выполненной работы — оценка частоты развития АГ при ВШГ, ГПА, МПА, УПА, ЭПА, ААТ и идиопатическом криоглобулинемическом васкулите (КГВ), изучение факторов риска повышения АД при СВ, связь с другими проявлениями заболеваний.
Объект и методы исследования
Под наблюдением находились 503 больных СВ, характеристика которых представлена в таблице. Соотношение количества больных с ВШГ, МПА, КГВ, УПА, ЭПА, ААТ и ГПА составило 7:3:3:1:1:1:1. Согласно Чэпел — Хиллской классификации (США, 2012), ААТ относится к СВ крупных сосудов, УПА — средних, все остальные — мелких, причем МПА, ГПА и ЭПА являются СВ, ассоциированными с антинейтрофильными цитоплазматическими антителами (ANCA), а ВШГ и КГВ — иммунокомплексными. При ААТ превалировали женщины, при УПА — мужчины, соответственно в соотношении 3:1 и 2:1, более молодого возраста были пациенты с ВШГ, а старшего — с КГВ. Отметим, что клиническая характеристика больных представлена на момент их обследования (например, на предыдущих этапах у всех обследованных с МПА, ВШГ и КГВ отмечали изменения кожи, у 93% с ВШГ — суставной синдром). В случаях УПА, МПА и КГВ превалировали поражения периферической нервной системы (моно- и полинейропатия, радикулопатия, мортоновская метатарзалгия), а у больных ААТ и ГПА — центральной нервной системы (дисциркуляторная энцефалопатия, нарушения мозгового кровообращения, кортиконуклеарный и псевдобульбарный синдромы). У 55% пациентов с ААТ диагностирован аортальный порок сердца, 17% — перенесли инфаркт миокарда, 21% — мозговой инсульт, 36% с УПА были носителями антигена вирусного гепатита В, а 29% с КГВ — гепатита С. Криоглобулины на момент обследования выявлены у 97% больных КГВ, гипериммуноглобулинемия-A — у 72% с ВШГ, ANCA — 75% с ГПА, 71% — с МПА и 57% — с ЭПА (соответственно в соотношениях антитела к миелопероксидазе (АМП) и антитела к протеиназе-3 — (АП3) как 1:6, 2:1 и 8:1). Уровень эозинофилов в крови больных ЭПА составил 15,1±2,12% лейкоцитов, или 2,1±0,82 ⋅ 10/л.
| Показатель | Группа больных СВ (n=503) | |||||||
|---|---|---|---|---|---|---|---|---|
| ААТ | УПА | МПА | ГПА | ЭПА | ВШГ | КГВ | ||
| Количество больных в группах, n | 29 | 39 | 89 | 28 | 30 | 193 | 95 | |
| Мужчины/женщины, % | 24/76 | 62/38 | 42/58 | 57/43 | 43/57 | 51/49 | 40/60 | |
| Возраст, лет (M±m) | 44,2±2,48 | 44,2±1,88 | 44,8±1,23 | 46,0±2,41 | 40,4±2,59 | 26,2±0,72 | 52,3±1,28 | |
| Длительность болезни, лет (M±m) | 10,4±1,98 | 8,5±1,30 | 6,4±0,70 | 4,3±0,83 | 10,7±2,05 | 9,0±0,60 | 4,6±0,62 | |
| II–III степень активности, % | 86 | 79 | 85 | 93 | 87 | 72 | 93 | |
| Острое и подострое течение, % | – | 15 | 28 | 56 | – | 19 | 43 | |
| Скорость клубочковой фильтрации (СКФ), мл/мин | 107,1±4,78 | 104,4±4,18 | 101,2±2,51 | 108,2±3,99 | 110,5±4,34 | 110,3±1,92 | 103,3±2,68 | |
| Признаки поражения, % |
кожи суставов мышц сердца легких печени селезенки ПНС, ЦНС почек |
17 41 48 76 10 28 4 21 62 |
31 67 54 80 46 56 13 90 62 |
82 64 38 51 50 56 8 48 67 |
21 32 36 50 68 46 7 46 64 |
53 63 37 47 100 33 20 37 57 |
64 47 15 31 5 22 7 18 67 |
85 67 26 61 57 62 25 40 68 |
ПНС — периферическая нервная система; ЦНС — центральная нервная система.
Рентгенологическое исследование периферических суставов, крестцовоподвздошных сочленений, позвоночника и легких выполнено на аппарате «Multix-Compact-Siеmens» (Германия), ультразвуковое исследование суставов и внутренних органов — на аппарате «Envisor-Philips» (Нидерланды), электрокардиографическое — на «МІДАК-ЕК1Т» (Украина) и «Bioset-8000» (Германия), трансторакальную и чреспищеводную эхокардиографию — на «Еnvisor-C-Philips» (Нидерланды) и «HD-11-XE-Philips» (Нидерланды), ангиографию — на «Angiostar-Plus-Siemens» (Германия). Для оценки лабораторных показателей использовали анализаторы «BS-200» (Китай) и «Olympus-AU640» (Япония), ридер «PR2100-Sanofi diagnostic pasteur» (Франция), иммуноблот «Euroline-Euroimmun» (Германия).
Подсчитывали число болезненных суставов (NPJ), индексы Лансбури (iL), активности артрита (iDAS, iDAS28) и интегральной тяжести поражений суставов (iWA). Индекс прогрессирования артрита (iPA) высчитывали по формуле:
| iPA = | (RS)+S | , |
| D |
где RS — рентгенологическая стадия, S — сумма рентгеносонографических признаков, D — длительность клинической манифестации суставного синдрома. Определяли также индекс прогрессирования нефропатии (iPN) по формуле:
| iPN = | 1+S | , |
| Q |
где S — стадия хронической болезни почек, Q — длительность заболевания.
Индексы тяжести поражений сердца (iWH) и сосудов (iWV) высчитывали по формуле:
| iWH (iWV) = | SN | , |
| n |
iWH (iWV) = SN ,
где SN — число измененных признаков, n — общее число изученных признаков. При оценке функционального состояния почек пользовались определением СКФ по формуле Кокрофта — Голта.
Статистическая обработка полученных результатов исследований проведена с помощью компьютерного вариационного непараметрического корреляционного регрессионного одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы «Microsoft Excel» и «Statistica-Stat-Soft», США). Оценивали средние значения (M), их стандартные ошибки (m), стандартные отклонения (SD), коэффициенты корреляции, критерии дисперсии, множественной регрессии, Стьюдента, Уилкоксона — Рао, Макнемара — Фишера и достоверность статистических показателей.
Результаты исследования
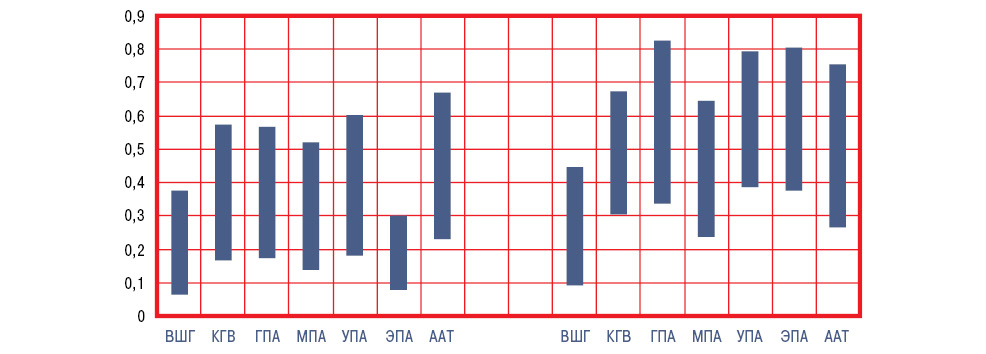
Повышение систолического артериального давления (САД) >115 мм рт. ст. установлено у 25,4% больных с ВШГ, у 65,3% — с КГВ, у 53,6% — с ГПА, у 60,7% — с МПА, у 71,8% — с УПА, у 20,0% — с ЭПА и у 69,0% — с ААТ. Усредненные показатели САД соответственно составили 105,7±1,01; 121,9±1,29; 114,1±2,27; 118,7±14,30; 124,5±19,05;106,3±2,34 и 122,9±3,64 мм рт. ст., а периферического сосудистого сопротивления (ПСС) — 2015,0±34,97; 2430,1±62,67; 2657,1±120,23; 2671,6±68,62; 2712,8±96,51; 2053,3±98,35 и 2386,2±149,77 дин ⋅ с ⋅ см. Сравнительная оценка параметров САД и ПСС у здоровых людей и больных с разными вариантами СВ представлена на рис. 1 и 2. При СВ существуют высокодостоверные прямые корреляционные связи показателей САД и ПСС при ВШГ, ГПА, МПА, УПА и ЭПА, что отражает патогенетическую значимость ПСС при развитии АГ у больных СВ.
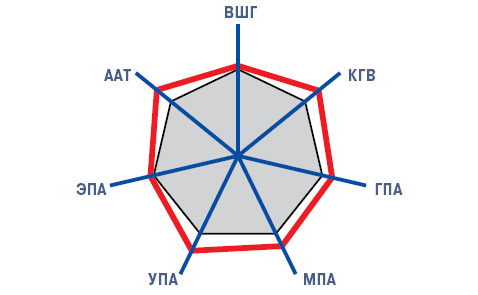
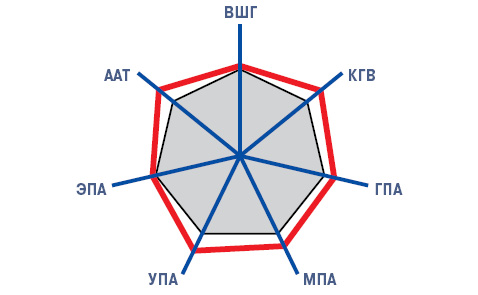
Обсуждение
Согласно данным однофакторного дисперсионного анализа, на уровень САД при ВШГ и КГВ оказывает влияние возраст пациентов, а при ВШГ, МПА и ЭПА — длительность заболевания. Как свидетельствуют результаты корреляционного анализа, с возрастом больных повышаются показатели САД при ВШГ, КГВ, ЭПА и ААТ, согласно продолжительности заболевания — только при ВШГ, а степени активности патологического процесса — при ВШГ и ААТ. Многофакторный дисперсионный анализ Уилкоксона — Рао показывает, что АГ влияет на интегральные клинические показатели у больных ВШГ, КГВ, МПА и ЭПА. Анализ множественной регрессии демонстрирует достоверную прямую зависимость от САД интегральных клинических показателей при ВШГ, ГПА, МПА, УПА, ЭПА и ААТ. Как видно из рис. 3 и 4, соотношение частоты зависимости признаков СВ от САД при ВШГ, ЭПА, МПА, КГВ, УПА, ААТ и ГПА составляет 19:9:6:6:3:1:1.
Результаты регрессионного анализа свидетельствуют о том, что от уровня САД прямо зависит тяжесть поражения сердца и почек при ВШГ, только сердца — при КГВ и МПА; обратная зависимость установлена с патологией суставов у больных ВШГ и ЭПА. АГ в 7,6 раза чаще развивается при наличии нефропатии у больных ВШГ по сравнению с пациентами без почечной патологии, в 1,9 раза — при МПА, в 1,7 раза — при УПА, в 1,5 раза — при КГВ. Это отчасти указывает на симптоматический (ренальный) генез АГ при некоторых вариантах СВ. Параметры САД прямо коррелируют с интегральной тяжестью течения ВШГ, КГВ и МПА. Кроме того, выраженность клинических проявлений влияет на показатели САД при этих СВ, а в случаях МПА, наоборот, САД оказывает достоверное воздействие на суммарную тяжесть признаков болезни, что показывает ANOVA.
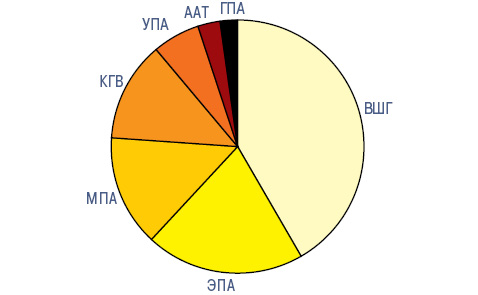
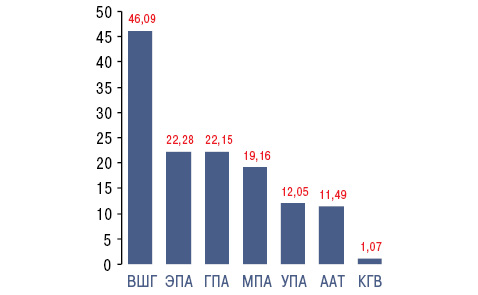
Нефротический синдром оказывает влияние на характер АД при ВШГ и КГВ, а снижение функции почек — при ВШГ, КГВ, ГПА, ЭПА и ААТ. От СКФ и iPN зависят параметры САД у больных ВШГ и МПА, а только от СКФ — при КГВ, ЭПА и ААТ. C показателем iPN корреляционные связи САД отсутствуют, тогда как при ВШГ, КГВ, ГПА и МПА существуют достоверные обратные соотношения с СКФ. Кроме того, в случаях ААТ с показателем САД прямо коррелирует степень почечной недостаточности. С учетом выполненной статистической обработки полученных данных можно сделать заключение, что показатели САД >120 мм рт. ст. при ВШГ и САД >130 мм рт. ст. — при МПА являются прогнознегативными в отношении снижения функции почек и темпов ее прогрессирования.
Параметры САД >120 мм рт. ст. у больных ВШГ относятся также к прогнознегативным в контексте суставного синдрома. Такое заключение базируется на установленных прямых корреляционных связях значений САД с показателями NPJ, iDAS, iDAS28 и iWA. Напрашивается вывод, что тяжелый суставной синдром (iWA >20 о.е. или >M+SD больных) относится к факторам риска развития АГ при ВШГ.
Как видно из рис. 5, iWH при ААТ>УПА>КГВ> ГПА>МПА>ВШГ>ЭПА, а iWV — при УПА>ЭПА> ГПА>ААТ>КГВ>МПА>ВШГ. Уровень вазодилатации в процессе допплерографии плечевой артерии у больных УПА>ААТ>ВШГ>МПА>КГВ>ГПА>ЭПА соответственно составлял 16,7±1,19; 14,5±0,90; 13,7±0,42; 13,2±0,52; 12,8±0,83; 10,6±1,00 и 8,1±0,59%. От уровней САД прямо зависит тяжесть сосудистой патологии при всех СВ.
Как демонстрирует однофакторный дисперсионный анализ, iWH и iWV высокодостоверно влияют на показатели САД при ВШГ, КГВ и МПА, а iWV, кроме того — при ГПА. Необходимо отметить, что повышение САД у больных КГВ сопровождается достоверным увеличением на 56% значений iWH и на 35% iWV.
Выводы
Повышение АД отмечается у 72% больных УПА, у 69% — ААТ, у 65% — КГВ, у 61% — МПА, у 54% — ГПА, у 25% — ВШГ, у 20% — ЭПА, что высокодостоверно прямо коррелирует с параметрами ПСС, связано с возрастом пациентов (ВШГ, КГВ), длительностью заболевания (ВШГ), степенью активности патологического процесса (ВШГ, ААТ), причем развитие АГ влияет на интегральную тяжесть клинических признаков СВ, что демонстрируют многофакторный дисперсионный анализ и анализ множественной регрессии, воздействует на поражение сердца (ВШГ, КГВ, МПА), суставов (ВШГ, ЭПА) и почек (ВШГ), определяя СКФ и темпы прогрессирования нефропатии, а возрастание АД взаимосвязано с общей выраженностью сосудистой патологии и характером вазодилатации. С учетом полученных данных можно говорить о симптоматическом (ренальном) характере АГ у большинства больных, что требует новых подходов к изучению патогенеза повышения АД и к разработке медицинской технологии лечения отдельных нозологических форм СВ.
Список использованной литературы
- Amoroso A., Danek G., Vatta S. et al. (2008) Polymorphisms in angiotensin-converting enzyme gene and severity of renal disease in Henoch-Schoenlein patients. Nephrol. Dial. Transplant., 13 (12): 3184–3188.
- Borchers A.T., Gershwin M.E. (2012) Giant cell arteritis: a review of classification, pathophysiology, geoepidemiology and treatment. Autoimmun. Rev., 11(6–7): 544–554.
- Cacoub P., Guillevin L. (2006) Microangiopathy and arterial hypertension in scleroderma and periarteritis nodosa. J. Mal. Vasc., 11(3): 282–287.
- Csernok E., Muller A., Gross W.L. (2009) Immunopathology of ANCA-associated vasculitis. Intern. Med., 38(10): 759–765.
- De Jesus G.R., d’Oliveira I.C., dos Santos F.C. et al. (2012) Pregnancy may aggravate arterial hypertension in women with Takayasu arteritis. Isr. Med. Assoc. J., 14(12): 724–728.
- De Souza A.W., de Carvalho J.F. (2014) Diagnostic and classification criteria of Takayasu arteritis. J. Autoimmun., 48–49: 79–83.
- Florian A., Slavich M., Blockmans D. et al. (2011) Cardiac involvement in granulomatosis with polyangiitis (Wegener granulomatosis). Circulation, 124(13): 342–344.
- Gao P., Xu T.T., Lu J. et al. (2014) Overexpression of SIRT1 in vascular smooth muscle cells attenuates angiotensin II-induced vascular remodeling and hypertension in mice. J. Mol. Med., 92(4): 347–357.
- Gibelin A., Maldini C., Mahr A. (2011) Epidemiology and etiology of wegener granulomatosis, microscopic polyangiitis, churg-strauss syndrome and goodpasture syndrome: vasculitides with frequent lung involvement. Semin. Respir. Crit. Care Med., 32(3): 264–273.
- Gross W.L., Trabandt A., Csernok E. (2008) Pathogenesis of Wegener’s granulomatosis. Ann. Med. Interne, 149(5): 280–286.
- Kawajiri H., Koh E., Masuda N. et al. (2013) Coronary artery bypass grafting in a patient with polyarteritis nodosa presenting with acute myocardial infarction and multiple coronary aneurysms. Ann. Thorac. Cardiovasc. Surg., 30(8): 135–139.
- Miszalski-Jamka T., Szczeklik W., Sokołowska B. et al. (2011) Cardiac involvement in Wegener’s granulomatosis resistant to induction therapy. Eur. Radiol., 21(11): 2297–2304.
- Mohammad A.J., Jacobsson L.T., Westman K.W. et al. (2009) Incidence and survival rates in Wegener’s granulomatosis, microscopic polyangiitis, Churg-Strauss syndrome and polyarteritis nodosa. Rheumatology, 48(12): 1560–1565.
- Naija O., Bouzaraa J., Goucha-Louzir R. et al. (2013) Henoch Schonlein nephrites in children: Clinical features and outcome: About 34 cases. Tunis Med., 91(12): 700–704.
- Ruperto N. (2012) Paediatric rheumatology international trials organisation (PRINTO). Classification criteria and diagnostic tests for vasculitides. J. Rheumatol., 39(8): 1503–1505.
- Sandeep S., Unni V.N., Sreekumar K.P. et al. (2014) Takayasu arteritis in an infant. Indian J. Nephrol., 24(4): 257–259.
- Soriano A., Lo Vullo M., Casale M. et al. (2012) Meningeal involvement in Wegener granulomatosis: case report and review of the literature. Int. J. Immunopathol. Pharmacol., 25(4): 1137–1141.
- Taormina G., Andolina G., Banco M.A. et al. (2014) An uncommon presentation of eosinophilic granulomatosis with polyangiitis: a case report. J. Med. Case Rep., 13(8): 190–198.
- Villiger P.M., Guillevin L. (2010) Microscopic polyangiitis: clinical presentation. Autoimmun. Rev., 9(12): 812–819.
Адрес для переписки:
Бевзенко Татьяна Борисовна
E-mail: tanya.bevzenko@gmail.com

Leave a comment