ФАКТОРЫ РИСКА И СУБКЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ АТЕРОСКЛЕРОЗА У БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ
Курята A.B.1, Нода О.Ю.2, Лысунец Т.К.3
- 1Днепропетровская государственная медицинская академия Днепропетровская областная клиническая больница им. И.И. Мечникова
- 2ДЗ «Дніпропетровська медична академія МОЗ України»
- 3КЗ «Обласна клінічна лікарня ім. І.І. Мечникова», Дніпропетровськ
Резюме. Цель исследования — оценка взаимосвязи между глобальными и дополнительными факторами риска и субклиническими проявлениями атеросклероза у больных системной красной волчанкой (СКВ).Методыисследования: общеклиническое обследование, определение уровня общего холестерина (ОХС) и триглицеридов (ТГ) в сыворотке крови, определение эндотелийзависимой вазодилатации (ЭЗВД) по результатам пробы с реактивной гиперемией, толщины комплекса интима-медиа, оценка риска фатальных сердечно-сосудистых событий по шкале SCORE, статистические методы. Обследовано 30 пациентов с достоверным диагнозом СКВ I и II степени активности, длительностью применения глюкортикостероидов не менее 1 года. Среди них было 25 женщин и 5 мужчин в возрасте от 30 до 59 лет, средняя продолжительность заболевания — 85,9±8,38 мес. Контрольную группу составили 293 лица сельского трудоспособного населения, сопоставимых по полу и возрасту с основной группой.Результаты: установлено, что у пациентов с СКВ среди традиционных факторов риска приоритетными являются ожирение (56,7% случаев), артериальная гипертензия (67% случаев) и дислипидемия (50% случаев). По сравнению с контрольной группой среди больных СКВ чаще отмечалось абдоминальное ожирение (у 70% больных, в контрольной группе — у 64,8%), повышенные показатели ОХС и ТГ (50 и 10% соответственно, в контрольной группе — 46 и 9% соответственно). При определении субклинических проявлений атеросклероза установлено, что в 33,3% случаев была возбуждена реактивная гиперемия, у 53,3% больных был увеличен комплекс интима-медиа. В то же время по данным исследования кардиоваскулярный риск у пациентов с СКВ, оцениваемый по классическим факторам риска, составил в среднем 1,0±0,89%, что считается низким уровнем риска, в контрольной группе этот показатель — 2,67±0,36%.Выводы: кардиоваскулярный риск у пациентов с СКВ, который оценивается по классическим факторам риска, не превышает среднепопуляционный уровень. В то же время у этих пациентов выявлены признаки субклинического атеросклероза и прямая корреляционная связь между уровнем сердечно-сосудистого риска и толщиной комплекса интима-медиа, реактивной гиперемией. Поэтому возможно, что именно дополнительные факторы отвечают за высокий риск развития сердечно-сосудистых осложнений при СКВ, что требует дальнейшего более глубокого исследования.
Методи дослідження: загальноклінічне обстеження, визначення рівня загального холестерину (ЗХС) і тригліцеридів (ТГ) у сироватці крові, визначення ендотелійзалежної вазодилатації (ЕЗВД) за результатами проби з реактивною гіперемією, товщини комплексу інтима-медіа, оцінка ризику фатальних серцево-судинних подій за шкалою SCORE, статистичні методи. Обстежено 30 пацієнтів із достовірним діагнозом СЧВ І та ІІ ступеня активності, тривалістю застосування глюкокортикостероїдів не менше 1 року. Серед них було 25 жінок та 5 чоловіків віком від 30 до 59 років, середня тривалість захворювання — 85,9±8,38 міс. Контрольну групу становили 293 особи сільського працездатного населення, зіставних за статтю та віком з основною групою.
Результати: встановлено, що у пацієнтів із СЧВ серед традиційних факторів ризику пріоритетними є ожиріння (56,7% випадків), артеріальна гіпертензія (67% випадків) та дисліпідемія (50% випадків). Порівняно з контрольною групою серед хворих на СЧВ частіше відзначалось абдомінальне ожиріння (у 70% хворих, у контрольній групі — у 64,8%), підвищені показники ЗХС і ТГ (50 та 10% відповідно, у контрольній групі — 46 та 9% відповідно). При визначенні субклінічних проявів атеросклерозу встановлено, що у 33,3% випадків була порушена реактивна гіперемія, у 53,3% хворих був збільшений комплекс інтима-медіа. Водночас за отриманими даними кардіоваскулярний ризик у пацієнтів із СЧВ, який оцінюється за класичними факторами ризику, становив в середньому 1,0±0,89%, що вважається низким рівнем ризику, в контрольній групі цей показник — 2,67±0,36%.
Висновки: кардіоваскулярний ризик у пацієнтів із СЧВ, який оцінюється за класичними факторами ризику, не перевищує середьопопуляційний рівень. Водночас у цих пацієнтів встановлені ознаки субклінічного атеросклерозу та прямий кореляційний зв’язок між рівнем серцево-судинного ризику та показником товщини комплексу інтима-медіа, реактивною гіперемією. Тому можливо, що саме додаткові фактори відповідають за високий ризик розвитку серцево-судинних ускладнень при СЧВ, що потребує подальшого більш глибокого дослідження.
Вступ
Після запровадження у клінічну практику глюкокортикостероїдів (ГКС), препаратів цитотоксичної дії, протималярійних препаратів та використання їх в оптимальних дозах, застосування нових ефективних антигіпертензивних, сечогінних і антибактеріальних засобів, а також широкого застосування терапії, яка заміщує функцію нирок (гемодіаліз, перитонеальний діаліз, трансплантація нирок), істотно підвищилася виживаність хворих на системний червоний вовчак (СЧВ). Якщо у 50–60-х роках ХХ ст. 5-річна виживаність хворих на СЧВ становила нижче 50% [10], то в останні 20 років 5-,10- та 20-річна виживаність становила відповідно 93; 85 та 68% [8]. У зв’язку зі значним збільшенням тривалості життя хворих на СЧВ виникли нові проблеми, одна з яких — ранній (прискорений) розвиток атеросклерозу, при цьому тяжкість і поширеність ураження коронарних та мозкових судин стали однією з провідних причин морбідності та летальності [8, 23, 27, 28].
Спектр серцево-судинної патології представлений патологією як запального, так і атеросклеротичного генезу. Серед причин ураження судинної системи у хворих на СЧВ обговорюють механізми, асоційовані з аутоімунним запальним процесом, активізацією атеросклеротичного процесу тощо [26, 19, 7, 25]. Більшість дослідників розцінюють ранній розвиток атеросклерозу у хворих на СЧВ як наслідок підвищеної частоти традиційних факторів ризику та безпосереднього впливу запального процесу [20, 22]. Певну роль може мати взаємодія традиційних факторів атеросклерозу та факторів, безпосередньо пов’язаних із СЧВ [13]. Так, за даними S. Manzi та співавторів (1997), частота виникнення ішемічної хвороби серця у хворих на СЧВ значно перевищує (з урахуванням статі та віку) частоту розвитку цієї нозології порівняно із загальною популяцією [16]. S. Manzi та співавтори також стверджують, що більш похилий вік, більша тривалість захворювання, тривалість застосування більш високих доз ГКС та постменопаузальний стан виявилися значущими факторами ризику формування атеросклеротичних бляшок [16].
Відомо, що лікування ГКС є фактором ризику атеросклерозу. Однак залишається нез’ясованим, чи пов’язано це з прямою атерогенною дією ГКС, чи цей зв’язок з атеросклерозом зумовлений посиленням таких традиційних факторів, як гіперліпідемія, артеріальна гіпертензія та ожиріння [1]. Останні дослідження також вказують на той факт, що вовчаковий процес безпосередньо здатний змінювати ліпідний профіль, який стає проатерогенним: підвищення рівня тригліцеридемії, холестерину ліпопротеїнів дуже низької щільності (ЛПДНЩ), зниженими значеннями холестерину ліпопротеїнів високої щільності (ЛПВЩ) та аполіпопротеїну [7].
Вважається, що патогенез атеросклеротичного ураження судин при СЧВ є багатофакторним і пов’язаний із взаємодією між традиційними факторами ризику, факторами, індукованими запаленням і пошкодженням, тромбозом судин, антифосфоліпідними антитілами, що важливо враховувати як при виборі підходу до первинної та вторинної профілактики, так і при проведенні адекватної терапії у хворих із клінічними проявами атеросклерозу [1, 17].
Слід зазначити, що в останніх рекомендаціях Європейської антиревматичної ліги (EULAR) вже розроблено вказівки щодо профілактики атеросклерозу при ревматоїдному артриті: оцінка сумарного серцево-судинного ризику (сумарний бал за шкалою SCORE множать на коефіцієнт 1,5), агресивний контроль запалення, раціональне застосування потенційно небезпечних препаратів (ГКС, нестероїдних протизапальних препаратів) [18]. У цих рекомендаціях ревматоїдний артрит розглядають як стан, асоційований із високим ризиком серцево-судинних захворювань та розцінюють еквівалентно ризику фатальних серцево-судинних подій при цукровому діабеті. Щодо СЧВ такі рекомендації ще не розроблені, незважаючи на численні повідомлення щодо високої розповсюдженості атеросклеротичного ураження серед цих хворих.
Мета дослідження — оцінка взаємозв’язку між глобальними та додатковими факторами ризику та субклінічними проявами атеросклерозу у хворих на СЧВ.
Об’єкти і методи дослідження
Обстежено 30 пацієнтів із СЧВ. Вік хворих становив від 30 до 59 років (середній — 45,15±3,05 року). Серед обстежених було 25 (83%) жінок та 5 (17%) чоловіків. Перший ступінь активності був встановлений у 11 (37%) хворих, другий — у 19 (63%) хворих. Тривалість захворювання становила від 12 до 324 міс (в середньому — 85,9±8,38 міс). Тривалість лікування ГКС від 1 року до 25 років (в середньому — 9,62±1,87 року). Добова доза ГКС на момент дослідження коливалася від 5 до 25 мг/добу за преднізолоном (в середньому — 9,88±1,25 мг/добу).
Діагноз СЧВ встановлювали згідно з класифікацією Асоціації ревматологів України (2002) та діагностичними критеріями Американської ревматологічної асоціації (1997) і формулювали відповідно до наказу від 12.10.2006 р. № 676 «Про затвердження протоколів надання медичної допомоги за спеціальністю «Ревматологія» [3, 4].
Критерії включення у дослідження: перший та другий ступені активності СЧВ, тривалість застосування ГКС не менше 1 року. Критерії виключення: третій ступінь активності СЧВ, хронічна ниркова недостатність ІІ–IV ступеня, цукровий діабет, ішемічна хвороба серця, гостра серцева недостатність, гіпотиреоз.
У контрольну групу увійшли 293 особи сільського працездатного населення, які можна зіставити за статтю та віком з основною групою: вік становив від 25 до 59 років (середній — 42,15±2,95 року), серед обстежених було 223 (76%) жінки та 70 (24%) чоловіків.
При клінічному та інструментальному обстеженні основної групи виявлено міокардит, міокардитичний кардіосклероз (100%), ураження суглобів: артралгія, поліартрит, вторинний остеоартроз — у 60%, ураження судин: синдром Рейно, васкуліт, тромбофлебіт — у 17%, livedo reticularis — у 13%, ураження шкіри: дерматит за типом «метелика» у 47%, дискоїдний вовчак — у 40%, ураження слизової оболонки: афтозний стоматит — у 23%, хейліт — у 7%, ураження нервової системи — у 17%, ураження легень: пульмоніт, пневмосклероз — у 7%, ураження серозних оболонок: плеврит, перикардит — у 37% (табл. 1). За віком хворі були розподілені на дві групи: перша — 30–44 роки (n=15) і друга — 45–59 років (n=15).
| Показник | Основна група (n=30), n (%) | Контрольна група (n=293), n (%) |
|---|---|---|
| Стать, чол./жін. | 5 (17)/25 (83) | 70 (24)/223 (76) |
| Вік, років | 45,15±3,05 | 42,15±2,95 |
| Маса тіла, кг | 75,34±3,12 | 83,47±3,70 |
| ІМТ, кг/м | 31,63±2,23 | 29,89±2,67 |
| ІМТ >25 кг/м | 17 (56,7) | 226 (77) |
| Окружність талії, см | 104,03±2,56 | 95,93±2,24 |
| Підвищений показник окружності талії | 21 (70) | 190 (64,8) |
| Артеріальна гапертензія | 20 (67) | 215 (73) |
| САТ, мм рт. ст. | 154,00±20,18 | 147,00±17,21 |
| ДАТ, мм рт. ст. | 90,00±18,36 | 82±17,45 |
| Спадковий анамнез | 27 (90) | 91 (31) |
| Тютюнопаління | 11 (35) | 48 (16) |
| Ліпідний профіль | ||
| ЗХС, ммоль/л | 5,90±0,36 | 5,02±0,25 |
| ЗХС >5,2 ммоль/л | 15 | 135 |
| ТГ, ммоль/л | 1,44±0,11 | 1,12±0,08 |
| ТГ >1,7 ммоль/л | 3 | 28 |
| Ризик фатальних ССЗ за шкалою SCORE | (1,0 ±0,89) | (2,67±0,36) |
| Комплекс інтима-медіа, мм | 0,92±0,64 | 0,83±0,06 |
| Комплекс інтима-медіа >0,9 мм | 16 (53,3) | – |
| ЕЗВД, % | 11,07±1,03 | 15,04±0,03 |
| ЕЗВД <10% | 10 (33,3) | – |
Усім пацієнтам визначали зріст і масу тіла, індекс маси тіла (ІМТ), досліджували рівні ЗХС і ТГ у сироватці крові. Вміст ЗХС та ТГ у сироватці крові визначали імуноферментативними методами за допомогою колориметричного тесту наборів фірми «HUMAN» (Німеччина) на біохімічному аналізаторі «Chemistry Analyzer RT-1904C».
Усім хворим також визначали за допомогою еходопплера у 2D, CFM-режимі імпульсним датчиком 12L (5–12 МГц) функціональний стан ендотелію судин шляхом вимірювання ендотелійзалежної вазодилатації (ЕЗВД) за результатами проби з реактивною гіперемією за методикою, яку описав D. Celermajer [12]. Нормою вважався приріст діаметра артерії на ≥10%.
Дуплексне дослідження екстракраніального відділу сонних артерій виконували за рекомендаціями Американського товариства ехокардіографії (2005) [6]. Сканування проводили на апараті HDI 5000 Sono CT. («Philips», Голландія) за наявності імпульсного кольорового допплера і тканинного допплера, використовували лінійні датчики 5, 7,5 мГц і конвексний датчик — 3,5 мГц. Досліджували в режимах В-сканування, імпульсно-хвильової допплерографії і кольорового картування потоку крові.
Визначали звивистість судин, лінійну швидкість кровотоку, з аналізом структури стінок судин, товщини комплексу інтима-медіа, наявності атеросклеротичних бляшок і ступеня стенозу. Нормальною вважали товщину комплексу інтима-медіа не більше 0,9 мм. Сумарний ризик фатальних ускладнень атеросклерозу оцінювали за шкалою SCORE. Ризик фатальних ускладнень вважався низьким, якщо він становив <5%, високим при значенні в межах від 5 до 10%, та дуже високим, якщо він становив >10%.
Досліджувані величини представлені у такому вигляді: вибіркове середнє значення ± стандартна похибка вибіркового середнього значення. Оцінку різниці сукупностей вибірки проводили, використовуючи
t-критерій Стьюдента. Оцінка ступеня взаємозв’язку між парами незалежних ознак, виражених у кількісній шкалі, відбувалася за допомогою коефіцієнта рангової кореляції P .Spearman — r. Для порівняння середніх значень кількісної, нормально розподіленої ознаки у групах, число яких більше двох, користувалися параметричним однофакторним аналізом варіацій (ANOVA). Усі статистичні процедури проводили з використанням пакетів прикладних програм «Microsoft Excel 2000» (Microsoft), «STATISTICA for Windows 6.0» (StatSoft Inc.).
Результати та їх обговорення
Результати аналізу отриманих показників свідчать, що частіше відзначаються традиційні фактори ризику у пацієнтів із СЧВ: тютюнопаління, абдомінальне ожиріння, АГ, дисліпідемія (підвищений рівень ЗХС, ТГ) (табл. 1).
Серед існуючих факторів ризику атеросклерозу істотне місце посідає тютюнопаління, тобто це найбільший, але керований фактор ризику розвитку атеросклерозу [13]. При опитуванні досліджуваних нами пацієнтів 11 палять, що становить 35%, причому частка осіб чоловічої статі більша порівняно з жінками в 2,5 раза (див. табл. 1).
За сучасними уявленнями важливий внесок у формування розвитку атеросклерозу вносить надмірна маса тіла. За даними В.М. Коваленка (2006) в Україні у 58,8% осіб — надмірна маса тіла [2]. За нашими даними у 17 (56,7%) хворих встановлений ІМТ >25 кг/м, з них у 13 (43,3%) хворих на СЧВ надмірна маса тіла, ожиріння — у 4 (13,3%) хворих. Підвищення показника окружності талії було виявлено у 21 (70%) пацієнта із СЧВ, причому лише у 14 (66,7%) з них був підвищений ІМТ. Серед пацієнтів контрольної групи більш розповсюдженим було підвищення ІМТ — у 226 (77%) хворих, збільшення окружності талії при цьому спостерігалось у 190 (64,8%) випадків. Таким чином, для діагностики ожиріння серед пацiєнтів із СЧВ бiльш значущим була окружність талії, нiж IМТ, що швидше за все пов’язано з розвитком синдрому Кушинга у цих осіб [15].
Найбільш поширений стандартний фактор ризику серцево-судинних ускладнень та атеросклерозу — артеріальна гіпертензія [9]. Підвищення артеріального тиску при СЧВ зазвичай є наслідком ураження нирок, терапії ГКС. За даними різних вчених артеріальну гіпертензію виявляють у 12–49% хворих на СЧВ [9]. Згідно з результатами нашого дослідження артеріальна гіпертензія виявлена у 20 (67%) обстежених хворих на СЧВ (середнє значення САТ — 154,00±20,18 мм рт. ст., ДАТ — 90,00±18,36 мм рт. ст.) (див. табл. 1), з них у 18 (90%) хворих виявлена систолічна гіпертензія, у 2 — ізольована діастолічна гіпертензія.
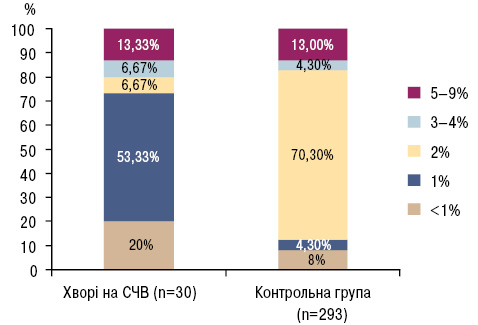
Гіперліпідемія — ще один важливий фактор ризику розвитку атеросклерозу. Серед обстежених основної групи гіперліпідемія була виявлена у 15 (50%) хворих (у контрольній групі — у 135 (46%), а саме: підвищення рівня ЗХС — у 15 (50%) обстежених, підвищення рівня ТГ встановлено у 3 (10%) хворих. Середній рівень ЗХС — 5,90±0,36 ммоль/л, ТГ — 1,44±0,11 ммоль/л (див. табл. 1), у контрольній групі — 4,82±0,25 та 1,12±0,08 ммоль/л відповідно, відмінності між цими групами достовірні.
Частота поєднання основних факторів ризику у хворих на СЧВ та серед пацієнтів контрольної групи відображена на рис. 1.

Згідно з даними літератури частота виявлення бляшок сонних артерій у хворих на СЧВ становить 17–41% [14, 21, 23]. Серед обстежених пацієнтів комплекс інтима-медіа був збільшений у 16 (53,3%).
Реактивна гіперемія була порушена у 10 (33,3%) обстежених хворих на СЧВ. Проте слід зазначити, що середні показники як комплексу інтима-медіа, так і реактивної гіперемії були в межах норми (0,92±0,64 мм і 11,07±1,03% відповідно).
За даними літератури у 1998 р. у США госпіталізовано 4951 хворого на СЧВ віком молодше 50 років, причиною якого був атеросклероз, що становить 8,9% всіх госпіталізацій хворих на СЧВ віком молодше 50 років [24]. Вивчаючи прояви факторів ризику атеросклерозу у хворих на СЧВ у віковому аспекті, слід зазначити, що вже у середньому віці спостерігається підвищений рівень ЗХС, який згодом має тенденцію до збільшення (у хворих віком 45–59 років рівень ЗХС підвищився на 17,8%) (табл. 2).
| Показник | 30–44 роки (n=15) | 45–59 років (n=15) |
|---|---|---|
| ЗХС, ммоль/л | 5,60±1,01 | 6,82±1,11 |
| ТГ, ммоль/л | 1,43±0,50 | 1,40±0,65 |
| Комплекс інтима-медіа, мм | 0,74±0,69 | 1,40±0,50* |
| ЕЗВД, % | 13,07±1,74 | 10,34±2,24* |
*Достовірність відмінностей між віком 30–44 роки та 45–59 років у хворих на СЧВ (р<0,05).
При аналізі виявлено достовірні зміни з боку екстракраніальних та периферичних судин. Так, комплекс інтима-медіа збільшився у пацієнтів із СЧВ віком 45–59 років на 47,14% (p<0,05) порівняно із хворими віком від 30 до 44 років, при цьому спостерігався позитивний кореляційний зв’язок між віком та комплексом інтима-медіа (r=0,37; p<0,05) (рис. 2).
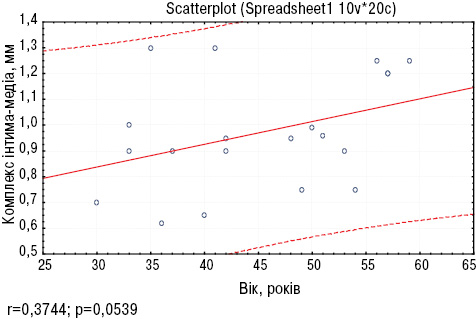
Слід зазначити, що показник проби з реактивною гіперемією (ЕЗВД) залишався у межах норми, проте з віком також достовірно підвищився на 20,9% (p<0,05), що може бути пов’язане з особливостями вікової фізіології [11].
10-річний ризик фатальних серцево-судинних подій за шкалою SCORE у обстежених хворих становив в середньому 1,0±0,89%, що вважається низким рівнем ризику. При цьому лише у 5 пацієнтів відзначено 10-річний фатальний ризик ≥5% (рис. 3). Серед пацієнтів контрольної групи ризик фатальних серцево-судинних подій за шкалою SCORE — 2,67±0,36%. При аналізі отриманих даних встановлено достовірний прямий зв’язок між підвищенням показника комплексу інтима-медіа та рівнем ризику фатальних подій за шкалою SCORE при СЧВ (r=0,69; p<0,05), а також достовірний прямий взаємозв’язок між підвищенням показника проби з реактивною гіперемією та рівнем ризику фатальних подій (r=0,71; p<0,05), достовірний прямий зв’язок між зростом рівня холестерину та ризиком фатальних подій (r=0,83; p<0,05). У обстежених, в яких не було виявлено ознак атеросклерозу, рівень ризику фатальних подій за шкалою SCORE був дуже низьким (в середньому <1%), у той час у всіх хворих із встановленим субклінічним атеросклерозом був у межах від 1 до 5% (в середньому 1,4±0,81%).
Таким чином, використання лише класичних факторів ризику дозволяє зробити висновок, що у пацієнтів із СЧВ ризик розвитку фатальних серцево-судинних ускладнень є низьким, та, як мінімум, відповідає популяційним показникам. Це, безумовно, суперечить наведеним даним про підвищену частоту несприятливих серцево-судинних ускладнень у хворих на СЧВ.
У зв’язку з цим особливе значення може мати аналіз додаткових (чи «нових») кардіоваскулярних факторів ризику: рівень СРБ, фібриногену, тромбоцитів у периферійній крові, активність фактора Віллебранда, активність антитромбіну III, фібринолітичну активність плазми крові, рівень циркулюючих ендотеліальних клітин та функціональний стан ендотелію. Також слід розглянути питання щодо додаткового обстеження на виявлення атеросклерозу серед хворих на СЧВ із низьким ризиком за шкалою SCORE та віднесення пацієнтів із СЧВ до групи високого ризику серцево-судинних ускладнень.
У численних доповідях відзначається, що терапія ГКС сприяє розвитку атеросклеротичного процесу. При аналізі отриманих даних встановлено достовірний взаємозв’язок між зростом активності процесу при СЧВ та підвищенням дози ГКС (r=0,68; p<0,05). Слід зазначити, що підвищення дози ГКС сприяло збільшенню товщини комплексу інтима-медіа (r=0,60; p<0,01) (рис. 4), що, у свою чергу, є несприятливим прогностичним фактором, але при цьому покращувалися показники проби з реактивною гіперемією (r=0,33; p<0,05).
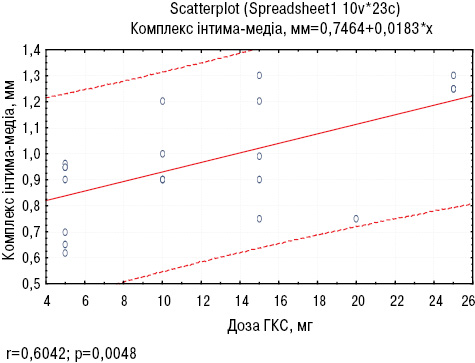
Проте встановлено, що негативний вплив на стан показників проби з реактивною гіперемією надавала саме тривалість застосування ГКС, незалежно від дози препарату (r=–0,21; p<0,05), при цьому також спостерігалося потовщення комплексу інтима-медіа (r=–0,26; p<0,05), що дає змогу вважати пріоритетність саме пульс-терапії у хворих на СЧВ на початку захворювання, а в подальшому — прийом підтримувальної дози ГКС.
Ряд досліджень свідчить про те, що терапія ГКС сприяє значним порушенням ліпідного балансу у хворих на СЧВ [1]. За нашими даними спостерігався незначний кореляційний зв’язок між тривалістю терапії ГКС та рівнями ЗХС і ТГ (r=0,17; p<0,05 і r=0,16; p<0,05 відповідно). Слід зазначити, що зміни показників ЗХС та ТГ асоціювалися із тривалістю захворювання (r=0,18; p<0,05 і r=0,16; p<0,05 відповідно).
Встановлено, що з підвищенням дози ГКС, а також зі збільшенням тривалості ГКС терапії підвищувався ризик фатальних ускладнень за шкалою SCORE (r=0,21; p<0,05 і r=0,23; p<0,05 відповідно).
Висновки
Встановлено, що у пацієнтів із СЧВ серед традиційних факторів ризику пріоритетними є ожиріння (55% випадків), артеріальна гіпертензія (67% випадків) та дисліпідемія (50% випадків). За показниками реактивної гіперемії та визначення комплексу інтима-медіа у 53,3% обстежених хворих встановлені ознаки субклінічного атеросклерозу.
10-річний ризик фатальних серцево-судинних подій за шкалою SCORE у хворих на СЧВ становив у середньому 1,0±0,89%, що вважається низким рівнем ризику та не перевищує середьопопуляційного рівня. Можливо, саме додаткові фактори відповідають за високий ризик розвитку серцево-судинних ускладнень при СЧВ, що потребує подальшого більш глибокого дослідження.
Література
1. Дядик А.І., Багрій О.Е. (2003) Системний червоний вовчак. Регіон, Донецьк, 463 с.
2. Коваленко В.М. (2006) Динаміка показників стану здоров’я населення України за 1999–2005 роки. Аналітичний посібник, 72 с.
3. Коваленко В.М., Шуба Н.М. (2002) Номенклатура, класифікація, критерії діагностики та програми лікування ревматичних хвороб. Катран груп, Київ, 214 с.
4. Про затвердження протоколів надання медичної допомоги за спеціальністю «Ревматологія»: Наказ МОЗ України № 676 від 12.10.2006 [електронний ресурс] / Офіційний сайт МОЗ України // Режим доступу: (http://www.moz.gov.ua/ua/portal/dn_20061012_676.html).
5. Рекомендації Європейського товариства кардіологів ЕSС — European Society of Cardiology (2008).
6. American College of Cardiology: 55th Annual Scientific Sessions (2005) Atlanta, Georgia, USA, р. 95.
7. Bruce I.N. (2005). Atherosclerosis and autoimmune disease: the model of lupus. Lupus, 14(9): 687–690.
8. Bruce I.N., Gladman D.D., Urowitz M.B. (2000) Premature atherosclerosis in systemic lupus erythematosis. Rheum. Dis. Clin. N.A.: 533–539.
9. Bruce I.N., Gladman D.D., Urowitz M.B. (2003) Risk factors for coronary heart disease in women with systemic lupus erythematosus: the Toronto Risk Factor study. Arthitis Rhem., 43(11): 3159–3167.
10. Bruce I.N., Gladman D.D., Urowitz M.B. et al. (2006) The natural history of hyperholesterolaemia in systemic lupus erythematosus. J. Rheumatol., 26: 2137–2143.
11. Cai H., Harrison D.O. (2007) Endothelial dysfunction in cardiovascular disease: the role of oxidant stress. Circ. Res., 87: 840–844.
12. Celermajer D.S. (2007) Endothelial dysfunction: does it matter? It is relevant? J. Am. Coll. Cardiology, 30: 325—333.
13. Doria A. et al. (2002) Risk factors for subclinical atherosclerosis in a prospective cohort of patient with systemic lupus erythematosus. Ann. Rheum. Dis., 62: 1071–1077.
14. Frieman A., Bird Q. (2004) Cutaneous effecta of smoking. J. Cutan. Mod. Surg., 8 (6): 415–423.
15. Janssen I., Katzmarzyk P.T., Ross R. (2008) Body Mass Index Is Inversely Related to Mortality in Older People After Adjustment for Waist Circumference. Am. J. Clin. Nutr, 75: 683–688.
16. Manzi S. et al. (1997) Age-spicific incidence rates of myocardial infarction and angina in women with systemic lupus erythematosus: comparison with the Framingham Study. Am. J. Epidemol.: 408–415.
17. Manzi S. (2000) Systemic lupus erythematosus: a model for atherogenesis? Rheumatology, 39: 353–359.
18. Peterson M.J., Symmons D.P., McCarrey D.W. et al. (2008) Cardiovascular risk management in patients with rheumatoid arthritis and other types of inflammatory arthritis — EULAR TASK FORCE «Cardiovascular risk management in RA». Ann. Rheum. Dis., 67(II): 310.
19. Petri M. (2006) Cardiovascular morbidity in the Hopkins Lupus Cohort. In. Atherosclerosis and autoimmunity. Y. Schoenfeld, D. Harats, G. Wick (Eds) Elsevier, р. 249–254.
20. Roman M.J. et al. (2003) Prevalence and correlates of accelerated atherosclerosis in systemic lupus erythematosus. N. Eng. J. Med., 349: 2399–2406.
21. Roman M. et al. (2001) Prevalence and relation to risk factors of carotid atherosclerosis and left ventricular hypertrophy in systemic lupus erythematosus. Am. J. Cardiol., 87(5): 663–666.
22. Selzer F. et al. (2004) Comparison risk factors for vascular disease in the carotid artery and aorta in woman with systemic lupus erythematosus. Arthritis Rheum., 50(1): 151–159.
23. Stahi-Hallengren C., Jonsen A. (2005) Incidence studies of systemic lupus erythematosus in Southern Sweden: increasing age, decreasing frequency of renal manifestations and good prognosis. J. Rheumatol., 27(3): 685–691.
24. Thorbura C., Ward M. (2003) Hospitalisations for coronary artery disease among patients with systemic lupus erythematosus. Arthritis Rheum., 43(9): 2519–2523.
25. Turiel M., Peretti R. (2005) Cardiac imaging techniques in systemic autoimmune diseases. Lupus,14(9): 727–731.
26. Urowitz M., Gladman D. (1999) Atherosclerosis and systemic lupus erythematosus. Curr. Rheumatol. Rep., 2(1): 19–23.
27. Ward M.M. (2008) Premature morbidity from cardiovascular and cerebrovascular disease in women with systemic lupus erythematosus. Arthr. Rheum., 42: 338–346.
28. Zampieri S., Laccarino L. (2005) Systemic lupus erythematosus, atherosclerosis, and autoantibodies. Ann. NY Acad. Sci., 1051: 351–356.
Адреса для листування:
Курята Олександр Вікторович
49044, Дніпропетровськ, вул. Дзержинського, 9
Дніпропетровська державна медична академія,
кафедра госпітальної терапії № 1 та профпатології

Leave a comment